1. 领域背景与文献引入
文献英文标题:FAK-dependent activation of src family kinase member BLK contributed to endometrial fibrosis via endoplasmic reticulum stress;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:生殖医学-宫腔粘连与子宫内膜纤维化
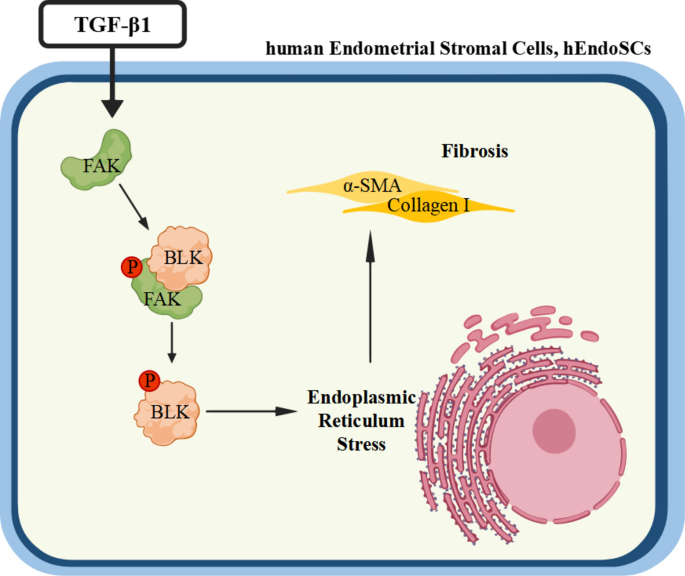
宫腔粘连(IUA)是临床常见的女性生殖系统疾病,主要由宫腔操作或感染引发,核心病理特征为子宫内膜纤维化,表现为宫腔内无血管纤维组织过度沉积,可导致闭经、不孕等严重临床结局。领域共识:目前IUA的治疗手段以宫腔镜粘连分离术为主,但术后复发率高,缺乏针对纤维化病理机制的靶向治疗策略。Src家族激酶(SFKs)作为非受体酪氨酸激酶,已被证实参与肝、肺等多器官纤维化进程,但其成员BLK在子宫内膜纤维化中的功能尚未明确;内质网应激(ERS)在纤维化中的调控作用已有报道,但在子宫内膜纤维化中的具体调控通路仍未阐明。本研究针对BLK在子宫内膜纤维化中的功能及调控机制展开探究,填补了该领域的研究空白,为IUA的靶向治疗提供了新的潜在靶点。
2. 文献综述解析
作者首先系统梳理了子宫内膜纤维化的病理机制,明确肌成纤维细胞活化与细胞外基质(ECM)过度沉积是核心驱动事件,转化生长因子-β1(TGF-β1)是诱导肌成纤维细胞分化的关键细胞因子。随后,作者对SFKs在纤维化中的研究进展进行分类综述,指出SRC、FYN等多个SFK成员已在肝、肺纤维化中被证实具有促纤维化作用,但BLK作为SFK成员,其在纤维化尤其是子宫内膜纤维化中的功能尚未得到实验验证;同时,作者综述了ERS在纤维化中的作用,ERS通过GRP78、CHOP等标志物介导细胞凋亡、ECM沉积等过程,但在子宫内膜纤维化中的上游调控机制仍不清晰。
作者进一步分析现有研究的局限性,指出当前针对IUA的研究多聚焦于临床治疗技术改进,缺乏对纤维化核心调控分子的机制探究,尤其是BLK与FAK、ERS的调控关系未被揭示,导致IUA的靶向治疗靶点匮乏。本研究的创新价值在于,首次通过临床样本、细胞实验与动物模型的多维度验证,明确了BLK作为FAK下游激酶,通过激活ERS通路促进子宫内膜纤维化的作用机制,为IUA的靶向治疗提供了新的分子靶点,弥补了现有研究的空白。
3. 研究思路总结与详细解析
本研究采用“临床样本观察-细胞功能验证-动物模型验证-分子机制探究”的闭环研究思路,核心目标是明确BLK在子宫内膜纤维化中的功能及调控机制,核心科学问题为BLK如何被激活并通过ERS通路促进子宫内膜纤维化。研究通过多维度实验验证,逐步揭示了FAK-BLK-ERS轴在子宫内膜纤维化中的调控作用。
3.1 临床与动物模型中BLK及ERS标志物表达特征分析
实验目的:验证BLK在纤维化子宫内膜组织中的表达及活化状态,同时检测ERS标志物的表达水平,明确BLK与子宫内膜纤维化的相关性。方法细节:收集宫腔粘连(IUA)患者的子宫内膜组织及小鼠IUA模型子宫组织,采用Masson三色染色观察胶原沉积,免疫组化(IHC)检测BLK磷酸化水平,Western blot与实时荧光定量PCR(RT-qPCR)检测BLK、磷酸化BLK(p-BLK)、ERS标志物GRP78、CHOP及纤维化标志物Collagen I、α-平滑肌肌动蛋白(α-SMA)的表达。结果解读:Masson染色显示IUA患者子宫内膜胶原沉积显著增加(n=6,P<0.001),IHC与Western blot结果显示,IUA患者及小鼠模型中BLK mRNA与蛋白表达显著上调,p-BLK水平升高,同时GRP78、CHOP、Collagen I、α-SMA的表达也显著增加(n=6,P<0.05),提示BLK活化与ERS激活、子宫内膜纤维化密切相关。
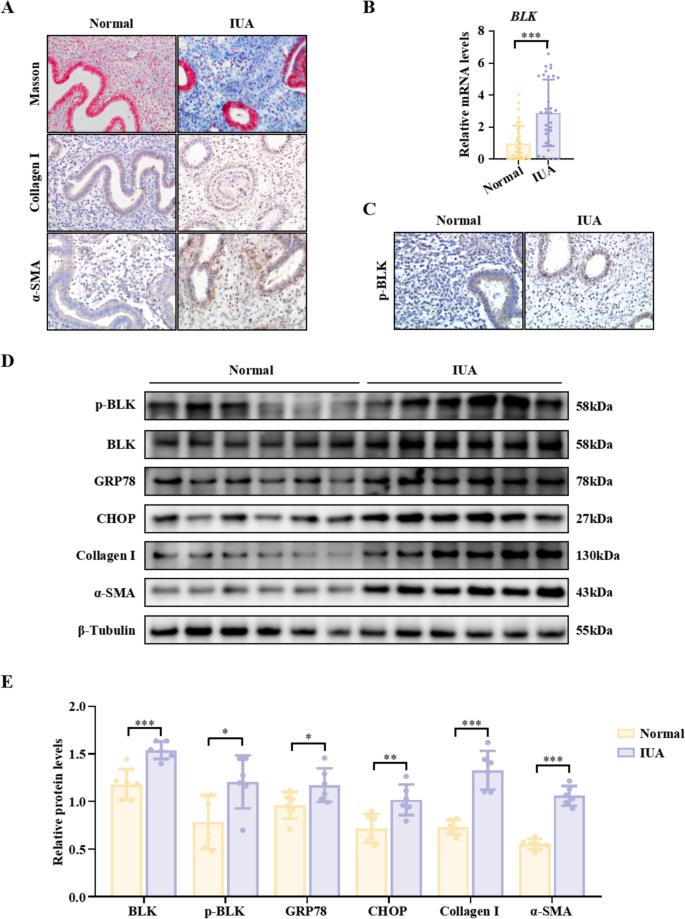
实验所用关键产品包括Novoprotein的重组人TGF-β1(Cat#CA59)、MedChemExpress的小分子抑制剂等,抗体购自商业供应商(详见补充材料Table S1)。
3.2 细胞实验中BLK对子宫内膜纤维化的调控功能验证
实验目的:在细胞水平验证BLK敲低或抑制对TGF-β1诱导的子宫内膜基质细胞(hEndoSCs)纤维化的影响。方法细节:分离原代hEndoSCs,用10 ng/mL TGF-β1诱导纤维化模型,采用小干扰RNA(siBLK)敲低BLK表达,或用Src家族激酶抑制剂SU6656以梯度浓度处理细胞,通过Western blot、免疫荧光检测纤维化标志物与ERS标志物的表达。结果解读:SU6656以剂量依赖性方式抑制p-BLK表达,5 μM与10 μM浓度下p-BLK表达分别降低(n=3,P=0.018、P=0.002),同时GRP78、CHOP、Collagen I、α-SMA的表达也显著降低;siBLK敲低后,TGF-β1诱导的上述标志物表达被显著抑制(n=3,P<0.05),免疫荧光结果进一步证实Collagen I与α-SMA的表达减少,提示BLK具有促子宫内膜纤维化的功能。
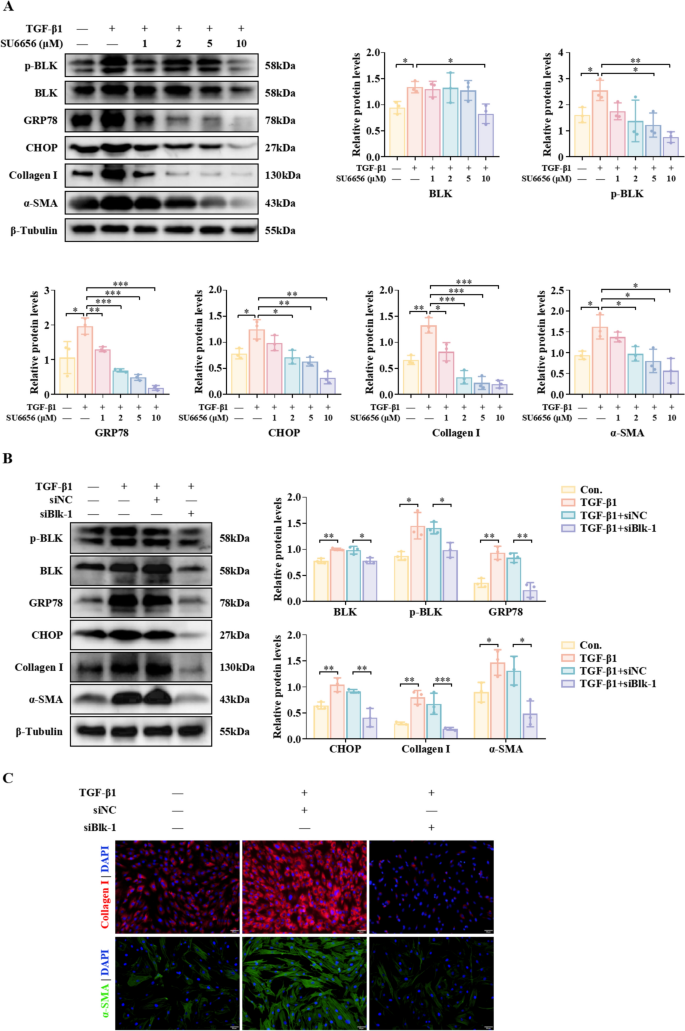
实验所用关键产品:siRNA由HANBIO设计合成,转染试剂为GenePharma的GP-transfect-Mate(Cat#G04009)。
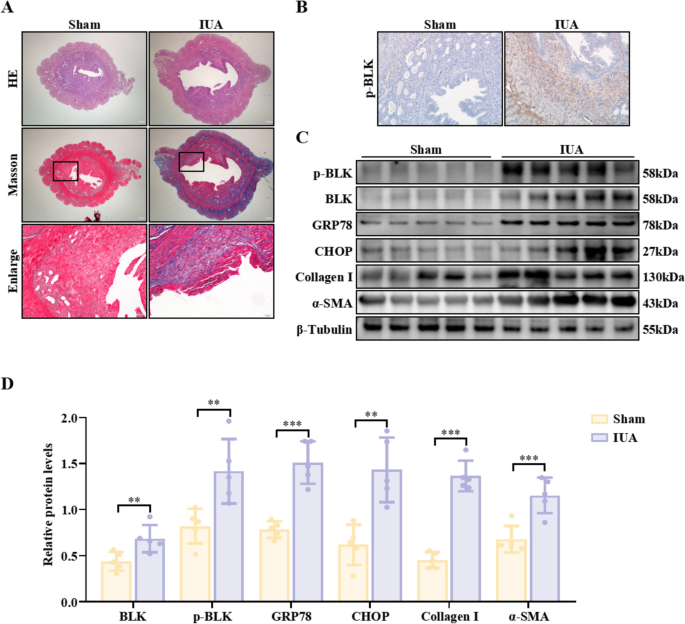
3.3 动物模型中BLK敲低对子宫内膜纤维化的改善作用验证
实验目的:在体内验证BLK敲低对IUA模型小鼠子宫内膜纤维化的改善效果。方法细节:构建子宫内膜特异性Blk敲低的IUA小鼠模型(IUA^{Blk[LKD]}),通过慢病毒注射实现Blk的组织特异性敲低,采用H&E染色观察子宫内膜形态,Masson染色检测胶原沉积,IHC与Western blot检测纤维化标志物与ERS标志物的表达。结果解读:H&E染色显示,IUA^{Blk[LKD]}小鼠的子宫内膜厚度较IUA模型小鼠显著增加(n=6,P=0.008),腺体与血管数量增多(n=6,P=0.009、P=0.001);Masson染色显示胶原沉积显著减少;Western blot与RT-qPCR结果显示,GRP78、CHOP、Collagen I、α-SMA的表达显著降低,提示BLK敲低可有效改善子宫内膜纤维化。
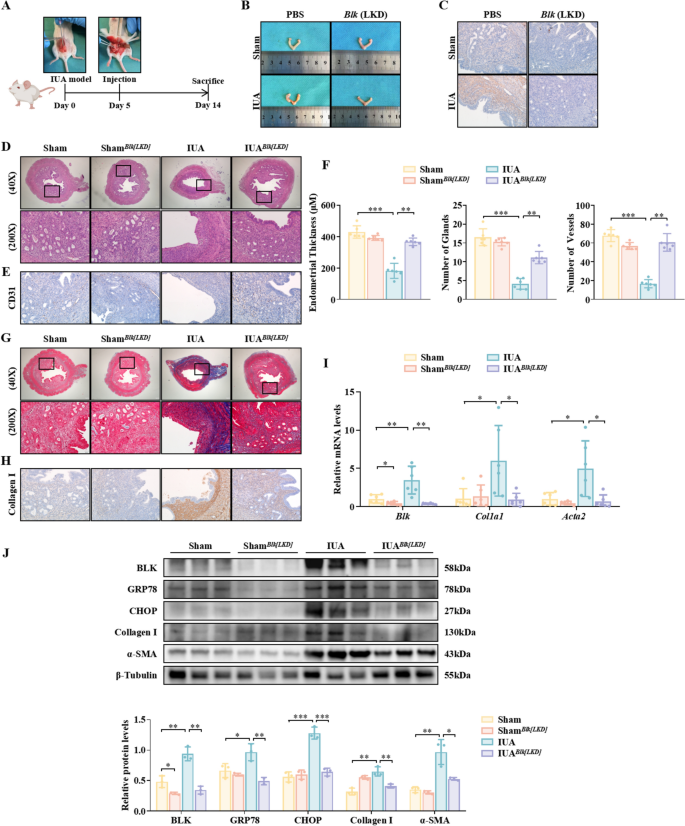
实验所用关键产品:Blk敲低慢病毒购自ABM(武汉)。
3.4 BLK通过ERS通路调控子宫内膜纤维化的机制验证
实验目的:明确BLK是否通过ERS通路介导子宫内膜纤维化。方法细节:用ERS抑制剂4-苯基丁酸(4PBA)与激活剂α-硫辛酸(α-LA)处理TGF-β1诱导的hEndoSCs,通过Western blot、免疫荧光检测纤维化标志物的表达;同时采用荧光探针检测细胞内Ca^{2+}浓度,验证ERS的激活状态。结果解读:TGF-β1诱导的hEndoSCs中Ca^{2+}浓度显著升高(n=5,P=0.003),提示ERS激活;4PBA处理显著抑制Collagen I与α-SMA的表达(n=3,P=0.027、P=0.008),α-LA处理则促进其表达(n=3,P=0.037、P=0.043);BLK敲低对纤维化的抑制作用可被α-LA逆转,提示BLK通过ERS通路调控子宫内膜纤维化。
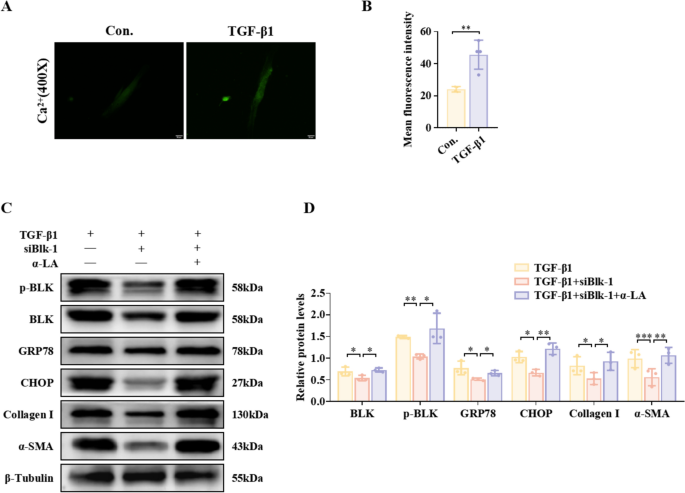
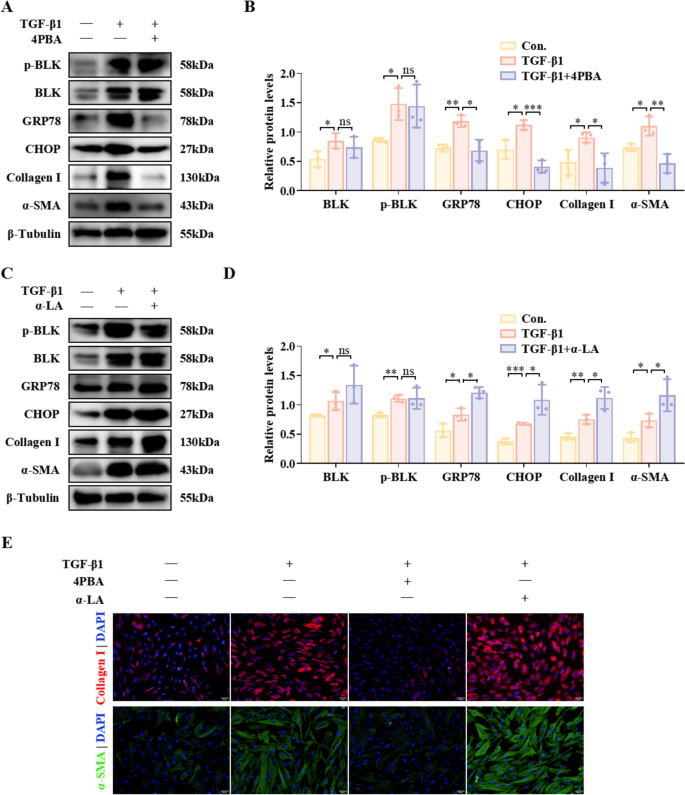
实验所用关键产品:4PBA与α-LA购自MedChemExpress。
3.5 BLK的激活依赖于与FAK的相互作用
实验目的:探究BLK的上游激活机制,明确FAK与BLK的相互作用关系。方法细节:检测IUA患者与小鼠模型中FAK的表达水平,用FAK抑制剂Y15处理TGF-β1诱导的hEndoSCs,通过Western blot检测p-BLK及下游标志物的表达;采用免疫共沉淀(Co-IP)、免疫荧光验证BLK与FAK的相互作用,通过分子对接预测两者的结合模式。结果解读:IUA患者与小鼠模型中FAK与p-FAK的表达显著上调;Y15处理显著抑制p-BLK的表达(n=3,P=0.005),但不影响总BLK的表达,同时GRP78、CHOP、Collagen I、α-SMA的表达也被抑制;Co-IP与免疫荧光结果证实BLK与FAK直接结合,分子对接显示两者存在14个氢键结合位点,提示BLK的激活依赖于与FAK的相互作用。
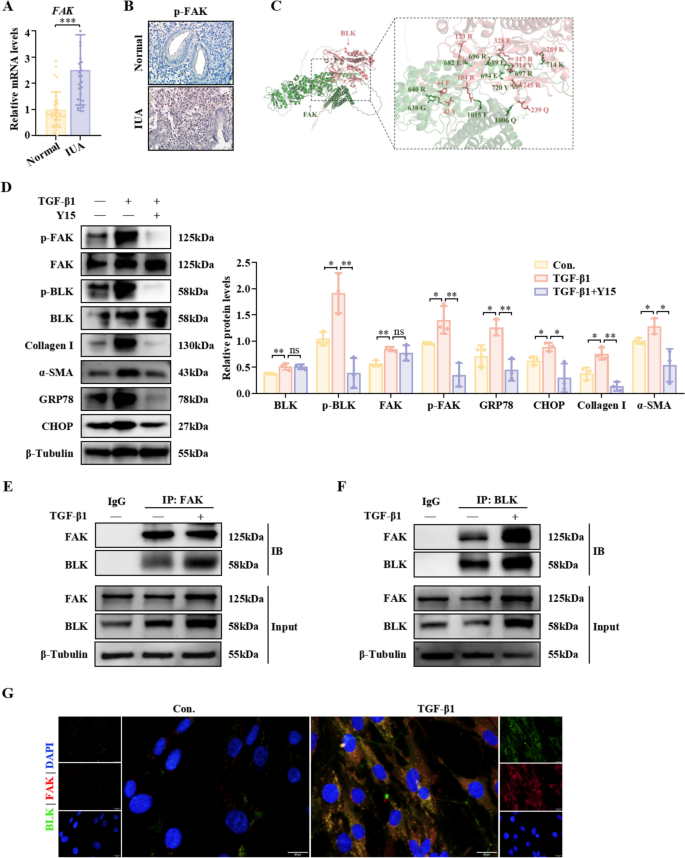
实验所用关键产品:FAK抑制剂Y15购自MedChemExpress,Co-IP试剂盒购自Absin(Cat#abs955)。
4. Biomarker研究及发现成果
本研究中,BLK被定位为子宫内膜纤维化的潜在治疗靶点Biomarker,筛选与验证逻辑为:首先通过RNA-seq分析IUA患者子宫内膜样本,发现BLK是唯一显著上调的Src家族激酶成员,随后通过临床样本、细胞实验、动物模型的多维度验证,明确了BLK的促纤维化功能及调控机制。
Biomarker的来源为IUA患者的子宫内膜组织、小鼠IUA模型的子宫组织及原代hEndoSCs,验证方法包括免疫组化、Western blot、RT-qPCR、Co-IP等多种实验技术。特异性方面,BLK仅在纤维化子宫内膜组织中显著上调,在正常子宫内膜组织中表达水平较低;敏感性方面,IUA患者子宫内膜中BLK mRNA表达显著升高(n=6,P<0.001),p-BLK的表达水平也显著增加(n=6,P=0.026)。
核心成果方面,BLK作为FAK下游的促纤维化激酶,通过激活ERS通路促进子宫内膜纤维化,其敲低可显著改善IUA模型小鼠的子宫内膜纤维化程度,子宫内膜厚度增加(n=6,P=0.008),腺体与血管数量增多(n=6,P=0.009、P=0.001)。本研究首次揭示了BLK与FAK、ERS的调控关系,证实BLK是子宫内膜纤维化的潜在治疗靶点,为IUA的靶向治疗提供了新的分子依据,具有重要的临床转化价值。