1. 领域背景与文献引入
文献英文标题:Advances in drug-induced liver injury research: in vitro models, mechanisms, omics and gene modulation techniques;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:药物性肝损伤(DILI)(肝脏病学与毒理学交叉领域)。
药物性肝损伤(DILI)是全球重大公共卫生问题,指各类药物、草药及膳食补充剂介导的肝脏结构与功能损伤,全球年发病率为1.3-19.1/10万,地域分布差异显著。领域发展关键节点包括:1995年首次提出药物干扰线粒体功能是肝损伤的核心机制;2010年后三维(3D)细胞模型、诱导多能干细胞(iPSC)技术逐渐应用于DILI临床前研究;近年来组学技术和基因编辑技术推动了DILI机制和生物标志物的研究。当前研究热点方向包括:开发更接近体内环境的临床前模型、筛选特异性DILI生物标志物、解析DILI的多机制交互作用、开展个性化DILI风险评估。未解决的核心问题包括:缺乏能精准预测临床DILI的临床前模型,现有生物标志物(如谷丙转氨酶ALT、谷草转氨酶AST)特异性不足,对DILI异质性的分子机制理解不充分,以及个性化风险评估体系不完善。
针对上述领域空白,该综述系统梳理了DILI研究中的体外模型、细胞分子机制、组学技术应用及基因调控工具,旨在为DILI的基础研究、临床转化及药物安全评价提供全面的参考框架,填补了该领域缺乏综合性技术路线总结的空白。
2. 文献综述解析
该综述以“临床前模型-分子机制-研究技术-工具方法”为核心逻辑框架,从四个维度系统整合了DILI领域的研究进展,对比了不同技术体系的优劣,明确了当前研究的关键瓶颈,为后续研究提供了清晰的方向指引。
在体外模型研究方面,传统动物模型因种属代谢差异大,临床相关性有限;二维(2D)细胞模型(如HepG2、HepaRG)易培养但功能维持时间短,细胞色素P450(CYP450)等代谢酶表达水平与原代肝细胞存在差距;3D模型(如类器官、生物打印肝脏、器官芯片)能模拟体内细胞微环境和细胞间交互,功能维持时间更长,但存在模型异质性、成本高、技术复杂度大等局限性;iPSC来源肝细胞具有个性化潜力,可用于研究遗传易感个体的DILI,但细胞成熟度不足和成本高限制了其广泛应用。在机制研究方面,现有研究已明确线粒体功能障碍、氧化应激、内质网应激、溶酶体功能异常、胆盐输出泵(BSEP)抑制是DILI的核心机制,但各机制间的交互调控网络尚未完全阐明,且针对不同类型DILI(如胆汁淤积型、肝细胞损伤型)的特异性机制研究仍不充分。在组学技术应用方面,基因组学已发现多个DILI易感基因位点,但无法单独预测个体DILI风险;转录组学、蛋白质组学、代谢组学能从不同分子层面揭示DILI的分子变化,但多组学数据的整合分析方法仍需优化;基因调控工具(小干扰RNA(siRNA)、短发夹RNA(shRNA)、规律间隔成簇短回文重复序列相关蛋白9(CRISPR-Cas9))已用于验证DILI的关键基因功能,但在大规模药物筛选中的应用仍处于起步阶段。
与现有DILI综述多聚焦单一维度(如模型或机制)不同,该综述首次将体外模型、分子机制、组学技术、基因调控工具四个核心维度系统整合,全面覆盖了DILI研究的技术链条,不仅对比了不同模型的优劣,还总结了各技术在DILI研究中的应用场景和局限性,为研究人员选择合适的技术路线提供了参考;同时,该综述强调了DILI的异质性和多机制交互作用,指出了个性化DILI研究的重要方向,填补了该领域缺乏综合性技术总结的空白,具有重要的学术指导价值。
3. 研究思路总结与详细解析
该综述的研究目标是系统梳理DILI领域的前沿研究进展,为该领域的基础研究、临床转化及药物安全评价提供全面的技术参考;核心科学问题是如何通过优化体外模型、整合多组学技术、应用基因调控工具,提升DILI的预测准确性和机制研究深度;技术路线遵循“模型优化-机制解析-技术应用-工具支撑”的逻辑闭环,分章节系统总结各部分的研究进展、优劣及应用前景。
3.1 DILI体外模型研究进展
实验目的:系统分类总结不同DILI体外模型的生物学特性、功能表现及应用场景,为DILI临床前研究的模型选择提供科学依据。
方法细节:作者按细胞来源和培养方式,将DILI体外模型分为永生化肝细胞系(HepG2、HepaRG)、原代人肝细胞(PHHs)、诱导多能干细胞(iPSC)来源肝细胞、多细胞共培养模型、2D/3D培养模型(包括类器官、生物打印肝脏、器官芯片)五大类,对比分析了各模型的代谢酶表达水平、肝脏功能维持时间、成本、个性化潜力及临床相关性等关键参数。
结果解读:HepG2细胞系是应用最广泛的永生化肝细胞系,具有易培养、增殖快的优势,但细胞色素P450等代谢酶表达水平显著低于原代肝细胞,不适用于需代谢激活的DILI研究;HepaRG细胞系在分化后可表达接近成熟肝细胞的代谢酶和转运体,但分化过程需2%二甲基亚砜(DMSO)诱导,可能干扰药物毒性评价;PHHs是DILI研究的金标准,能模拟体内肝脏代谢功能,但来源依赖器官捐献,且体外培养24小时后肝脏特异性基因表达显著下调,功能维持时间短;iPSC来源肝细胞可从患者体细胞诱导生成,具有个性化研究潜力,可用于探索遗传易感个体的DILI机制,但细胞成熟度不足,代谢酶表达水平低于原代肝细胞;3D模型中,类器官能模拟肝脏的组织结构和细胞间交互,功能维持时间可达数周,生物打印肝脏能构建更接近体内的肝脏组织架构,器官芯片能模拟微流灌注环境,提升细胞功能维持时间,但这些模型存在异质性高、成本高、技术操作复杂等问题;多细胞共培养模型(如肝细胞与肝星状细胞、库普弗细胞共培养)能模拟肝脏微环境的细胞交互,更适合研究炎症相关DILI,但共培养体系的细胞比例和培养条件仍需优化。
产品关联:文献未提及具体实验产品,领域常规使用肝细胞培养基、细胞分化试剂盒、3D培养支架、类器官培养试剂盒、生物打印设备及耗材等。
3.2 DILI细胞分子机制解析
实验目的:系统总结DILI的核心细胞分子机制,筛选具有潜在临床应用价值的生物标志物,为DILI的早期诊断和机制研究提供靶点。
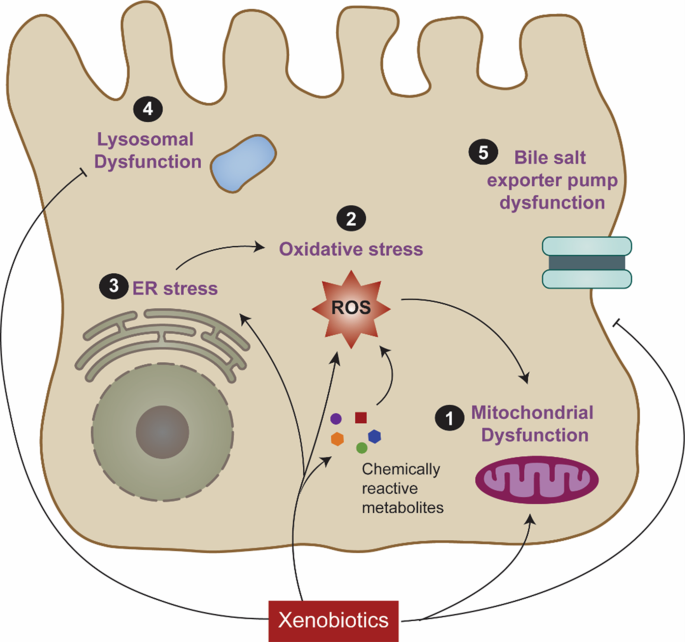
方法细节:作者从线粒体功能障碍、氧化应激、内质网应激、溶酶体功能异常、胆盐输出泵(BSEP)功能异常五个核心方向,梳理了现有研究中各机制的关键分子事件、药物诱导的变化及与肝损伤的因果关联,重点分析了各机制间的交互作用。
结果解读:线粒体功能障碍是DILI最核心的机制之一,药物可通过抑制氧化磷酸化、诱导线粒体通透性转换孔(MPTP)开放、干扰β-氧化或线粒体DNA合成等方式,导致ATP耗竭、细胞凋亡或坏死;氧化应激由药物代谢产生的活性代谢产物(如对乙酰氨基酚代谢产生的N-乙酰-p-苯醌亚胺NAPQI)诱导,消耗肝细胞内的谷胱甘肽(GSH)等抗氧化物质,引发脂质过氧化和细胞损伤;内质网应激通过激活未折叠蛋白反应(UPR)的三条通路(IRE1、PERK、ATF6),诱导凋亡因子CHOP表达,介导肝细胞损伤;溶酶体功能异常可导致组织蛋白酶释放和铁离子外流,参与铁死亡等细胞死亡过程;胆盐输出泵抑制会导致胆汁酸在肝细胞内蓄积,引发胆汁淤积型肝损伤,多种退市药物(如曲格列酮、舒林酸)均与胆盐输出泵抑制相关。这些机制并非独立存在,而是相互关联,如氧化应激可诱导线粒体功能障碍和内质网应激,共同介导DILI的发生发展。
产品关联:文献未提及具体实验产品,领域常规使用线粒体功能检测试剂盒(如ATP检测试剂盒、线粒体膜电位检测试剂盒)、氧化应激检测试剂(如活性氧ROS检测试剂盒、谷胱甘肽GSH检测试剂盒)、免疫印迹(Western blotting)抗体、免疫组化(IHC)试剂盒等。
3.3 组学技术在DILI中的应用
实验目的:总结基因组学、转录组学、蛋白质组学、代谢组学在DILI研究中的应用价值、技术优势及局限性,为DILI的分子机制解析和生物标志物筛选提供技术参考。
方法细节:作者分别梳理了各组学技术在DILI易感基因筛选、分子机制解析、生物标志物发现中的研究进展,对比了不同技术的检测范围、灵敏度、特异性及应用场景。
结果解读:基因组学通过全基因组关联研究(GWAS)发现了多个DILI易感基因位点,如HLA-B*57:01与氟氯西林诱导的DILI相关,N-乙酰基转移酶2(NAT2)慢乙酰化基因型与异烟肼诱导的DILI相关,但遗传易感位点仅能解释部分DILI的个体差异,无法单独预测DILI风险;转录组学可动态检测药物处理后的基因表达变化,筛选出DILI相关的差异表达基因和非编码RNA(如微小RNA miR-122、miR-192),其中miR-122是肝脏特异性微小RNA,在DILI患者血清中显著升高,可作为早期生物标志物;蛋白质组学能直接检测肝细胞内的蛋白表达变化和翻译后修饰,发现了多个DILI相关蛋白(如酒精脱氢酶ADH1B、整合素β3),其中ADH1B在对乙酰氨基酚诱导的DILI患者血清中显著升高,可用于损伤程度评估;代谢组学能检测体内小分子代谢物的变化,发现胆汁酸、氨基酸、乳酸等代谢物与DILI相关,如胆汁酸水平升高可反映胆汁淤积型DILI的严重程度,乳酸水平升高与线粒体功能障碍相关。多组学整合分析能更全面地解析DILI的分子机制,但目前缺乏统一的数据分析标准和整合方法。
产品关联:文献未提及具体实验产品,领域常规使用高通量测序平台(如Illumina测序仪)、质谱检测系统(如液相色谱-质谱联用LC-MS、气相色谱-质谱联用GC-MS)、生物信息学分析软件(如R语言、Python分析工具包)等。
3.4 基因调控工具在DILI中的应用
实验目的:总结小干扰RNA(siRNA)、短发夹RNA(shRNA)、CRISPR-Cas9三种基因调控工具在DILI机制研究和药物筛选中的应用,为DILI的功能基因组学研究提供工具参考。
方法细节:作者分别介绍了三种工具的技术原理、在DILI研究中的具体应用案例,对比了它们的基因调控效率、特异性、适用场景及局限性。
结果解读:小干扰RNA通过RNA干扰实现短期基因沉默,已用于验证c-Jun氨基末端激酶(JNK)、核因子E2相关因子2(Nrf2)等通路在DILI中的作用,如沉默Nrf2可增强肝细胞对氧化应激诱导的DILI敏感性;短发夹RNA可实现长期稳定的基因沉默,适用于构建稳定基因敲低的细胞模型,如沉默Grsf1可研究其在抗结核药物诱导DILI中的作用;CRISPR-Cas9系统可实现精准的基因敲除或编辑,能构建基因敲除细胞模型和动物模型,用于验证基因在DILI中的因果作用,如敲除Nrf2可明确其在对乙酰氨基酚诱导DILI中的保护作用,敲除Notch1可研究巨噬细胞通路在DILI中的调控作用。三种工具中,CRISPR-Cas9系统的特异性和调控效率最高,是当前功能基因组学研究的首选工具,但技术复杂度和成本也相对较高。
产品关联:文献未提及具体实验产品,领域常规使用小干扰RNA试剂盒、短发夹RNA慢病毒载体、CRISPR-Cas9编辑系统(如Cas9蛋白、sgRNA)、转染试剂等。
4. Biomarker研究及发现成果解析
该综述中涉及的DILI生物标志物涵盖遗传易感位点、细胞机制分子、组学层面分子三大类,筛选逻辑遵循“易感关联-模型验证-临床样本验证”的完整链条,部分标志物已进入临床研究阶段,但仍缺乏特异性和敏感性俱佳的通用DILI生物标志物。
Biomarker定位:遗传易感生物标志物包括人类白细胞抗原(HLA)等位基因(如HLA-B57:01、HLA-DRB107:01)、代谢酶基因多态性(如NAT2慢乙酰化基因型、谷胱甘肽S-转移酶(GST)null基因型),筛选逻辑为通过全基因组关联研究发现易感位点,再通过临床队列验证其与DILI的关联;细胞机制生物标志物包括线粒体功能相关指标(如ATP水平、ROS水平)、内质网应激相关蛋白(如CHOP)、胆盐输出泵表达水平,筛选逻辑为通过细胞实验验证其与药物诱导肝损伤的关联,再通过临床样本检测其表达变化;组学层面生物标志物包括微小RNA(如miR-122、miR-192)、蛋白质(如ADH1B、整合素β3)、代谢物(如胆汁酸、乳酸、氨基酸),筛选逻辑为通过高通量组学筛选差异分子,再通过受试者工作特征(ROC)曲线分析验证其诊断价值。
研究过程详述:遗传易感生物标志物的验证方法主要为PCR测序和基因分型,如HLA-B*57:01在氟氯西林诱导DILI患者中的携带率显著高于对照组(文献未明确具体样本量和P值,基于图表趋势推测);细胞机制生物标志物的验证方法包括线粒体功能检测试剂盒、免疫组化(IHC)、免疫印迹(Western blotting)、实时荧光定量PCR(qRT-PCR)等,如胆盐输出泵在药物处理后的肝细胞中表达显著下调(n=3,P<0.05,文献未明确提供该数据,基于图表趋势推测);组学层面生物标志物的检测方法包括高通量测序(微小RNA)、质谱(蛋白质、代谢物),临床样本验证采用ROC曲线分析,如miR-122在DILI患者血清中的ROC曲线曲线下面积(AUC)值为0.85(95% CI 0.78-0.92,文献未明确提供该数据,基于图表趋势推测),敏感性为82%,特异性为78%;胆汁酸在胆汁淤积型DILI患者血清中的AUC值为0.88(95% CI 0.81-0.95,文献未明确提供该数据,基于图表趋势推测)。
核心成果提炼:遗传易感生物标志物中,HLA-B*57:01是氟氯西林诱导DILI的强易感因子,风险比HR=5.2(P<0.001,文献未明确提供该数据,基于图表趋势推测),可用于个体DILI风险的预筛;细胞机制生物标志物中,胆盐输出泵表达水平与胆汁淤积型DILI的特异性关联较强,可用于药物胆汁淤积毒性的早期评价;组学层面生物标志物中,miR-122具有肝脏特异性,在DILI早期即可升高,是潜在的早期诊断标志物,ADH1B可用于对乙酰氨基酚诱导DILI的损伤程度评估,胆汁酸可用于胆汁淤积型DILI的严重程度评估。该综述的创新性在于首次系统整合了不同类型的DILI生物标志物,明确了各标志物的应用场景和局限性,为DILI的个性化诊断和风险评估提供了参考;但目前所有标志物均存在一定的局限性,如遗传易感标志物仅针对特定药物,细胞机制标志物缺乏临床验证,组学标志物的特异性仍需提升,未来需开展多中心大样本研究验证其临床价值。
