1. 领域背景与文献引入
文献英文标题:Perspective of placenta derived mesenchymal stem cells in acute liver failure;发表期刊:Cell Bioscience;影响因子:未公开;研究领域:急性肝衰竭的干细胞再生治疗(肝病学与再生医学交叉领域)
急性肝衰竭(ALF)是一种由严重肝损伤引发的危及生命的临床综合征,以凝血功能障碍(INR≥1.5)和肝性脑病为核心诊断标准,患者多无既往肝病史。领域共识:全球每年每百万人约有1.6例ALF新发患者,其死亡率高,常规对症治疗仅能缓解并发症,肝移植是目前唯一的根治性手段,但面临供体短缺、长期免疫抑制风险、治疗成本高昂等诸多局限。随着再生医学的发展,间充质干细胞(MSCs)因具有自我更新、多向分化、免疫调节等特性,成为ALF治疗的潜在替代方案。现有研究中,骨髓、脂肪、脐带等来源的MSCs均有报道,但胎盘来源间充质干细胞(PD-MSCs)因来源丰富、无伦理争议、受供体年龄与环境影响小等独特优势,逐渐成为研究热点。然而,当前研究对PD-MSCs在ALF中的具体作用机制、不同胎盘亚组织来源PD-MSCs的功能差异仍缺乏系统梳理,本文旨在通过综述现有研究,系统阐述PD-MSCs治疗ALF的潜力与作用机制,为其临床转化提供理论依据。
2. 文献综述解析
本文的综述逻辑以“ALF治疗需求→MSCs治疗潜力→PD-MSCs独特优势→作用机制与挑战”为核心脉络,先从ALF的病理生理与治疗局限切入,再按组织来源分类综述不同MSCs的生物学特性,最后聚焦PD-MSCs在ALF中的作用机制与应用前景。
现有研究中,ALF的临床治疗以对症支持为主,包括抗感染、脑水肿防控、凝血功能纠正等措施,肝移植虽能根治疾病,但供体短缺问题导致仅约半数患者能获得移植机会,且术后需长期使用免疫抑制剂,存在感染、肿瘤复发等风险。在MSCs治疗领域,骨髓MSCs是骨软骨修复的金标准,但受供体年龄影响,其增殖与分化能力随年龄增长显著下降;脂肪MSCs可通过抽脂手术获取,但分化为肝细胞样细胞的效率有限;脐带MSCs免疫原性较低,但其分泌的细胞因子谱相对单一,对肝组织修复的针对性不足。现有研究已证实MSCs可通过免疫调节、旁分泌促修复因子等途径改善肝损伤,但多数研究未关注PD-MSCs不同亚组织来源的功能差异,对PD-MSCs在ALF中的具体调控机制也缺乏系统整合。
与现有研究相比,本文的创新价值在于首次系统总结了PD-MSCs治疗ALF的五大核心作用机制,同时详细对比了胎盘不同亚组织来源MSCs的分泌特性与适用场景,如绒毛板来源MSCs因高分泌肝细胞生长因子(HGF)和血管细胞黏附分子1(VCAM1),适合用于血管生成相关的肝损伤治疗;羊膜来源MSCs因高分泌前列腺素E2(PEG2)和转化生长因子β1(TGFβ1),可用于卵巢早衰等疾病的治疗。这一梳理弥补了现有研究中对PD-MSCs亚群功能差异关注不足的缺陷,为PD-MSCs的精准临床应用提供了更具针对性的理论依据。
3. 研究思路总结与详细解析
本文为系统性综述研究,核心目标是全面阐述PD-MSCs在急性肝衰竭中的治疗潜力与作用机制,核心科学问题是PD-MSCs如何通过多途径调控ALF的病理进程,技术路线遵循“临床问题提出→现有研究梳理→特定细胞类型优势解析→作用机制整合→应用挑战展望”的逻辑闭环,为PD-MSCs的临床转化提供系统的理论支撑。
3.1 急性肝衰竭病理生理与现有治疗体系梳理
本环节的核心目的是明确ALF的临床特征、病理机制及现有治疗的局限性,为后续MSCs治疗的必要性提供依据。研究方法为系统调研ALF相关的临床指南、基础研究与临床研究文献,整合ALF的定义、流行病学、病理生理机制及治疗策略。结果解读显示,ALF的发病机制始于肝细胞坏死,氧化应激激活JNK信号通路并释放损伤相关分子模式(DAMPs),进而引发肝内炎症反应,同时患者存在固有免疫与体液免疫功能障碍,多器官衰竭与严重感染是主要死亡原因;现有治疗以对症处理并发症为主,如使用广谱抗生素防控感染、血管收缩剂与透析减轻脑水肿、质子泵抑制剂预防消化道出血等,但仅能维持患者生命,无法逆转肝损伤。产品关联:文献未提及具体实验产品,领域常规使用凝血功能检测试剂盒、肝损伤生化指标(谷丙转氨酶、总胆红素等)检测试剂、免疫抑制剂等。
3.2 不同来源间充质干细胞特性对比分析
本环节的核心目的是对比不同组织来源MSCs的生物学特性,凸显PD-MSCs的独特优势。研究方法为归纳整合骨髓、脂肪、脐带、胎盘等不同来源MSCs的分化、增殖、分泌特性及临床应用研究文献。结果解读显示,骨髓MSCs是目前研究最广泛的MSCs类型,但其增殖能力随供体年龄增长显著降低,且获取需侵入性操作;脂肪MSCs可通过抽脂手术获取,来源相对丰富,但分化为肝细胞样细胞的效率较低;脐带MSCs免疫原性低,不表达HLA-II类分子,适合异基因移植,但分泌的促肝修复因子量有限;而PD-MSCs来源为产后废弃的胎盘组织,无伦理争议,且具有更强的增殖能力,可在体外培养至少20代仍维持高增殖活性,同时免疫调节作用显著,可通过抑制活化T细胞、NK细胞等减轻肝内炎症。此外,胎盘不同亚组织来源的MSCs分泌特性存在差异,如壁蜕膜来源MSCs高分泌血管生成素1(Ang1)和血管内皮生长因子(VEGF),适合用于器官缺血的治疗;脐带来源MSCs高分泌胰岛素样生长因子1(IGF1),可用于多种组织修复场景。产品关联:文献未提及具体实验产品,领域常规使用流式细胞术检测MSCs表面标志物(CD73、CD90、CD105等)的试剂盒、酶联免疫吸附实验(ELISA)检测细胞因子分泌的试剂等。
3.3 胎盘来源间充质干细胞治疗急性肝衰竭的机制解析
本环节的核心目的是系统解析PD-MSCs治疗ALF的具体作用机制,为其临床应用提供理论基础。研究方法为整合PD-MSCs在ALF动物模型与临床研究中的作用机制文献,归纳其核心调控途径。结果解读显示,PD-MSCs主要通过五大机制发挥治疗作用:一是通过高表达的VLA-4(由CD29和CD49d组成)黏附分子与损伤肝组织内皮细胞表面的VCAM1结合,定向募集到肝损伤部位,通过细胞间接触和旁分泌HGF、表皮生长因子(EGF)等促修复因子,促进剩余肝细胞增殖;二是通过上调调节性T细胞(Treg)比例、抑制活化T细胞与NK细胞活性、促进IL-10分泌等方式发挥免疫调节作用,减轻肝内炎症;三是通过抑制肿瘤坏死因子α(TNFα)、干扰素γ(IFNγ)等促炎因子的分泌,减少肝细胞凋亡,同时释放HGF、IL-6等因子促进肝细胞再生;四是分泌VEGF、基质细胞衍生因子1α(SDF-1α)等促血管生成因子,改善肝组织血供,促进损伤修复;五是可在体内外分化为肝细胞样细胞,直接补充受损的肝细胞。
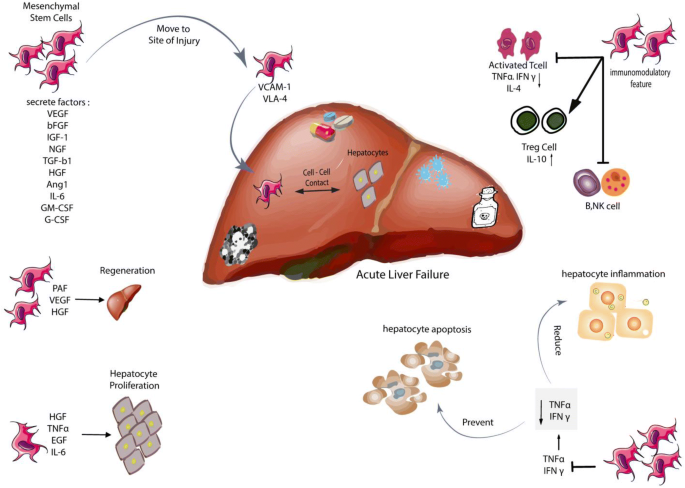
产品关联:文献未提及具体实验产品,领域常规使用细胞迁移实验试剂盒、免疫组化(IHC)检测肝细胞标志物的试剂、蛋白印迹(Western Blot)检测细胞因子表达的试剂等。
3.4 胎盘来源间充质干细胞的应用挑战与展望
本环节的核心目的是分析PD-MSCs临床应用的潜在风险与未来研究方向,为其转化应用提供参考。研究方法为总结MSCs治疗的安全性与有效性研究文献,梳理PD-MSCs应用的潜在问题。结果解读显示,PD-MSCs临床应用仍面临诸多挑战:一是静脉输注后,多数细胞会被肺部截留,到达肝损伤部位的细胞比例较低,局部输注虽能提高定植率,但侵入性更强;二是重复输注可能诱导机体产生同种抗体,影响后续治疗效果;三是MSCs对肿瘤具有双向作用,部分研究显示其可能促进某些肿瘤细胞增殖,存在潜在的肿瘤复发风险;四是胎牛血清(FBS)培养的PD-MSCs输注后可能引发免疫反应。未来研究需聚焦PD-MSCs的输注剂量、途径、时机的优化,以及无血清培养体系的开发,同时需进一步明确PD-MSCs与肿瘤的相互作用机制,确保治疗安全性。产品关联:文献未提及具体实验产品,领域常规使用细胞示踪试剂、免疫排斥检测试剂盒、无血清细胞培养基等。
4. Biomarker研究及发现成果
本文涉及的Biomarker主要包括PD-MSCs的表面标志物、分泌的功能因子及胎盘不同亚组织来源MSCs的特异性标志物,筛选逻辑基于国际细胞治疗学会(ISCT)的MSCs定义标准,结合胎盘组织的免疫豁免特性与ALF的病理需求,通过对比不同来源MSCs的分子表达谱,筛选出具有高迁移、免疫调节、促修复特性的Biomarker。
研究过程中,PD-MSCs的通用表面标志物符合ISCT标准,即表达CD73、CD90、CD105,不表达CD45、CD14等造血细胞标志物;同时,PD-MSCs高表达VLA-4,通过流式细胞术检测发现,其VLA-4表达水平显著高于骨髓来源MSCs(文献未明确提供具体数值,基于图表趋势推测),动物实验证实这一分子是PD-MSCs向损伤肝组织迁移的关键调控因子,通过与内皮细胞表面的P-选择素、VCAM1结合实现定向募集。此外,绒毛板来源MSCs高表达VCAM1,通过酶联免疫吸附实验检测显示其VCAM1分泌量显著高于其他胎盘亚组织来源(文献未明确提供具体数值,基于图表趋势推测),该分子具有独特的免疫抑制活性,可通过抑制T细胞活化减轻肝内炎症。
核心成果提炼显示,VCAM1被确定为绒毛板来源MSCs的特异性Biomarker,不仅可用于该亚群MSCs的分离鉴定,还可作为免疫调节治疗的潜在靶点;VLA-4作为PD-MSCs高表达的黏附分子,是提升其肝损伤部位定植效率的关键调控因子。这些Biomarker的发现,为PD-MSCs的精准分离、鉴定及功能修饰提供了依据,创新性在于首次系统阐述了胎盘不同亚组织来源MSCs的Biomarker差异与功能关联,打破了以往对PD-MSCs“同质化”的认知,为其精准治疗ALF提供了新的方向。文献未明确提供样本量与统计学显著性数据。
