1. 领域背景与文献引入
文献英文标题:A novel 3-miRNA network regulates tumour progression in oral squamous cell carcinoma;发表期刊:Biomarker Research;影响因子:未公开;研究领域:口腔鳞状细胞癌分子标志物与肿瘤进展机制。
口腔鳞状细胞癌是全球范围内导致恶性肿瘤相关死亡的重要原因之一,领域共识:近四十年来其5年生存率始终维持在较低水平,核心瓶颈在于多数患者确诊时已处于晚期,错失最佳治疗时机。尽管分子诊断技术近年来取得一定进展,但目前仍缺乏可用于临床的疾病特异性早期诊断标志物,传统组织活检存在难以获取深部肿瘤样本、无法全面反映肿瘤异质性的局限性。液体活检尤其是外泌体来源的微小RNA(miRNA)作为非侵入性生物标志物的研究是当前领域热点,miRNA具有稳定性高、组织特异性强的特点,适合用于疾病的早期检测与预后监测,但现有研究多存在样本量较小、缺乏多组学整合分析及体内外功能验证的问题,尚未形成可转化至临床的miRNA标志物组合。本研究针对这一研究空白,旨在从OSCC患者的唾液外泌体中筛选可用于早期诊断及预后预测的miRNA标志物,并系统解析其调控肿瘤进展的分子机制,为OSCC的临床诊疗提供新的策略。
2. 文献综述解析
作者对领域内现有OSCC miRNA标志物研究的分类维度主要包括miRNA的来源(肿瘤组织/体液外泌体)、研究设计的系统性(单组学分析/多组学整合)、验证阶段的完整性(仅表达谱分析/细胞功能验证/临床样本验证)。
现有研究的关键结论表明,OSCC患者的组织与体液中存在多种差异表达的miRNA,部分miRNA可作为潜在的诊断或预后标志物;技术方法层面,外泌体miRNA检测具有非侵入性、样本易获取、标志物稳定性高的优势,适合大规模人群筛查;但现有研究的局限性较为明显,多数研究仅停留在miRNA表达谱的筛选阶段,缺乏大样本的临床验证数据,且未深入解析miRNA调控肿瘤进展的下游分子网络与信号通路,难以明确其在肿瘤发生发展中的功能作用。
本研究的创新价值在于首次整合匹配的OSCC患者肿瘤组织与唾液外泌体的小RNA测序、转录组测序数据及TCGA公共数据库资源,筛选得到由miR-140-5p、miR-143-5p、miR-145-5p组成的3-miRNA标志物组合,并通过细胞功能实验全面验证了该组合调控肿瘤增殖、凋亡、迁移及上皮间质转化的分子机制,弥补了现有研究缺乏多组学整合分析及功能验证的不足,为OSCC的非侵入性标志物研究提供了新的范式。
3. 研究思路总结与详细解析
本研究的整体研究目标是筛选OSCC患者唾液外泌体中可用于早期诊断及预后预测的miRNA标志物,并解析其调控肿瘤进展的分子机制;核心科学问题是3-miRNA组合如何通过调控下游分子网络影响OSCC细胞的恶性表型;技术路线遵循“样本收集与鉴定→标志物筛选与验证→分子网络构建→功能机制验证”的闭环逻辑,确保研究结果的可靠性与系统性。
3.1 唾液外泌体的分离与鉴定
实验目的为验证从OSCC患者唾液中分离的外泌体的纯度与生物学特性,为后续miRNA分析提供可靠的样本基础。方法细节上,采用超速离心结合试剂盒沉淀法分离唾液外泌体,使用纳米颗粒跟踪分析(NTA)检测外泌体的浓度与粒径分布,通过透射电子显微镜(TEM)观察外泌体的形态结构,利用流式细胞术检测外泌体表面特异性标志物CD9、CD63、CD81的表达水平。结果解读显示,NTA结果表明OSCC患者唾液外泌体的浓度为7.31×10^8 particles/mL,是健康对照人群的10倍(n=23,P<0.05);TEM观察到外泌体为直径30-50nm的球形囊泡,符合外泌体的典型形态;流式细胞术结果显示86%-88%的分离囊泡表达CD9、CD63、CD81,证实分离得到的是高纯度的外泌体样本。实验所用关键产品:Invitrogen™ Total Exosome Isolation Reagent(Thermo Fisher Scientific)、NanoSight LM10 Nanoparticle Tracking Analysis软件(Malvern Instruments Ltd.)、JEM1400 Plus透射电子显微镜(Jeol)、FACS Calibur™流式细胞仪(Becton Dickinson Biosciences)、抗人CD9-APC、CD63-Alexa 488、CD81-PE抗体(Thermo Fisher Scientific)。
3.2 差异miRNA的筛选与临床验证
实验目的是从OSCC患者的肿瘤组织与唾液外泌体中筛选具有诊断与预后价值的差异表达miRNA,并通过大样本临床队列验证其有效性。方法细节上,对23例OSCC患者的肿瘤组织、唾液外泌体及匹配的健康对照样本进行小RNA测序,结合TCGA数据库中114例OSCC患者的miRNA表达数据,筛选在两个数据集中共同差异表达的miRNA;在70例大样本临床队列中采用实时荧光定量聚合酶链反应(qRT-PCR)验证差异miRNA的表达水平;通过受试者工作特征(ROC)曲线、主成分分析(PCA)评估miRNA组合的诊断效能,采用Kaplan-Meier生存分析评估其与患者预后的相关性。结果解读显示,小RNA测序与TCGA数据整合分析筛选得到12个差异表达miRNA,实时荧光定量聚合酶链反应验证发现miR-140-5p、miR-143-5p、miR-145-5p在OSCC患者的肿瘤组织与唾液外泌体中均显著下调;该3-miRNA组合在肿瘤组织样本中的ROC曲线下面积(AUC)为0.93(P<0.0001),灵敏度为93.02%,特异性为93.33%;在唾液外泌体样本中的AUC为0.99(P<0.0001),灵敏度为98%,特异性为99%;PCA分析可有效区分OSCC患者与健康对照人群;Kaplan-Meier生存分析显示,低表达该3-miRNA组合的OSCC患者总生存期显著短于高表达患者(n=114,P<0.05),且该组合的表达水平与疾病进展、复发显著相关。
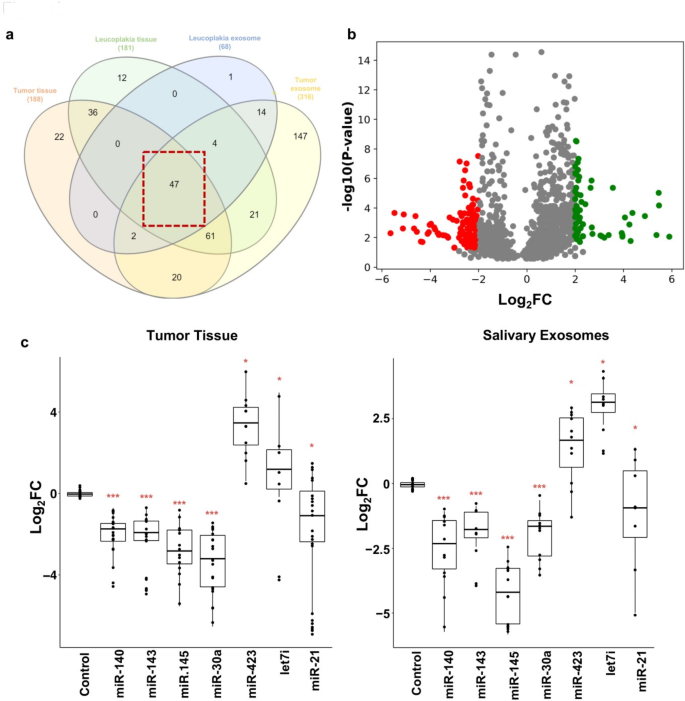
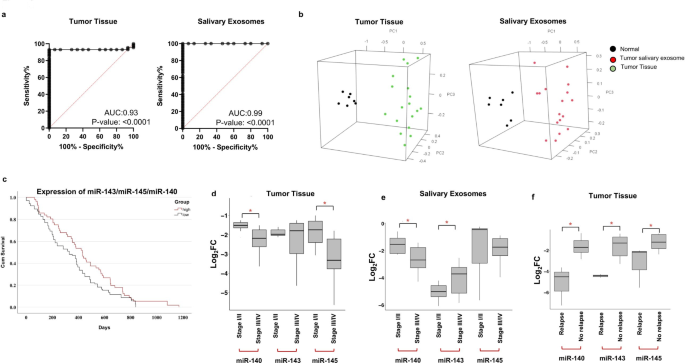
实验所用关键产品:QIAseq® miRNA文库构建试剂盒(QIAGEN)、miScript-II逆转录试剂盒(QIAGEN)、miScript SYBR® Green PCR试剂盒(QIAGEN)、QuantStudio 5实时PCR系统(Applied Biosystems)。
3.3 miRNA-mRNA调控网络的构建与通路分析
实验目的是解析3-miRNA组合调控OSCC肿瘤进展的下游分子靶点与信号通路,明确其分子调控机制。方法细节上,对OSCC患者的肿瘤组织进行转录组测序,结合TCGA数据库的mRNA表达数据,采用TargetScan、miRDB、miRWalk三种生物信息学算法预测3-miRNA组合的靶基因;通过Cytoscape软件构建miRNA-mRNA相互作用网络,利用Ingenuity Pathways Analysis(IPA)软件进行通路富集分析。结果解读显示,共预测得到315个差异表达的靶基因,构建的相互作用网络中HIF1A、CDH1、CD44、EGFR、CCND1为核心枢纽基因;通路富集分析显示上皮间质转化(EMT)是最显著的调控通路,提示3-miRNA组合通过调控这些核心枢纽基因参与EMT过程,进而影响OSCC的恶性进展。
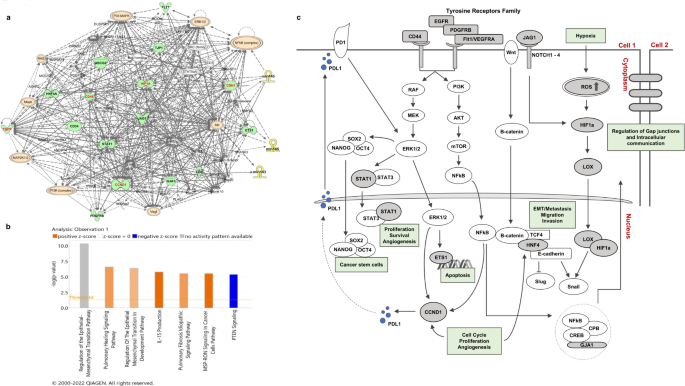
实验所用关键产品:NEBNext® Ultra™ II定向RNA文库构建试剂盒(New England Biolabs)、Cytoscape软件(v3.6.1)、Ingenuity Pathways Analysis软件(QIAGEN)。
3.4 3-miRNA组合的细胞功能验证
实验目的是在细胞水平验证3-miRNA组合对OSCC细胞恶性表型的调控作用,明确其生物学功能。方法细节上,将miR-140-5p、miR-143-5p、miR-145-5p的模拟物及阴性对照转染至人OSCC细胞系OECM-1,采用实时荧光定量聚合酶链反应验证转染效率;通过MTT法检测细胞增殖能力,流式细胞术检测细胞周期分布与凋亡率,划痕实验检测细胞迁移能力,Transwell实验检测细胞侵袭能力,实时荧光定量聚合酶链反应检测EMT标志物的表达水平,JC-1染色检测线粒体膜电位变化。结果解读显示,转染后3-miRNA的表达水平显著上调(miR-143上调5.13±0.9倍,miR-145上调18.04±2.55倍,miR-140上调23±2.46倍,n=3,P<0.01);细胞增殖率较阴性对照降低20%(n=3,P<0.01),G2/M期细胞比例显著增加(41.73±5% vs 阴性对照20.93±2.1%,n=3,P<0.01);早期凋亡率从4.33±2.48%升至17.33±3.36%(n=3,P<0.01),线粒体膜电位显著降低,提示通过线粒体途径诱导细胞凋亡;细胞迁移距离从420.44±35.01μm降至230.85±30.56μm(n=3,P<0.01),细胞侵袭率从81.46±6%降至42.34±18%(n=3,P<0.05);EMT标志物E-钙粘蛋白表达上调,N-钙粘蛋白表达下调,提示逆转了EMT过程。
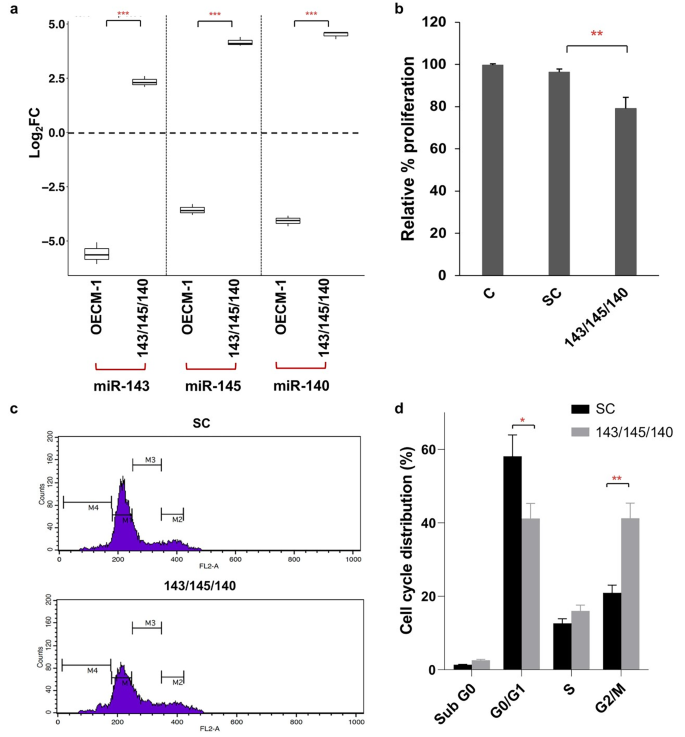
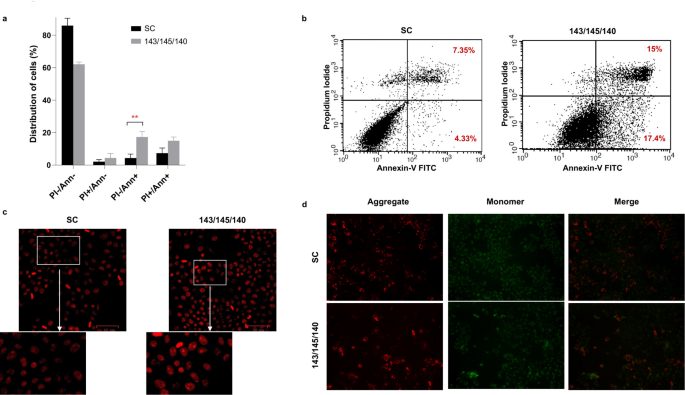
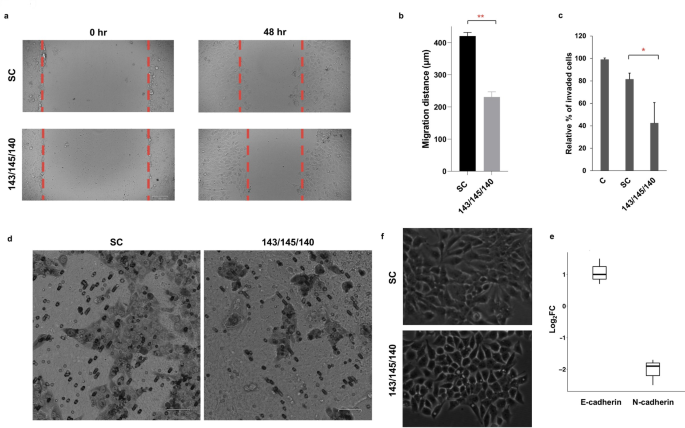
实验所用关键产品:OECM-1细胞系(Sigma Aldrich)、miRNA模拟物与阴性对照(Thermo Fisher Scientific)、Lipofectamine 2000转染试剂(Invitrogen)、MTT试剂(Sigma-Aldrich)、Annexin V-FITC/PI凋亡检测试剂盒(Biolegend)、JC-1染色试剂、QCM Collagen细胞侵袭检测试剂盒(Millipore Sigma)。
4. Biomarker研究及发现成果解析
本研究发现的核心Biomarker为唾液外泌体来源的miR-140-5p、miR-143-5p、miR-145-5p组成的3-miRNA组合,其筛选与验证过程遵循“多组学筛选→大样本临床验证→功能机制解析”的完整逻辑链条,为OSCC的非侵入性诊断与预后预测提供了新的候选标志物。
该Biomarker来源于OSCC患者的唾液外泌体与肿瘤组织,验证方法包括实时荧光定量聚合酶链反应定量检测miRNA表达水平、ROC曲线分析诊断效能、Kaplan-Meier生存分析评估预后相关性;特异性与敏感性数据显示,该3-miRNA组合在肿瘤组织样本中的AUC为0.93(P<0.0001),灵敏度93.02%,特异性93.33%,在唾液外泌体样本中的AUC为0.99(P<0.0001),灵敏度98%,特异性99%,具有优异的诊断效能。
核心成果提炼显示,该3-miRNA组合可作为OSCC的预后标志物,低表达该组合的患者总生存期显著缩短(n=114,P<0.05);其创新性在于首次从匹配的唾液外泌体与肿瘤组织样本中筛选得到该组合,并通过多组学整合分析与细胞功能实验明确其通过调控HIF1A、CDH1、CD44等核心枢纽基因逆转EMT过程,从而抑制肿瘤细胞增殖、迁移与侵袭,诱导细胞凋亡的分子机制;该Biomarker为OSCC的非侵入性早期诊断与预后监测提供了新的工具,同时为OSCC的分子靶向治疗提供了潜在的靶点方向。
