1. 领域背景与文献引入
文献英文标题:Nuclear protein IK undergoes dynamic subcellular translocation and forms unique nuclear bodies during the cell cycle;发表期刊:Biomarker Research;影响因子:未公开;研究领域:细胞周期调控与核结构生物学。
细胞周期调控是维持细胞稳态的核心分子机制,纺锤体组装检查点(SAC)作为保障染色体正确分离的关键关卡,其功能异常会直接导致染色体不稳定性,与肿瘤发生、发展及耐药性产生密切相关。领域共识:目前已发现MAD1、BubR1等多个纺锤体组装检查点调控蛋白,但其具体调控网络仍存在大量未知环节。核体作为核内高度组织化的功能区室,参与基因转录、RNA加工等多种核内生物学过程,但其参与细胞周期调控的具体机制及相关特异性标志物研究仍处于空白阶段。针对核蛋白IK的功能及亚细胞定位机制的未知,本研究通过细胞功能验证、活细胞成像、蛋白互作分析等多维度实验,系统揭示了IK在细胞周期中的动态定位模式及调控作用,为核结构与细胞周期调控的关联研究提供了新的研究靶点与视角。
2. 文献综述解析
作者从IK的发现历程、已知功能维度、现有研究局限三个核心维度对领域内研究进行了系统梳理与评述。现有研究显示,IK最初被鉴定为免疫应答调控因子,可抑制IFN-γ诱导的HLA II类抗原表达;后续蛋白组学研究将其归类为剪接体组分,提示其参与RNA加工过程;全基因组siRNA文库筛选发现IK缺失会导致有丝分裂阻滞,近期研究进一步证实IK是纺锤体组装检查点蛋白MAD1定位到动粒的必需因子,初步揭示了其在细胞周期调控中的作用。但现有研究仍存在明显局限:对IK在细胞周期中的亚细胞定位动态变化规律、核体形成的结构基础及具体调控机制尚不明确,且缺乏IK与剪接体组分直接互作的实验证据,无法明确其参与剪接体功能的具体方式。
本研究通过构建IK缺失突变体、活细胞实时成像、两步亲和下拉结合质谱分析等创新实验设计,首次明确了IK在细胞周期不同阶段的动态亚细胞定位模式,揭示了其C端区域对核定位及核体形成的必要性,并直接证实了IK与剪接体RNA解旋酶DHX15的互作关系,填补了IK功能及核结构调控机制的研究空白,为核体参与细胞周期调控的机制研究提供了新的实验依据。
3. 研究思路总结与详细解析
本研究的核心目标是明确IK在细胞周期中的功能及亚细胞定位调控机制,核心科学问题为IK的动态亚细胞定位如何参与细胞周期调控,技术路线遵循“功能验证→定位分析→结构域功能鉴定→蛋白互作机制解析”的逻辑闭环,通过多维度实验系统阐明了IK的生物学功能及调控机制。
3.1 IK缺失诱导有丝分裂阻滞的功能验证
实验目的:验证IK缺失对细胞周期进程的影响,明确其在细胞周期调控中的核心作用。
方法细节:采用HeLa细胞系,分别转染IK siRNA和荧光素酶siRNA作为阴性对照,转染48小时后通过相差显微镜观察细胞形态变化,采用免疫印迹(Western blot)技术验证IK蛋白的敲低效率,通过流式细胞术分析细胞周期分布;同时通过环己酰亚胺(CHX)处理阻断新蛋白合成,结合免疫印迹检测IK蛋白的半衰期。
结果解读:转染IK siRNA 48小时后,HeLa细胞出现明显的圆形化表型,提示细胞发生有丝分裂阻滞;免疫印迹结果显示IK蛋白表达水平显著降低,证实敲低效率可靠;流式细胞术分析显示G2/M期细胞比例显著增加(文献未明确具体数值,基于图表趋势推测);CHX处理24小时后IK蛋白水平显著下降,表明IK蛋白半衰期约为24小时(n=3,P<0.05)。
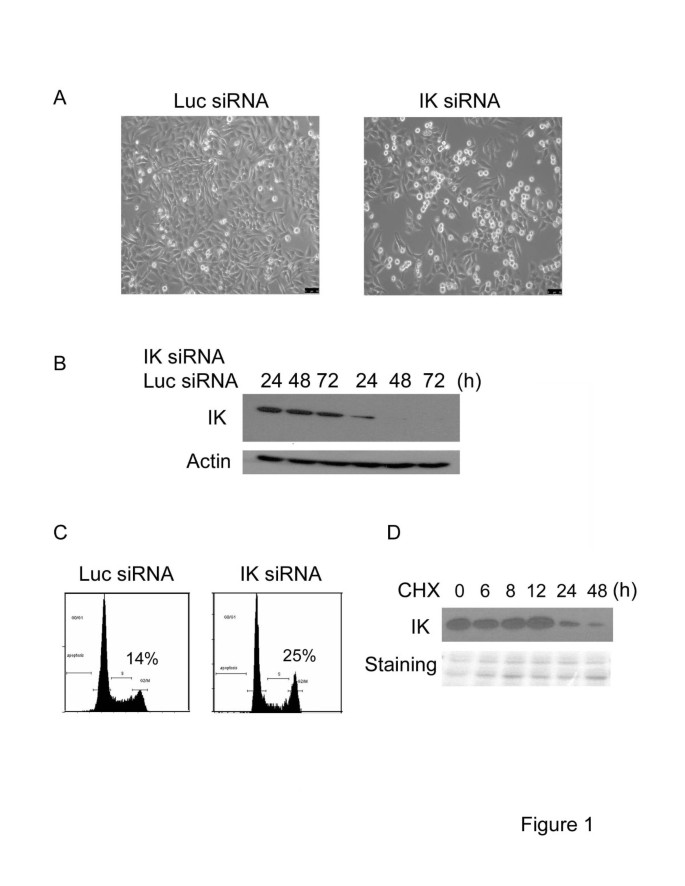
实验所用关键产品:Bethyl Laboratory Inc的IK抗体、Dharmacon的IK siRNA、Bio-Rad的SDS-PAGE迷你凝胶系统、Beckman Coulter的Epics XL-MCLTM流式细胞仪。
3.2 IK在细胞周期中的动态亚细胞定位分析
实验目的:系统解析IK在细胞周期不同阶段的亚细胞定位模式,明确其动态变化规律。
方法细节:构建GFP标记的野生型IK表达质粒,转染HeLa细胞48小时后,通过荧光显微镜观察间期细胞的IK定位模式;采用活细胞共聚焦显微镜进行时间 lapse 成像,实时追踪IK核体的形成与消失过程;通过免疫荧光染色结合荧光显微镜,观察有丝分裂不同阶段(前中期、中期、后期、末期、G1期)的IK定位变化。
结果解读:间期细胞中,GFP-IK主要呈现两种定位模式:约92%的阳性细胞中IK均匀分布于细胞核,约8%的细胞中IK形成大小不一的核体;活细胞成像显示IK核体随细胞周期进程逐渐形成并浓缩,随后消失并恢复均匀分布;有丝分裂阶段,前中期、中期、后期IK主要分布于核质,染色体区域无明显信号;末期IK开始逐渐积累于染色体;G1期IK完全定位于染色体,与DAPI染色信号高度重叠。
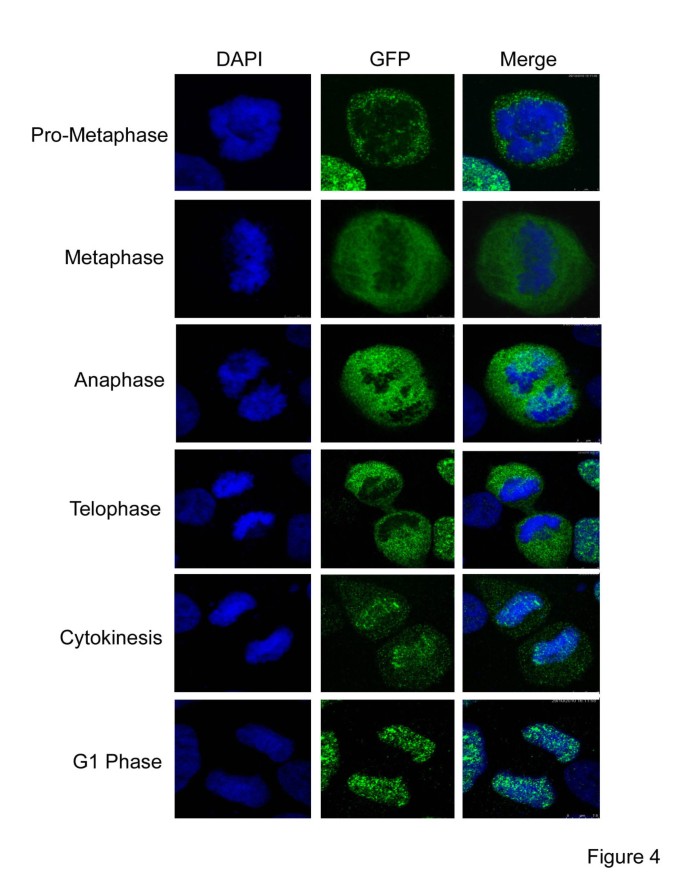
实验所用关键产品:Leica的TCS SP5共聚焦显微镜、Leica的AF6000荧光显微镜、Molecular Probe的DAPI染色剂。
3.3 IK结构域对亚细胞定位的调控作用研究
实验目的:鉴定参与IK核定位及核体形成的关键结构域,明确其结构与功能的关联。
方法细节:构建GFP标记的IK缺失突变体,其中IK280包含N端区域但缺失RED结构域及C端区域,IK380保留RED结构域但缺失C端区域;将野生型IK及突变体分别转染HeLa细胞,通过荧光显微镜观察突变体的亚细胞定位模式。
结果解读:野生型IK仅特异性定位于细胞核,而IK280和IK380同时存在于细胞核和细胞质,且均无法形成核体,表明IK的C端区域(380-557位氨基酸)是其核定位及核体形成的必需结构域,RED结构域对该过程的调控作用尚不明确。
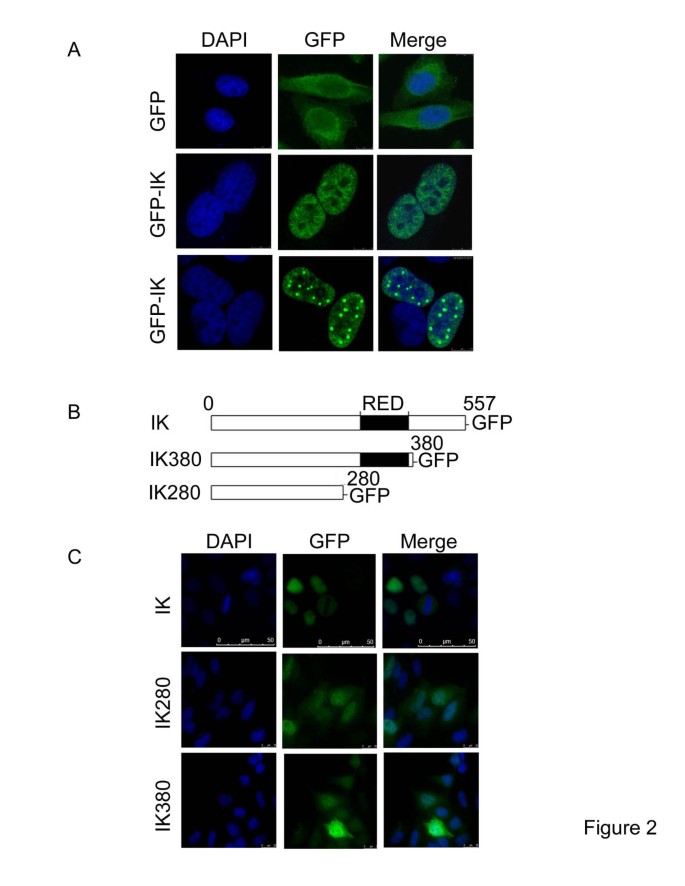
文献未提及具体突变体构建相关产品,领域常规使用PCR克隆试剂盒、质粒载体等试剂。
3.4 IK互作蛋白的鉴定与功能关联分析
实验目的:筛选与IK互作的蛋白分子,明确其参与细胞周期调控及核体功能的分子机制。
方法细节:构建His6标记的IK表达质粒,转染HEK293K细胞后,通过Ni²⁺-IDA琼脂糖树脂进行亲和下拉,结合免疫沉淀(IP)富集IK互作蛋白;经SDS-PAGE分离后,通过质谱分析鉴定互作蛋白;同时通过免疫荧光染色验证IK与Cajal体组分coilin的共定位情况。
结果解读:质谱分析鉴定到DHX15(ATP依赖的RNA解旋酶,参与pre-mRNA剪接)为IK的核心互作蛋白;免疫荧光结果显示IK与coilin无明显共定位,结合前期研究中IK核体与核仁、PML体无共定位的结果,表明IK形成的核体为一种新型未知核结构。
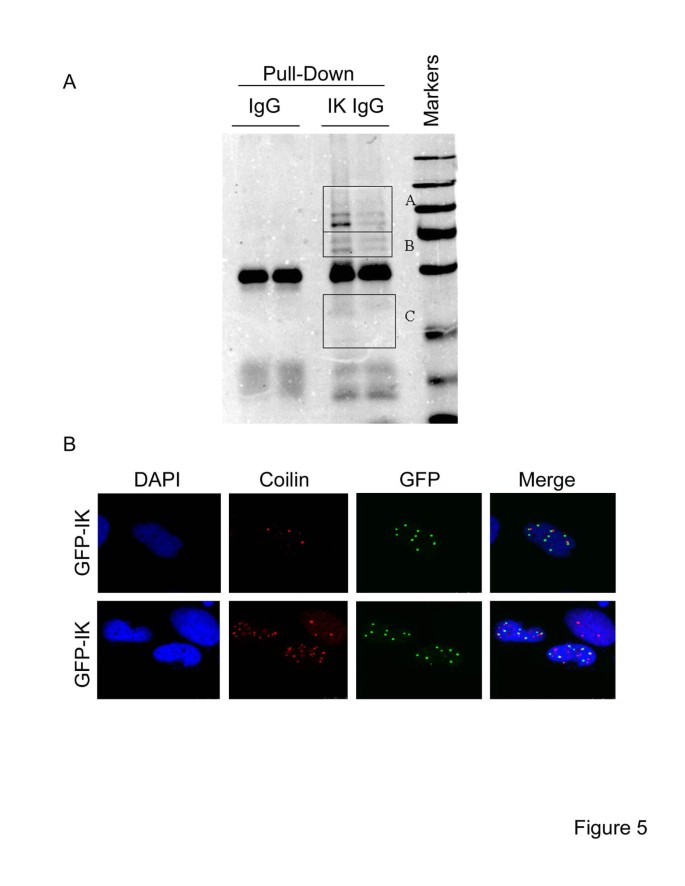
实验所用关键产品:Clonetech的Ni²⁺-IDA-琼脂糖树脂、Millipore的蛋白G-琼脂糖树脂。
4. Biomarker研究及发现成果解析
Biomarker定位
本研究中IK被定位为一种新型核体特异性标志物,其筛选与验证遵循“细胞功能验证→亚细胞定位分析→结构域功能鉴定→蛋白互作验证”的完整逻辑链条:首先通过siRNA敲低实验验证IK在细胞周期调控中的核心功能,随后通过活细胞成像明确其核体形成的动态特征,通过缺失突变体实验鉴定核定位及核体形成的关键结构域,最后通过蛋白互作分析明确其核体功能的分子基础。
研究过程详述
IK来源于HeLa细胞及HEK293K细胞的核蛋白组分,通过免疫荧光染色、活细胞共聚焦成像等方法验证了其在细胞周期中的动态定位模式,通过缺失突变体实验证实其C端区域对核定位及核体形成的必要性,通过两步亲和下拉结合质谱分析证实其与剪接体RNA解旋酶DHX15的直接互作;免疫荧光结果显示IK核体与已知核结构(核仁、PML体、Cajal体)无共定位,表明其为新型核结构标志物。文献未提供IK作为Biomarker的特异性、敏感性定量数据。
核心成果提炼
IK作为新型核体标志物,其形成的核体为一种未知核结构,可能通过与剪接体组分DHX15互作参与pre-mRNA剪接过程,进而调控细胞周期进程;首次证实IK缺失会导致有丝分裂阻滞,提示其可作为细胞周期调控异常的潜在标志物;本研究为核结构参与细胞周期调控的机制研究提供了新的靶点,为染色体不稳定性相关疾病的诊断与治疗提供了新的理论依据,文献未提供相关统计学结果(如HR值、AUC值等)。
