1. 领域背景与文献引入
文献英文标题:Outgrowth of a CSF3R-mutant clone drives a second myeloproliferative neoplasm in a chronic myeloid leukemia patient: a case report;发表期刊:Biomarker Research;影响因子:未公开;研究领域:骨髓增殖性肿瘤(MPN)的克隆演化与靶向治疗耐药
骨髓增殖性肿瘤(MPN)是一类由造血干细胞缺陷驱动成熟髓系细胞过度增殖的克隆性血液恶性肿瘤,慢性髓系白血病(CML)和慢性中性粒细胞白血病(CNL)是两类诊断标准互斥的MPN亚型。CML的核心分子标志是费城(Ph)染色体[t(9;22)]形成的BCR-ABL1融合基因,该基因通过组成性激活酪氨酸激酶驱动疾病进展,酪氨酸激酶抑制剂(TKI)是其一线标准治疗方案,但治疗过程中常出现ABL1激酶域突变导致的耐药克隆。CNL则属于Ph阴性MPN,其发病依赖CSF3R突变激活JAK/STAT信号通路,此前两类疾病被认为不会在同一患者中先后发生。当前领域的研究热点聚焦于TKI选择压力下CML患者的克隆演化规律,但此前尚无CML治疗后发生CNL的病例报道,针对复杂克隆结构患者在靶向治疗下出现跨亚型MPN克隆演化的机制与临床特征研究存在空白,本文通过首例相关病例的系统分析填补了这一空白。
2. 文献综述解析
本文的背景综述围绕MPN的分类体系、CML与CNL的互斥诊断标准及TKI治疗下的克隆演化展开,作者按疾病亚型分类梳理了现有研究进展。现有研究已明确CML的BCR-ABL1驱动机制及TKI耐药的主要类型为ABL1激酶域点突变,同时也证实CSF3R突变是CNL的高度特异性诊断标志物,但现有研究多关注单一MPN亚型内的克隆演化,未涉及TKI选择压力下CML患者出现第二种MPN亚型的情况。现有研究的局限性在于缺乏对复杂克隆结构MPN患者靶向治疗后克隆演化的全面认知,尤其是不同MPN亚型克隆在同一患者中的先后发生机制尚未被揭示。本文的创新价值在于首次报道了CML患者在TKI治疗后出现CNL的病例,填补了该领域的研究空白,为复杂克隆结构MPN患者的治疗策略优化提供了新的临床依据。
3. 研究思路总结与详细解析
本文为临床病例报告,整体研究思路为追踪一名69岁男性CML患者的全程诊疗过程,通过系列分子生物学检测(荧光原位杂交、下一代测序、BCR-ABL1转录本定量)分析患者在TKI治疗下的克隆演化轨迹,明确CSF3R突变克隆的出现与CNL诊断的关联,最终提出复杂克隆结构MPN患者的潜在治疗方向。
3.1 初始CML诊断与基线分子检测
实验目的:明确患者的初始血液系统疾病诊断及核心分子特征。方法细节:对患者进行骨髓活检,采用荧光原位杂交(FISH)检测BCR-ABL1染色体易位,通过定量PCR检测BCR-ABL1转录本水平(国际标准化IS)。结果解读:骨髓活检显示骨髓增生极度活跃(100%),原始细胞占比约4%,符合慢性期CML诊断;FISH检测200个细胞证实存在BCR-ABL1易位,Ph染色体阳性;BCR-ABL1(p210)转录本水平为66.45%(IS,n=1,文献未提供P值)。产品关联:文献未提及具体实验产品,领域常规使用荧光原位杂交检测试剂盒、qRT-PCR检测BCR-ABL1转录本。
3.2 TKI治疗下的耐药克隆监测与治疗调整
实验目的:监测患者TKI治疗后的疗效及克隆演化情况,及时调整治疗方案以应对耐药。方法细节:患者先后接受尼洛替尼、伊马替尼、达沙替尼、普纳替尼治疗,定期检测血常规、BCR-ABL1转录本水平,通过Sanger测序或下一代测序检测ABL1激酶域突变。结果解读:尼洛替尼治疗18周后BCR-ABL1降至0.403%(IS,n=1,文献未提供P值),但患者出现严重血小板减少(11000/mm³,n=1,文献未提供P值)及ABL1 E255V突变(对伊马替尼、尼洛替尼耐药);更换达沙替尼后BCR-ABL1降至0.1%(IS)以上,随后出现ABL1 T315I突变(对多类TKI耐药);更换普纳替尼3个月后BCR-ABL1降至0.1%(IS)以下,2年后荧光原位杂交检测200个细胞未发现Ph染色体,BCR-ABL1转录本为0.000%(IS,n=1,文献未提供P值)。产品关联:文献未提及具体实验产品,领域常规使用Sanger测序或NGS panel检测ABL1突变,全自动血细胞分析仪检测血常规指标。
3.3 CSF3R突变克隆的鉴定与CNL诊断
实验目的:明确患者在Ph染色体阴性后出现持续性中性粒细胞升高的病因。方法细节:采用220基因下一代测序(NGS) panel检测患者骨髓样本的体细胞基因突变,回顾性分析存档骨髓样本的突变情况。结果解读:NGS检测到CSF3R T618I(变异等位基因频率VAF=41.1%)和W818*(VAF=40.3%)突变,回顾性分析显示该克隆至少已存在3年;此时患者白细胞计数为22800/mm³,中性粒细胞占比83%,符合世界卫生组织(WHO)定义的CNL诊断标准,确诊为第二种骨髓增殖性肿瘤。
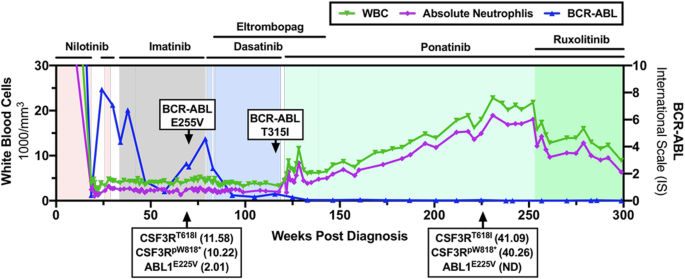
该图直观展示了患者在靶向治疗过程中,BCR-ABL1克隆被逐渐抑制后,CSF3R突变的中性粒细胞克隆逐渐增殖的克隆演化轨迹。产品关联:文献未提及具体实验产品,领域常规使用大panel NGS检测血液系统肿瘤基因突变。
3.4 后续靶向治疗与疗效评估
实验目的:评估针对CSF3R突变的靶向药物对CNL的治疗疗效。方法细节:患者开始接受鲁索替尼(5mg每日两次)治疗,7个月后剂量调整为7.5mg每日两次,定期检测血常规监测疗效。结果解读:鲁索替尼治疗后患者白细胞计数稳定在12800-17400/mm³,中性粒细胞计数稳定在9700-14300/mm³;剂量调整后白细胞计数进一步降至8900-13000/mm³,中性粒细胞计数降至6300-10000/mm³,血小板、血红蛋白水平保持稳定,提示鲁索替尼对CSF3R突变克隆具有明确疗效。产品关联:文献未提及具体实验产品,领域常规使用全自动血细胞分析仪监测血常规指标。
4. Biomarker研究及发现成果
Biomarker定位与筛选验证逻辑
本文涉及的Biomarker为CSF3R基因的T618I和W818*体细胞突变,属于驱动性突变类Biomarker。其筛选逻辑为:患者在TKI治疗后Ph染色体转阴但出现持续性中性粒细胞升高,通过临床表型驱动的分子检测筛选潜在致病突变;验证逻辑为下一代测序检测结合WHO的CNL诊断标准,确认突变克隆与临床表型的关联。
研究过程详述
该Biomarker来源于患者的骨髓样本,验证方法为下一代测序。特异性方面,CSF3R突变是CNL的高度特异性诊断标志物(领域共识),本文中患者的CSF3R突变VAF分别为41.1%和40.3%,对应的临床表型完全符合CNL的诊断标准,但文献未提供该Biomarker的敏感性、ROC曲线等定量评估数据。
核心成果提炼
该Biomarker的功能关联为通过激活JAK/STAT信号通路驱动CNL的发生,促进中性粒细胞的异常增殖;创新性在于首次发现该Biomarker克隆在CML患者TKI治疗的选择压力下获得增殖优势,导致第二种MPN亚型的发生;文献未提供该Biomarker与患者预后相关的统计学数据(如风险比HR、生存曲线等)。
