1. 领域背景与文献引入
文献英文标题:Prognostic value of secretory autophagosomes in patients with acute respiratory distress syndrome;发表期刊:Biomarker Research;影响因子:未公开;研究领域:急性呼吸窘迫综合征(ARDS)生物标志物研究
急性呼吸窘迫综合征是一种致死性肺部疾病,以急性发作的严重低氧性呼吸衰竭为核心特征,领域共识:其临床死亡率达30%-40%,通过精准的患者分层优化治疗方案可有效降低死亡率。当前临床广泛使用的SOFA(序贯器官衰竭评估)等评分系统虽能提供患者预后的整体信息,但存在缺乏病理生理依据、对死亡风险的预测准确性不足的局限,无法满足个性化治疗的需求。细胞外囊泡作为细胞间通讯的重要载体,在免疫炎症反应中发挥关键调控作用,此前基础研究发现巨噬细胞来源的分泌型自噬体(SAPs)可通过传递促炎细胞因子IL-1β在小鼠模型中加重肺损伤,但SAPs在ARDS患者中的临床价值尚未明确,这一研究空白促使本团队开展临床队列研究,探索其作为预后生物标志物的潜在价值,为ARDS患者的风险分层提供新的病理生理相关指标。
2. 文献综述解析
本文献综述部分围绕ARDS的临床困境、现有预后评估工具的局限及细胞外囊泡在炎症性疾病中的作用展开,以“临床需求-基础研究铺垫-研究空白”的逻辑串联核心内容。首先,作者梳理了ARDS的疾病现状,明确现有评分系统如SOFA虽能评估患者整体器官功能状态,但无法精准预测个体死亡风险,且未整合疾病的核心病理生理特征——失控的肺泡炎症,难以指导针对性的抗炎治疗;接着,作者总结了细胞外囊泡在免疫炎症反应中的调控作用,提及免疫细胞分泌的囊泡可通过传递生物活性分子参与炎症进程,此前团队的基础研究已证实巨噬细胞来源的SAPs可直接加重小鼠肺损伤,为临床研究提供了理论依据;最后,作者明确当前研究空白:针对SAPs在ARDS患者中临床价值的探索完全缺失,现有生物标志物研究多聚焦于常规炎症因子,缺乏针对细胞外囊泡亚群的特异性研究。通过对比现有研究的不足,本研究的创新价值凸显为首次在临床队列中验证SAPs比例与ARDS患者28天死亡率的关联,并提出联合SOFA评分的优化预测方案,弥补了现有预后评估工具的病理生理缺失,为ARDS的精准预后评估提供了新方向。
3. 研究思路总结与详细解析
本研究的核心目标是明确支气管肺泡灌洗液(BALF)中SAPs比例对ARDS患者的预后预测价值,核心科学问题为SAPs比例是否与ARDS患者28天死亡率独立相关,技术路线遵循“队列建立-样本处理-标志物鉴定-关联分析-优化验证”的闭环逻辑,从临床样本入手,结合多种分子生物学技术完成SAPs的鉴定与预后价值评估。
3.1 研究对象入组与样本收集
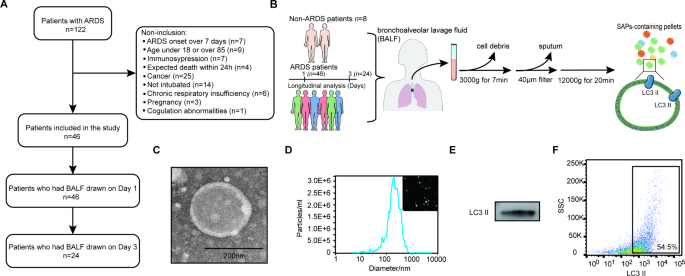
本环节的实验目的是建立具有临床代表性的ARDS患者队列与对照队列,为后续标志物分析提供可靠样本基础。方法细节为开展前瞻性单中心研究,于2020年11月至2022年1月筛选122例疑似ARDS患者,最终纳入46例符合柏林定义的ARDS患者与8例非ARDS对照,收集ARDS患者入组第1天或第3天的BALF样本,对照组仅收集第1天的BALF样本。结果解读为入组流程显示37.7%的筛选患者符合纳入标准,基线特征分析显示ARDS患者的器官功能损伤程度显著高于对照组,为后续组间比较提供了临床背景匹配性依据。文献未提及具体实验产品,领域常规使用支气管肺泡灌洗液收集套件、样本低温保存管等试剂/仪器。
3.2 分泌型自噬体的分离与鉴定
本环节的实验目的是从BALF中分离并鉴定SAPs,明确其形态、大小及分子特征,确保后续比例检测的特异性。方法细节为采用梯度离心法分离细胞外囊泡(EVs),通过纳米颗粒追踪分析(NTA)检测EVs的粒径分布与浓度,结合流式细胞术、透射电子显微镜及免疫印迹(Western blot)技术鉴定SAPs,通过流式细胞术检测EVs中SAPs的比例(PSV)。结果解读为透射电子显微镜显示分离的EVs具有典型的囊泡形态,NTA分析显示其直径峰值为214.2nm,符合分泌型自噬体的粒径特征;免疫印迹与流式细胞术均检测到SAPs特异性标志物LC3II的表达,证实成功分离出高纯度的含SAPs的EVs组分。文献未提及具体实验产品,领域常规使用梯度离心设备、纳米颗粒追踪分析仪、透射电子显微镜及免疫印迹相关试剂等。
3.3 SAPs比例的组间比较与来源分析
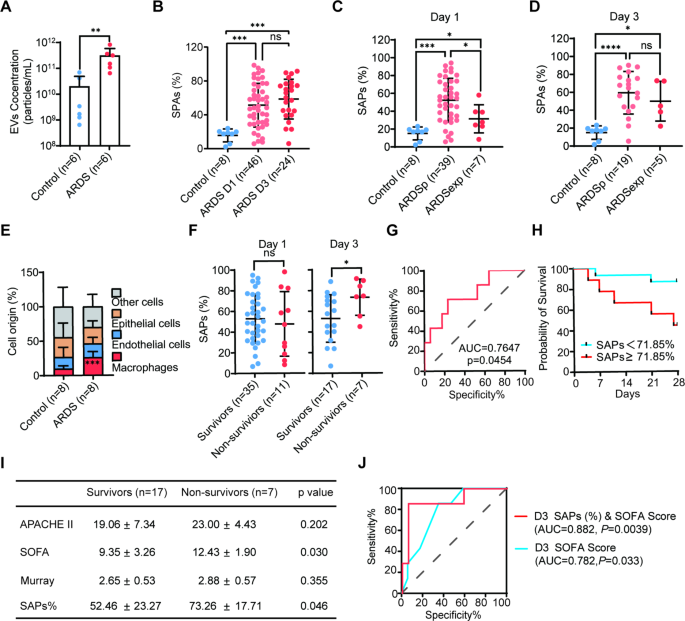
本环节的实验目的是比较ARDS患者与对照组的SAPs比例差异,并分析SAPs的细胞来源,明确其病理生理关联。方法细节为分别比较第1天、第3天ARDS患者与对照组的SAPs%,按感染部位将ARDS患者分为肺内感染组(ARDSp)与肺外感染组(ARDSexp)进行亚组分析,通过检测CD68(巨噬细胞)、CD31(内皮细胞)、CD326(上皮细胞)等细胞特异性标志物分析SAPs的细胞来源。结果解读为第1天和第3天ARDS患者的SAPs%均显著高于对照组(P<0.001),第1天ARDSp患者的SAPs%高于ARDSexp患者(P<0.05),第3天两组无显著差异;细胞来源分析显示ARDS患者中巨噬细胞来源的SAPs比例显著升高,支持此前基础研究中巨噬细胞在SAPs介导肺损伤中的核心作用。文献未提及具体实验产品,领域常规使用细胞特异性单克隆抗体、流式细胞术荧光标记试剂等。
3.4 SAPs比例与预后的关联分析
本环节的实验目的是评估SAPs比例与ARDS患者28天死亡率的关联,明确其预后预测价值。方法细节为比较存活者与非存活者的SAPs%,通过ROC曲线分析SAPs%的预测效能,采用Kaplan-Meier曲线分析不同SAPs%水平患者的生存率差异。结果解读为第1天存活者与非存活者的SAPs%无显著差异,第3天非存活者的SAPs%显著高于存活者(n=17 vs n=7,P<0.05);ROC曲线显示第3天SAPs%的AUC为0.765(95% CI 0.552-0.977,P=0.045),最佳截断值为71.85%,高SAPs%组患者的28天生存率显著低于低SAPs%组(P=0.028),提示第3天SAPs%可有效区分高死亡风险患者。文献未提及具体实验产品,领域常规使用生存分析软件、ROC曲线分析工具等。
3.5 联合SOFA评分的预测价值评估
本环节的实验目的是探索SAPs%联合SOFA评分对ARDS患者预后的预测价值,优化现有评估体系。方法细节为比较存活者与非存活者的SOFA评分,将第3天SAPs%与SOFA评分联合进行ROC曲线分析,对比联合指标与单一指标的预测效能。结果解读为第3天非存活者的SOFA评分显著高于存活者(P<0.05),联合指标的AUC为0.882(95% CI 0.715-1.000,P=0.004),显著高于单独使用SOFA评分的AUC(0.782,95% CI 0.595-0.968,P=0.033),提示联合指标可显著提升预后预测的准确性,为临床提供更精准的风险分层工具。文献未提及具体实验产品,领域常规使用临床评分系统、统计分析软件等。
4. Biomarker研究及发现成果
核心信息段
本研究鉴定的核心生物标志物为支气管肺泡灌洗液(BALF)中分泌型自噬体占细胞外囊泡的比例(SAPs%),其筛选与验证逻辑为:基于前期基础研究中SAPs在小鼠肺损伤中的致病作用,在临床队列中分离鉴定SAPs亚群,通过组间比较明确其与ARDS疾病状态的关联,进一步分析与患者28天死亡率的相关性,并联合现有临床评分系统优化预测效能,形成“基础-临床-转化”的完整验证链条。
研究过程详述
该生物标志物的样本来源为ARDS患者入组第3天的BALF,样本处理流程为梯度离心分离EVs后,采用流式细胞术结合SAPs特异性标志物LC3II检测其占EVs的比例;验证结果显示,第3天非存活者的SAPs%显著高于存活者,ROC曲线分析显示其AUC为0.765(95% CI 0.552-0.977,P=0.045),以71.85%为截断值时,可有效区分高死亡风险患者;细胞来源分析证实ARDS患者中巨噬细胞来源的SAPs比例显著升高,为其病理生理机制提供了直接依据,与前期基础研究结果一致。
核心成果提炼
本研究首次在临床中证实BALF中第3天SAPs%是ARDS患者的新型预后生物标志物,其水平与患者28天死亡率显著相关,高SAPs%患者的死亡风险显著升高;联合SOFA评分可显著提升预测价值,AUC达0.882,为ARDS患者的精准风险分层提供了更可靠的工具;同时,研究明确了巨噬细胞是ARDS患者中SAPs的主要细胞来源,为后续探索SAPs的干预靶点提供了方向。研究的局限性包括样本量较小、缺乏多中心验证队列、未实现所有患者的双时间点采样,推测:扩大样本量并开展多中心验证研究可进一步提升该生物标志物的临床应用价值,深入探索SAPs的分泌调控机制可开发新的ARDS抗炎治疗靶点。
