1. 领域背景与文献引入
文献英文标题:Advances in technology and applications of nanoimmunotherapy for cancer;发表期刊:Biomark Res;影响因子:未公开;研究领域:肿瘤免疫治疗与纳米医学交叉领域。
肿瘤免疫治疗领域发展历经百年关键节点:19世纪末Coley通过注射细菌产物观察到肿瘤抑制效应,开启免疫治疗先河;现代依托多学科进展,发展出嵌合抗原受体T细胞免疫治疗(CAR-T)、免疫检查点抑制剂、树突状细胞(DC)疫苗等策略,但均存在核心局限性:CAR-T在实体瘤中响应率低且易引发细胞因子风暴,免疫检查点抑制剂存在免疫相关不良反应且对“冷肿瘤”疗效有限,DC疫苗难以诱导显著临床应答。当前领域未解决的核心问题包括:肿瘤抗原有效靶向递送不足、免疫原性细胞死亡(ICD)诱导效率低且副作用大、冷肿瘤免疫微环境难以有效重塑。纳米技术为同时攻克这些难题提供独特范式,可实现抗原靶向递送、ICD高效介导及冷肿瘤微环境重塑,本文综述聚焦宿主-肿瘤免疫相互作用的关键环节,系统总结纳米技术在肿瘤免疫治疗中的应用进展,为领域提供全面技术框架与方向指引。
2. 文献综述解析
本文综述以宿主-肿瘤免疫相互作用的三个核心维度为分类框架,分别围绕新抗原与纳米疫苗递送、免疫原性细胞死亡与纳米介导ICD、肿瘤免疫微环境的纳米重塑展开系统评述,清晰梳理了各方向的研究进展、优势与局限性。
现有研究中,传统肿瘤疫苗存在抗原体内清除快、抗原提呈细胞(APC)摄取效率低的问题,难以诱导强效抗肿瘤免疫应答;新抗原筛选依赖高通量测序与质谱技术,但精准性与临床转化效率仍有待提升。传统ICD诱导剂如化疗、放疗存在全身毒性高、肿瘤靶向性差的局限,难以在有效诱导ICD的同时避免正常组织损伤。传统免疫检查点抑制剂、细胞因子治疗等策略存在靶向性不足、全身副作用大的问题,难以有效将冷肿瘤转化为热肿瘤。
本文通过系统整合纳米技术在上述三个关键环节的应用进展,弥补了现有研究缺乏全面技术框架梳理的不足,首次从宿主-肿瘤免疫相互作用的整体视角,总结了纳米免疫治疗的技术范式与临床转化潜力,为领域内的研究提供了清晰的方向指引,凸显了纳米技术在突破传统免疫治疗局限性中的核心价值。
3. 研究思路总结与详细解析
本文为综述类研究,整体研究思路为:围绕宿主-肿瘤免疫相互作用的核心科学问题,系统梳理纳米技术在肿瘤抗原递送、ICD诱导、肿瘤免疫微环境重塑三个关键方向的研究进展,总结各类纳米平台的技术优势、应用场景及临床转化潜力,为肿瘤纳米免疫治疗的进一步发展提供参考。
3.1 新抗原与纳米疫苗递送系统
实验目的为解决传统肿瘤疫苗抗原递送效率低、APC摄取不足的问题,增强新抗原的交叉提呈与抗肿瘤免疫应答。方法上综述了多种纳米平台的应用,包括聚合物纳米粒、脂质体、无机纳米粒等,如负载自组装肽新抗原的pH响应性纳米疫苗,可响应内体酸性pH将抗原递送至细胞质;脂质体递送体外转录mRNA新抗原疫苗,可靶向全身DC细胞。结果显示纳米疫苗可有效保护新抗原免受降解,增强淋巴结靶向性与APC摄取,显著提升抗原特异性细胞毒性T淋巴细胞(CTL)应答,与免疫检查点抑制剂联合使用可进一步缩小已建立的肿瘤。
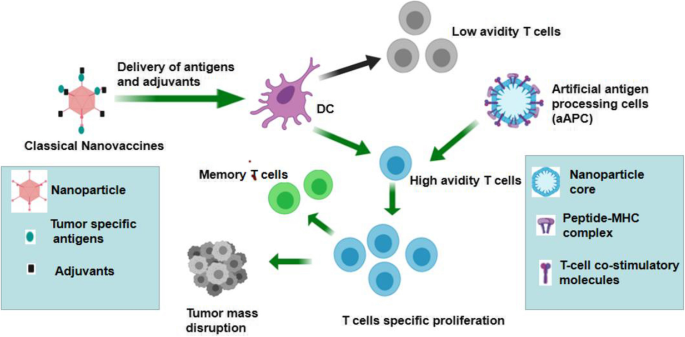
实验所用关键产品:pH响应性聚合物纳米粒、脂质体、mRNA新抗原疫苗载体等(文献未明确具体品牌及货号)。
3.2 免疫原性细胞死亡与纳米介导ICD
实验目的为增强传统ICD诱导剂的肿瘤靶向性,降低全身副作用,提升ICD诱导效率,进而增强抗肿瘤免疫应答。方法上综述了纳米载体包裹传统ICD诱导剂(如奥沙利铂、阿霉素、紫杉醇)的应用,以及纳米介导的热疗、放疗等物理ICD诱导策略,如PLGA-mPEG纳米粒包裹奥沙利铂,Fe3O4磁性纳米粒介导的磁热疗,金纳米粒介导的光热疗。结果显示纳米介导的ICD诱导可促进损伤相关分子模式(DAMPs)的释放,包括钙网蛋白(CRT)、热休克蛋白(HSP)、ATP、高迁移率族蛋白B1(HMGB1),增强DC细胞的活化与抗原提呈,进而诱导强效的CTL应答,抑制肿瘤生长并产生远隔效应。
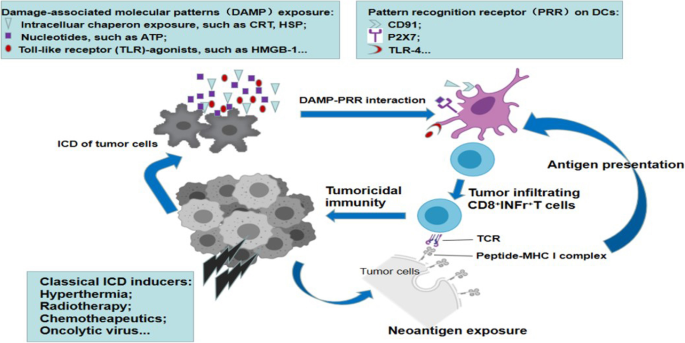
实验所用关键产品:PLGA-mPEG纳米粒、Fe3O4磁性纳米粒、金纳米粒等(文献未明确具体品牌及货号)。
3.3 肿瘤免疫微环境的纳米重塑策略
实验目的为靶向重塑肿瘤免疫抑制微环境,将冷肿瘤转化为热肿瘤,提升免疫治疗的应答率。方法上综述了纳米技术在靶向免疫检查点、调节DC细胞功能、重编程肿瘤相关巨噬细胞(TAM)、抑制髓源性抑制细胞(MDSC)、调节细胞因子与代谢酶等方面的应用,如脂质鱼精蛋白-DNA(LPD)纳米粒负载PD-L1拮抗剂质粒,TiO2纳米粒促进DC成熟,脂质纳米粒负载siRNA靶向TAM的CCR2受体,纳米载体联合递送TGF-β拮抗剂与IL-2。结果显示纳米介导的肿瘤免疫微环境重塑可有效降低免疫检查点抑制剂的全身毒性,增强DC细胞的抗原提呈功能,将M2型TAM重编程为M1型,抑制MDSC的免疫抑制功能,调节细胞因子平衡与代谢酶活性,显著提升肿瘤内CTL的浸润,抑制肿瘤生长并延长荷瘤小鼠生存期。
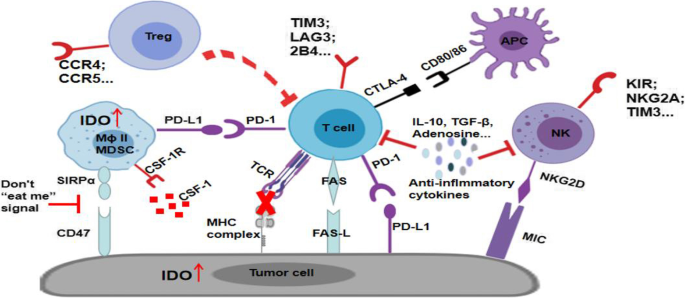
实验所用关键产品:LPD纳米粒、TiO2纳米粒、脂质纳米粒等(文献未明确具体品牌及货号)。
4. Biomarker研究及发现成果
本文综述涉及三类关键Biomarker,分别为肿瘤新抗原、免疫原性细胞死亡相关DAMPs、肿瘤免疫微环境分型标志物,系统总结了这些Biomarker的筛选、验证逻辑及临床应用价值。
Biomarker定位方面,肿瘤新抗原为肿瘤特异性突变抗原,筛选逻辑为通过全外显子测序、转录组测序、质谱技术鉴定肿瘤体细胞突变,预测其与主要组织相容性复合体(MHC)的亲和力及免疫原性;ICD相关DAMPs包括CRT、HSP、ATP、HMGB1,验证逻辑为检测肿瘤细胞死亡后这些分子的释放与表面暴露水平;肿瘤免疫微环境分型标志物包括PD-L1、CD8B、Treg细胞、M2型TAM,筛选逻辑为通过基因表达谱、免疫组化、流式细胞术分析临床样本中的标志物表达水平,将肿瘤微环境分为热肿瘤、冷肿瘤等亚型。
研究过程详述中,肿瘤新抗原来源于肿瘤体细胞突变,通过高通量组学技术筛选后,经纳米疫苗递送至APC细胞,诱导抗原特异性CTL应答;DAMPs在纳米介导的ICD诱导后释放,通过ELISA、免疫荧光、流式细胞术等方法检测其水平,作为ICD发生的标志物;肿瘤免疫微环境标志物通过临床样本的基因表达谱分析(如HOPE项目基于PD-L1与CD8B表达将微环境分为4型),指导纳米免疫治疗策略的选择,如针对PD-L1+CD8B+的热肿瘤,联合纳米疫苗与免疫检查点抑制剂可增强疗效。
核心成果提炼方面,肿瘤新抗原作为个性化纳米疫苗的核心靶点,可诱导强效的肿瘤特异性免疫应答,避免免疫耐受;DAMPs作为ICD的特异性标志物,可用于评估纳米介导ICD的效率;PD-L1、CD8B等微环境标志物可用于肿瘤免疫分型,指导精准纳米免疫治疗策略的制定。其中,部分研究显示纳米新抗原疫苗联合免疫检查点抑制剂可使已建立的肿瘤进一步缩小(文献未明确具体样本量及P值),纳米介导的ICD诱导可显著提升荷瘤小鼠的生存期(文献未明确具体样本量及P值)。
