1. 领域背景与文献引入
文献英文标题:Phosphatidylinositol 3-kinase-δ (PI3K-δ) is a potential therapeutic target in adult T-cell leukemia-lymphoma;发表期刊:Biomark Res;影响因子:未公开;研究领域:成人T细胞白血病淋巴瘤(ATL)靶向治疗
成人T细胞白血病淋巴瘤是由人类T淋巴细胞病毒I型(HTLV-1)感染引发的外周T淋巴细胞恶性肿瘤,领域共识:约5%的HTLV-1携带者会在终身发展为ATL。该疾病根据临床特征分为急性型、淋巴瘤型、慢性型和冒烟型四种亚型,其中慢性型又进一步分为预后良好与不良亚型,急性型、淋巴瘤型及不良慢性型被归为侵袭性ATL。目前侵袭性ATL的一线治疗方案为多细胞毒药物化疗联合人源化抗CCR4单克隆抗体或抗病毒治疗,但患者预后仍极差,5年生存率不足30%,临床亟需探索新型治疗策略。磷脂酰肌醇3-激酶(PI3K)通路是人类癌症中常见异常激活的信号通路,其中PI3K-δ亚型的表达通常局限于造血细胞,是调控特定癌症细胞存活的关键分子,其抑制剂idelalisib已被证实对慢性淋巴细胞白血病具有显著治疗效果。基于ATL现有治疗的局限性及PI3K-δ抑制剂的临床潜力,本研究聚焦ATL细胞中PI3K-δ的表达特征及idelalisib的抗肿瘤效应,旨在为ATL的靶向治疗提供新的靶点依据。
2. 文献综述解析
作者对领域内现有研究的分类维度涵盖ATL治疗现状、PI3K通路在癌症中的调控作用、PI3K-δ抑制剂在其他血液系统恶性肿瘤的应用、ATL中PI3K通路的激活机制四个核心方向。现有研究已明确ATL的发病机制与临床亚型特征,证实侵袭性ATL现有治疗方案的局限性,同时揭示PI3K通路在多种癌症中通过调控细胞存活、增殖发挥促癌作用,PI3K-δ作为造血细胞特异性亚型,其抑制剂idelalisib在慢性淋巴细胞白血病中展现出良好的治疗潜力。在ATL相关研究中,已有证据表明HTLV-1的反式激活蛋白Tax可通过下调磷酸酶及张力蛋白同源物(PTEN)激活PI3K-AKT通路,趋化因子受体CCR4的功能获得性突变也可通过结合配体CCL22激活该通路,进而促进ATL细胞存活。现有研究的技术方法多采用细胞系转染模型,虽能揭示通路调控机制,但缺乏原代临床样本的验证,无法直接反映临床治疗潜力,且未针对PI3K-δ抑制剂在ATL中的效应进行直接验证。本研究的创新价值在于首次利用原代ATL患者样本,直接验证PI3K-δ抑制剂idelalisib的促凋亡效应及对CCL22诱导存活信号的阻断作用,弥补了现有研究在临床转化层面的不足,为ATL的靶向治疗提供了直接的临床前依据。
3. 研究思路总结与详细解析
本研究的核心目标是验证PI3K-δ作为ATL潜在治疗靶点的有效性,核心科学问题为PI3K-δ抑制剂idelalisib是否能特异性诱导ATL细胞凋亡并阻断其依赖的PI3K-AKT存活通路,技术路线遵循“分子表达检测→药物效应验证→通路机制解析”的闭环逻辑,通过临床样本检测与原代细胞功能实验相结合的方式完成研究验证。
3.1 PI3K活性与PI3K-δ蛋白表达检测
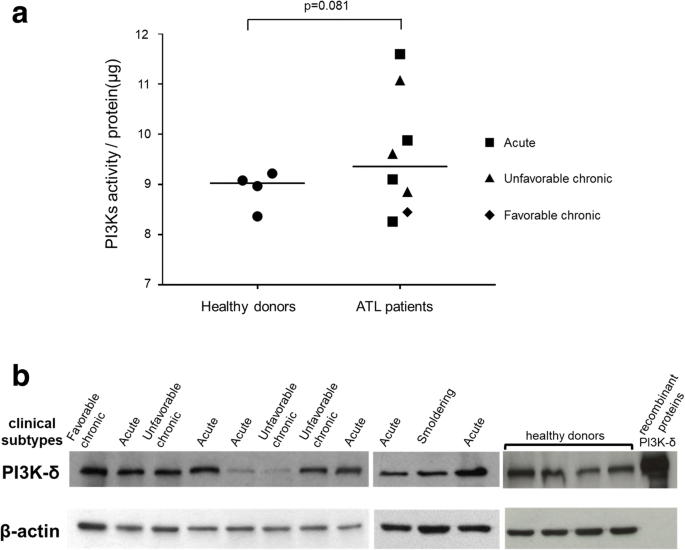
本环节的实验目的是明确ATL患者与健康人群的PI3K通路活性差异,以及ATL细胞中PI3K-δ蛋白的表达特征。实验方法上,研究人员采用PI3-Kinase Activity ELISA试剂盒,对4例健康供体和8例ATL患者的CD4+细胞进行PI3K活性定量检测,细胞分离使用Dynabeads磁珠;同时采用免疫印迹(Western Blot)技术,对11例肿瘤细胞占外周血单个核细胞(PBMC)比例超过75%的ATL患者及4例健康供体的PBMC样本进行PI3K-δ蛋白表达检测。实验结果显示,健康供体与ATL患者的平均PI3K活性无显著差异(n=4/8,P>0.05,文献未明确具体数值),但部分ATL病例的PI3K活性极高;PI3K-δ蛋白在多数ATL病例中可检测到,不同患者间的表达水平存在个体差异。
3.2 Idelalisib对原代ATL细胞凋亡的影响
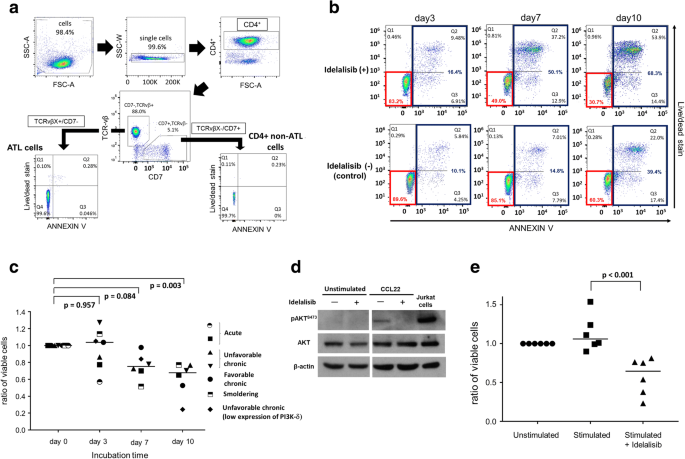
本环节的实验目的是验证idelalisib对原代ATL细胞的促凋亡效应,并明确其对患者体内非恶性T细胞的影响。实验方法分为两个阶段,首先对4例ATL患者的冻存复苏PBMC样本,采用0.1-100μM浓度梯度的idelalisib处理72小时后检测细胞活力;随后选取7例涵盖不同临床亚型的ATL患者新鲜分离PBMC,采用10μM idelalisib进行0-10天的培养,通过流式细胞术结合TCR-Vβ亚基与CD7染色区分ATL细胞与非恶性T细胞,利用Annexin V和死细胞染色试剂盒检测细胞凋亡情况。实验结果显示,3例患者的冻存样本细胞活力随idelalisib浓度升高呈剂量依赖性降低;新鲜样本中,idelalisib以时间依赖性方式诱导ATL细胞凋亡,培养10天时存活ATL细胞比例显著降低(n=7,P<0.05,文献未明确具体数值),且即使PI3K-δ表达水平较低的ATL样本也呈现出相似的凋亡效应;同一患者的非恶性T细胞未出现idelalisib诱导的时间依赖性凋亡。
3.3 Idelalisib对CCL22诱导PI3K-AKT通路的阻断作用
本环节的实验目的是解析idelalisib对ATL细胞存活信号通路的调控机制,重点验证其对CCL22诱导的PI3K-AKT通路的阻断效应。实验方法上,研究人员从ATL患者新鲜PBMC中分离CD4+细胞,经idelalisib预处理30分钟后,采用50μg/ml的CCL22刺激2小时,通过免疫印迹检测AKT在Ser473位点的磷酸化水平;同时选取6例ATL患者的PBMC样本,经CD8+细胞去除后用idelalisib预处理,再加入CCL22培养0-10天,检测细胞增殖情况。实验结果显示,CCL22刺激可显著诱导ATL细胞中AKT的Ser473位点磷酸化,而idelalisib可完全阻断该磷酸化效应;此外,idelalisib可显著抑制CCL22诱导的ATL细胞增殖(n=6,P<0.05,文献未明确具体数值)。实验所用关键产品:PI3-Kinase Activity ELISA kit(Echelon)、Dynabeads(Invitrogen)、Beckman Coulter IOTest Beta mark单抗试剂盒、Annexin V(BioLegend)、Fixable Dead Cell Stain(Thermo Fisher)、CCL22(R&D SYSTEMS)。
4. Biomarker研究及发现成果
本研究中PI3K-δ及PI3K通路活性作为潜在的ATL治疗响应Biomarker,其筛选与验证逻辑为“临床样本分子特征检测→靶向药物功能验证→通路机制确认”的完整链条。Biomarker的来源为ATL患者的临床血液样本,包括外周血CD4+细胞与PBMC样本。验证方法上,采用ELISA定量检测PI3K通路活性,免疫印迹检测PI3K-δ蛋白表达,通过原代细胞培养结合流式细胞术、免疫印迹技术验证靶向药物的效应。特异性方面,idelalisib可特异性诱导ATL细胞凋亡,对同一患者的非恶性T细胞无显著时间依赖性影响;敏感性方面,部分PI3K活性极高的ATL病例对idelalisib的响应更为显著,且低PI3K-δ表达的ATL细胞也可被idelalisib诱导凋亡。核心成果方面,本研究证实PI3K-δ是ATL的潜在治疗靶点,idelalisib可通过诱导ATL细胞凋亡、阻断CCL22介导的PI3K-AKT存活通路发挥抗肿瘤效应,为ATL的靶向治疗提供了直接的临床前证据;研究未提供该Biomarker的诊断特异性与敏感性量化数据(如ROC曲线),但明确了PI3K通路激活的ATL病例可能对idelalisib治疗产生响应,为后续临床研究提供了方向。
