1. 领域背景与文献引入
文献英文标题:Metallothionein-3 is a multifunctional driver that modulates the development of sorafenib-resistant phenotype in hepatocellular carcinoma cells;发表期刊:Biomark Res;影响因子:未公开;研究领域:肝细胞癌耐药机制与生物标志物研究。
肝细胞癌是全球范围内发病率与死亡率均居前列的恶性肿瘤,领域共识:手术切除是早期肝细胞癌的首选治疗方案,但由于疾病早期症状隐匿,约70%的患者确诊时已处于晚期,失去手术机会。索拉非尼作为晚期肝细胞癌的一线系统治疗药物,通过抑制多激酶通路发挥抗肿瘤作用,但仅约30%的患者能从中获益,且多数患者在治疗6个月内出现耐药,其耐药机制尚未完全阐明,成为制约肝癌治疗效果提升的核心瓶颈。现有研究表明,金属硫蛋白(MT)家族因具备活性氧(ROS)清除能力,与多种肿瘤化疗耐药密切相关,其中MT1G已被证实通过抑制铁死亡参与肝细胞癌索拉非尼耐药调控,但MT家族中结构独特的MT3亚型在肝细胞癌耐药中的功能尚未见系统性报道,这一研究空白限制了对肝癌耐药多维度机制的理解,也缺乏针对性的干预靶点。本文旨在明确人源MT3(hMT3)在肝细胞癌索拉非尼耐药中的功能,并解析其调控的分子通路,为耐药肝癌的精准治疗提供新的靶点与生物标志物。
2. 文献综述解析
作者围绕MT家族不同亚型的功能差异、肝细胞癌索拉非尼耐药的现有机制两大维度展开综述,分类维度涵盖MT亚型的结构特性与肿瘤功能、耐药机制的分子层面(ROS清除、药物转运、细胞凋亡抑制、代谢重编程等)。
现有研究显示,MT家族中的MT1、MT2亚型在部分肿瘤中可通过清除ROS、抑制细胞凋亡等途径促进化疗耐药,其中MT1G已被证实通过调控铁死亡参与肝细胞癌索拉非尼耐药;索拉非尼耐药的机制还包括肿瘤细胞药物转运体上调、抗凋亡通路激活、糖酵解增强等,但这些研究多聚焦于已知通路,对MT3这类结构独特的亚型关注不足,且缺乏对MT3调控肝癌耐药的系统性研究,现有研究的局限性在于未揭示MT3在肝癌中的功能,也未阐明其与索拉非尼耐药的直接关联。
本文通过对比固有耐药与敏感肝癌细胞系的转录组差异,首次发现hMT3在耐药细胞中显著高表达,并通过细胞与体内实验证实hMT3可将敏感肝癌细胞重塑为耐药表型,填补了MT3在肝癌耐药研究中的空白,为肝癌耐药机制提供了新的视角,也为耐药患者的精准分层治疗提供了潜在的生物标志物与干预靶点。
3. 研究思路总结与详细解析
本文的研究目标是明确hMT3在肝细胞癌索拉非尼耐药中的功能及调控机制,核心科学问题是hMT3如何通过多通路调控肝癌细胞的耐药表型,技术路线遵循“耐药细胞系差异筛选→基因功能验证→代谢与分子机制解析→体内模型验证→蛋白质组学通路阐释”的闭环逻辑。
3.1 肝癌细胞系索拉非尼敏感性验证
实验目的:验证固有耐药(BCLC-3WT)与敏感(Huh7WT)肝癌细胞系对索拉非尼的敏感性差异,为后续研究奠定细胞模型基础。
方法细节:采用MTT法检测2D培养细胞的药物敏感性,将约2.5×10^4个细胞接种于48孔板,培养过夜后给予不同浓度索拉非尼处理24小时,加入MTT试剂孵育3小时后检测吸光度;采用悬滴法构建3D球状体模型,将约1×10^4个细胞悬滴培养4天形成球状体,给予索拉非尼处理24小时后,通过EVOS FL显微镜拍摄图像,使用ImageJ软件定量分析球状体面积。
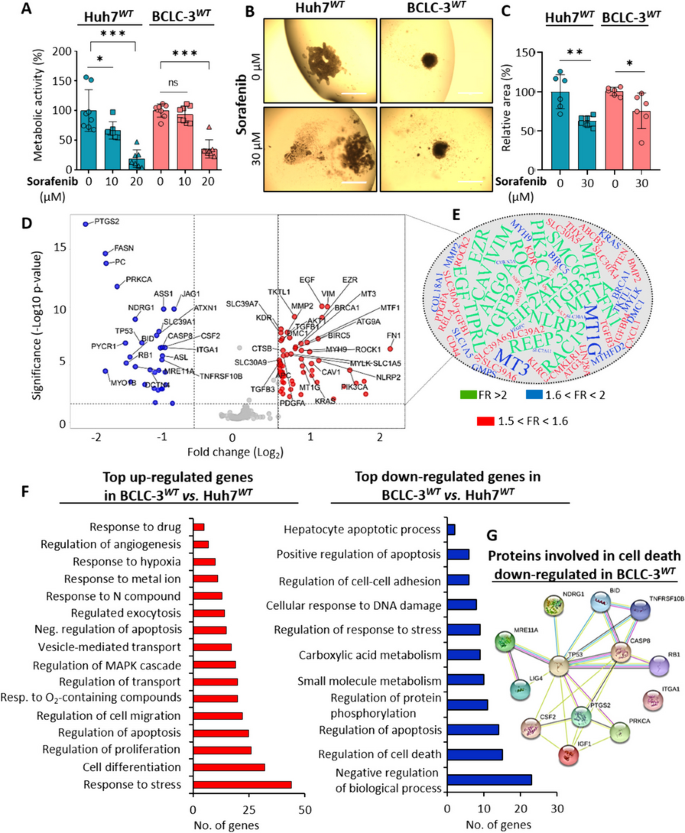
结果解读:2D培养中BCLC-3WT细胞对索拉非尼的耐药性显著高于Huh7WT细胞;3D球状体实验显示,索拉非尼处理后Huh7WT球状体面积减少37.7±6.02%(n=3,P≤0.05),而BCLC-3WT球状体面积仅减少24.4±20.7%,进一步验证了两种细胞系的敏感性差异,且3D模型更贴近体内肿瘤的耐药特性。
产品关联:实验所用关键产品:Sigma-Aldrich的3-(4,5-二甲基噻唑-2-基)-2,5-二苯基四氮唑溴盐(MTT)试剂、Thermo Fisher Scientific的EVOS FL荧光显微镜、美国国立卫生研究院(NIH)的ImageJ图像分析软件。
3.2 转录组筛选耐药相关基因
实验目的:筛选固有耐药与敏感肝癌细胞系的差异表达基因,鉴定与索拉非尼耐药相关的关键分子。
方法细节:提取BCLC-3WT与Huh7WT细胞的总RNA,反转录为cDNA后进行电化学cDNA微阵列分析,将cDNA 3"端生物素标记后与ElectraSense 4×2k芯片杂交,设置差异表达阈值为fold ratio≥1.5(上调)或≤0.5(下调);通过STRING软件对差异基因进行功能富集分析。
结果解读:转录组分析显示,BCLC-3WT与Huh7WT细胞存在显著的转录组差异,共鉴定出64个上调基因与33个下调基因;其中hMT3、MT1G、MT1A等MT家族基因在耐药细胞中显著高表达;功能富集分析显示,上调基因参与应激反应、增殖调控、血管生成、药物转运等通路,下调基因参与凋亡、DNA损伤修复等通路,提示hMT3可能参与耐药调控。
产品关联:实验所用关键产品:Roche的高纯度总RNA提取试剂盒、Thermo Fisher Scientific的Biotin 3" End DNA Labeling Kit、Custom Array的ElectraSense 4×2k芯片。

3.3 hMT3过表达细胞系构建与功能验证
实验目的:验证hMT3过表达是否可诱导敏感肝癌细胞产生索拉非尼耐药表型,并分析其临床相关性。
方法细节:构建hMT3过表达质粒,通过Lipofectamine 2000转染Huh7WT细胞,获得Huh7hMT3细胞,同时构建空载体转染的Huh7mock细胞作为对照;采用qRT-PCR验证hMT3表达水平;采用实时细胞阻抗检测(xCELLigence)检测细胞增殖能力;采用MTT法和3D球状体实验检测索拉非尼敏感性;通过临床数据库(TNMplot、cBioPortal、Kaplan-Meier plotter)分析hMT3在肝癌组织中的表达及与预后的关联。
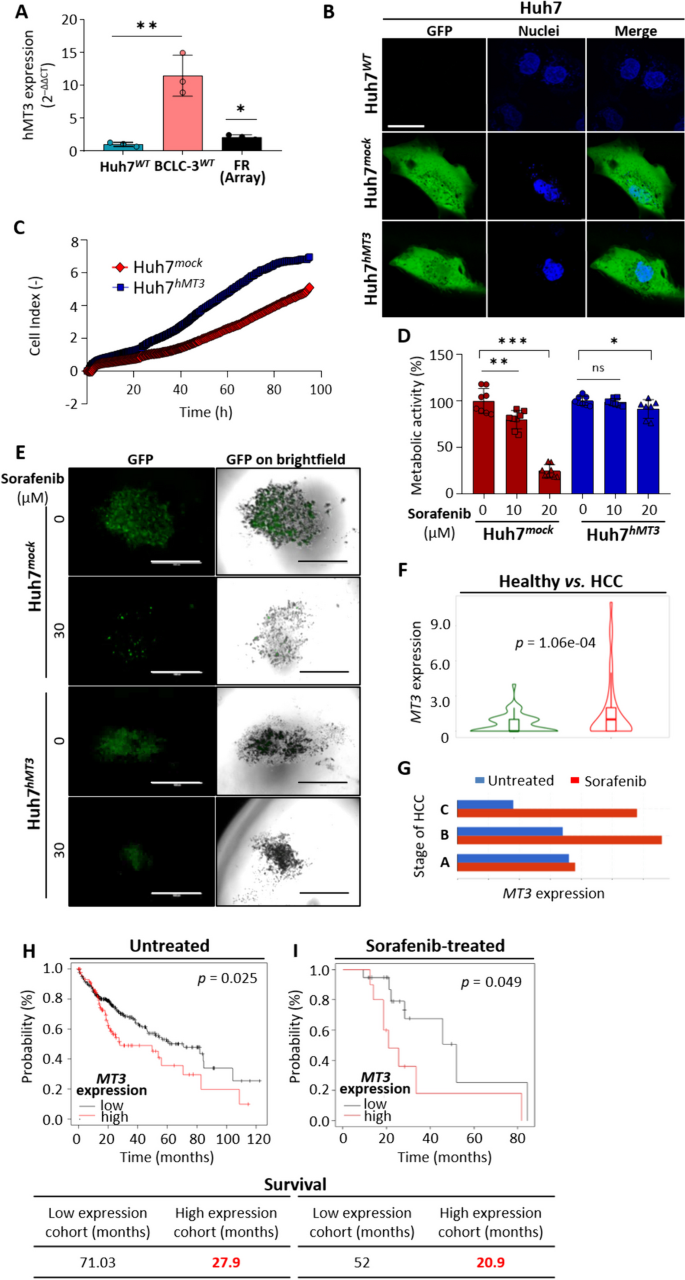
结果解读:转染后Huh7hMT3细胞的hMT3表达水平较对照升高约12倍;hMT3过表达显著促进Huh7细胞增殖;2D培养中Huh7hMT3细胞对索拉非尼的耐药性显著高于Huh7mock细胞;3D球状体实验显示,索拉非尼对Huh7hMT3球状体面积的抑制作用显著降低;临床数据库分析显示,肝癌组织中hMT3表达显著高于正常肝组织(n=50,P≤0.05),索拉非尼治疗的晚期肝癌患者中hMT3表达更高,且高表达hMT3的肝癌患者总生存期显著低于低表达患者(n=364,P≤0.05),索拉非尼治疗的高hMT3患者生存期更短(n=30,P≤0.05)。
产品关联:实验所用关键产品:Thermo Fisher Scientific的Lipofectamine 2000转染试剂、Analytik Jena的qTOWER3实时荧光定量PCR仪、Roche的xCELLigence RTCA DP细胞增殖分析仪。
3.4 hMT3对细胞代谢与氧化应激的调控
实验目的:解析hMT3调控索拉非尼耐药的代谢与氧化应激机制。
方法细节:采用Seahorse细胞外通量分析仪检测细胞的氧消耗率(OCR)和细胞外酸化率(ECAR),评估线粒体呼吸和糖酵解水平;采用CellROX Deep Red试剂检测总ROS水平,MitoSOX Red试剂检测线粒体超氧化物水平;采用超氧化物歧化酶(SOD)活性检测试剂盒检测SOD活性;采用Annexin V/7-AAD双染流式细胞术检测索拉非尼诱导的细胞凋亡;采用PI染色流式细胞术检测细胞周期分布。
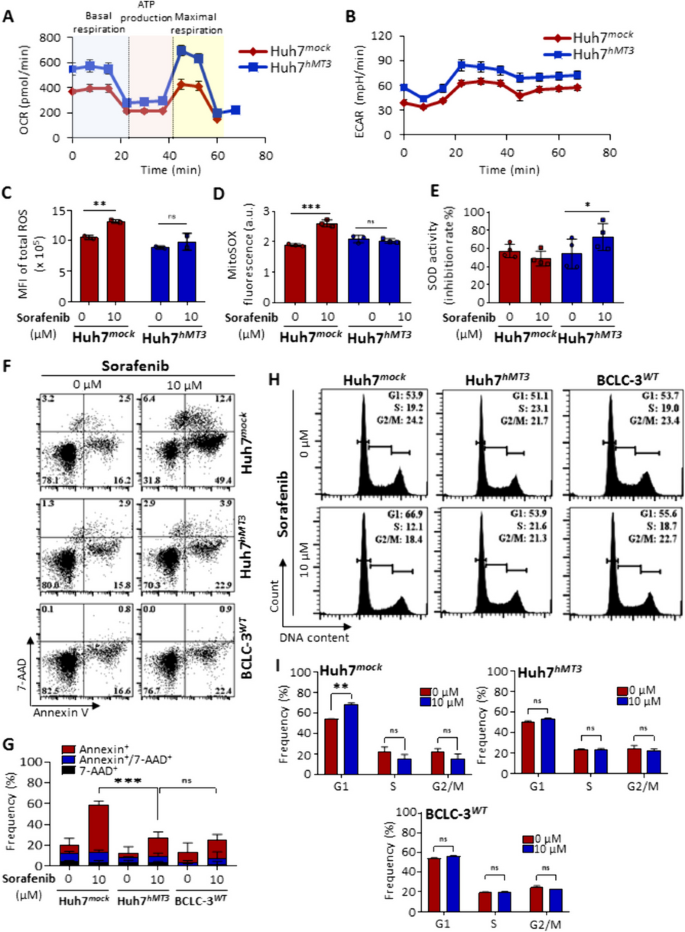
结果解读:hMT3过表达显著提高Huh7细胞的OCR和ECAR水平,增强线粒体呼吸和糖酵解能力;索拉非尼处理后,Huh7mock细胞的总ROS和线粒体超氧化物水平显著升高,而Huh7hMT3细胞无显著变化,且Huh7hMT3细胞的SOD活性显著高于对照(n=3,P≤0.05);hMT3过表达显著抑制索拉非尼诱导的细胞凋亡,且逆转索拉非尼引起的G1期细胞周期阻滞。
产品关联:实验所用关键产品:Seahorse Biosciences的细胞外通量分析仪、Thermo Fisher Scientific的CellROX Deep Red和MitoSOX Red试剂、Abcam的SOD活性检测试剂盒、BD Biosciences的Accuri C6 Plus流式细胞仪。
3.5 体内CAM模型验证hMT3的耐药与转移作用
实验目的:在体内模型中验证hMT3对肝癌细胞索拉非尼耐药及转移能力的调控。
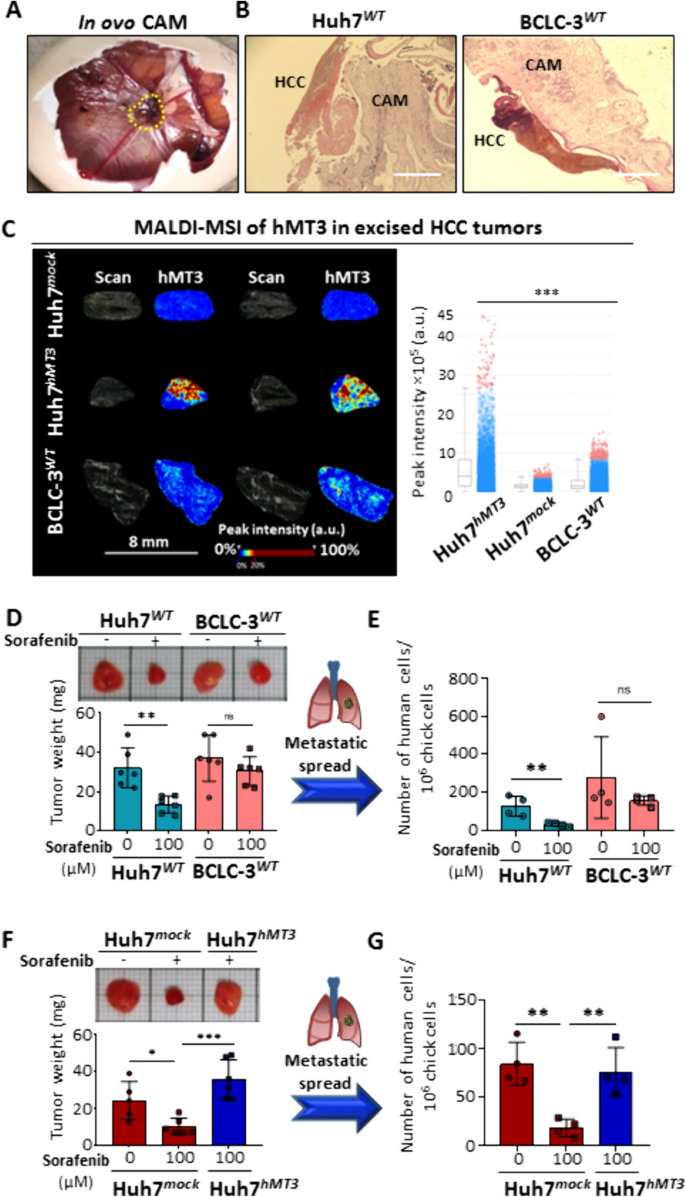
方法细节:采用鸡胚绒毛尿囊膜(CAM)模型,分为ex ovo和in ovo实验;ex ovo实验中,将Huh7mock、Huh7hMT3、BCLC-3WT细胞接种于CAM,培养3天后给予100μM索拉非尼处理,24小时后检测肿瘤面积、肿瘤细胞血管内渗能力及肺转移情况;in ovo实验中,接种细胞后培养7天,给予索拉非尼处理,24小时后检测肿瘤重量及肺转移情况;采用基质辅助激光解吸电离质谱成像(MALDI-MSI)验证肿瘤组织中hMT3的表达。
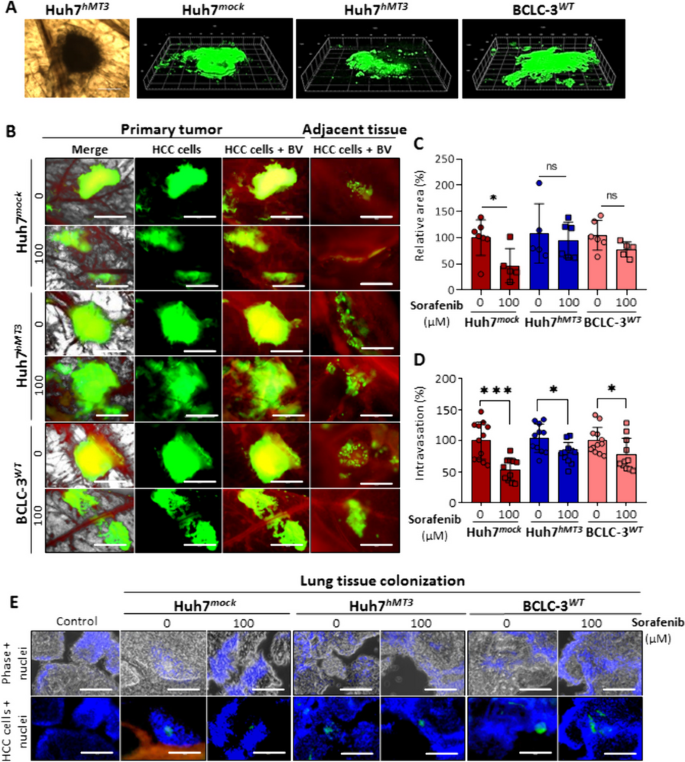
结果解读:ex ovo实验显示,索拉非尼对Huh7hMT3和BCLC-3WT肿瘤面积的抑制作用显著低于Huh7mock细胞,且Huh7hMT3细胞的血管内渗能力受索拉非尼影响较小,肺转移能力显著高于对照;in ovo实验显示,索拉非尼显著降低Huh7mock肿瘤重量,但对Huh7hMT3肿瘤无显著抑制作用,且Huh7hMT3细胞的肺转移能力显著高于对照;MALDI-MSI证实Huh7hMT3肿瘤中hMT3高表达。
产品关联:实验所用关键产品:Invitrogen的CellTracker Green细胞标记试剂、Vector Laboratories的rhodamine-labeled Lens culinaris agglutinin(LCA)、Bruker的ultrafleXtreme MALDI-TOF/TOF质谱仪。
3.6 蛋白质组学解析hMT3调控的分子通路
实验目的:通过蛋白质组学解析hMT3调控肝癌细胞耐药的分子通路。
方法细节:提取Huh7mock和Huh7hMT3细胞的蛋白质,采用液相色谱-串联质谱(LC-MS/MS)进行蛋白质组学分析,采用Mascot搜索引擎对质谱数据进行鉴定,设置差异表达阈值为fold ratio≥1.5(上调)或≤0.5(下调);通过STRING和METASCAPE对差异蛋白进行功能富集分析;对比Huh7hMT3与BCLC-3WT细胞的蛋白质组,筛选共同差异表达蛋白;采用BODIPY染色检测小鼠原代肝细胞的脂质体积累情况。
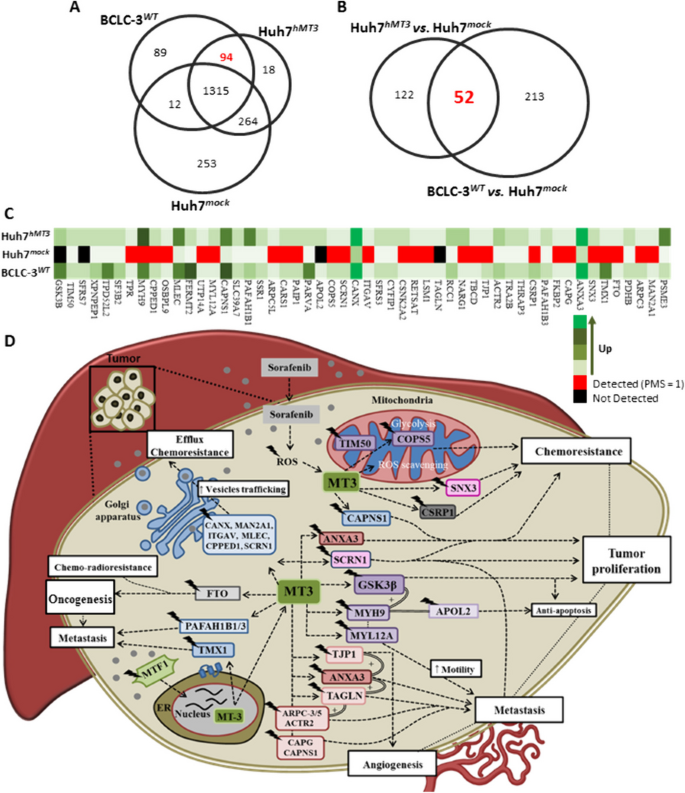
结果解读:蛋白质组学分析共鉴定1869种蛋白,其中25种蛋白仅在Huh7hMT3细胞中表达,197种蛋白上调、103种蛋白下调;功能富集分析显示,上调蛋白参与胞吐作用、糖酵解、血管生成、细胞应激等通路,下调蛋白参与脂质代谢、氨基酸代谢等通路;Huh7hMT3与BCLC-3WT细胞存在94种共同上调蛋白,提示hMT3过表达可使敏感细胞的蛋白质组向耐药细胞转变;进一步验证显示,hMT3过表达抑制肝细胞内脂质体积累,与脂质代谢通路下调一致。
产品关联:实验所用关键产品:Thermo Fisher Scientific的Easy-nLC 1000液相色谱系统、Q-Exactive质谱仪、Matrix Science的Mascot搜索引擎。

4. Biomarker研究及发现成果
本文鉴定的Biomarker为金属硫蛋白3(hMT3),属于蛋白质类生物标志物,筛选逻辑为通过固有耐药与敏感肝癌细胞系的转录组差异筛选到hMT3,经细胞功能实验验证其可诱导耐药表型后,通过多中心临床数据库进行临床相关性验证,形成“细胞系差异筛选→细胞功能验证→临床预后关联”的完整逻辑链条。
hMT3的来源为肝癌细胞系及临床肝癌组织样本;验证方法包括qRT-PCR检测细胞系中hMT3表达水平,通过TNMplot数据库分析肝癌组织与正常组织的表达差异,通过cBioPortal数据库分析不同分期肝癌及索拉非尼治疗患者的hMT3表达,通过Kaplan-Meier plotter数据库分析hMT3与患者总生存期的关联;特异性与敏感性数据显示,肝癌组织中hMT3表达显著高于正常肝组织(n=50,P≤0.05),索拉非尼治疗的晚期肝癌患者中hMT3表达显著升高,高表达hMT3的肝癌患者总生存期显著低于低表达患者(n=364,P≤0.05),索拉非尼治疗的高hMT3患者生存期更短(n=30,P≤0.05),提示hMT3对索拉非尼耐药患者的预后具有一定的预测价值。
hMT3的功能关联为作为多功能驱动因子,通过调控线粒体代谢、糖酵解、氧化应激、细胞凋亡、血管生成等通路,诱导肝癌细胞索拉非尼耐药,并促进肿瘤转移;创新性在于首次揭示hMT3在肝癌索拉非尼耐药中的功能及调控机制,填补了MT3在肝癌研究中的空白;统计学结果显示,hMT3在肝癌组织中的表达与正常组织存在显著差异(P≤0.05),与患者总生存期及索拉非尼治疗后的生存期显著相关(P≤0.05),为耐药肝癌的精准分层治疗提供了潜在的生物标志物。
