1. 领域背景与文献引入
文献英文标题:Repressing HIF-1α-induced HDAC9 contributes to the synergistic effect of venetoclax and MENIN inhibitor in KMT2Ar AML;发表期刊:Biomarker Research;影响因子:未公开;研究领域:KMT2A重排急性髓系白血病精准治疗
急性髓系白血病(AML)是一类异质性极强的血液系统恶性肿瘤,KMT2A重排型AML(KMT2Ar-AML)作为高危亚型,具有疾病进展快、常规化疗响应率低、远期预后差的临床特征。领域共识:BCL2抑制剂维奈克拉(VEN)的问世为AML治疗带来突破性进展,KMT2Ar-AML细胞对维奈克拉单药具有固有敏感性,但现有基于维奈克拉的联合方案(维奈克拉联合阿扎胞苷或低剂量阿糖胞苷)无法为这类患者带来持续临床获益,核心瓶颈在于缺乏针对KMT2A重排特异性的联合治疗靶点。MENIN抑制剂(MEN1i)通过阻断MENIN-KMT2A复合物的形成,下调HOXA9/MEIS1通路发挥抗白血病作用,是针对KMT2Ar-AML的潜在特异性靶点,但维奈克拉与MENIN抑制剂联合的协同效应及分子机制尚未明确,这一研究空白直接限制了KMT2Ar-AML精准联合治疗方案的开发,正是本文的核心研究出发点。
2. 文献综述解析
作者对领域内现有研究的分类维度主要围绕治疗靶点与药物作用机制,分为维奈克拉单药及联合方案、MENIN抑制剂单药研究两大方向。现有研究证实,维奈克拉通过调控BCL-2/BCL-XL蛋白平衡诱导AML细胞凋亡,KMT2Ar-AML细胞对维奈克拉单药敏感,但现有维奈克拉联合方案在KMT2Ar-AML中的疗效存在响应持续时间短、无法改善长期预后的局限性;MENIN抑制剂通过特异性阻断MENIN-KMT2A复合物,下调HOXA9/MEIS1转录因子表达抑制KMT2Ar-AML细胞增殖,但其单药起效缓慢,且长期使用易诱导MEN1基因突变导致耐药,缺乏可快速起效的联合治疗药物。本文的创新价值在于首次系统验证了维奈克拉与MENIN抑制剂在KMT2Ar-AML中的显著协同抗白血病效应,且揭示了完全不同于单药机制的全新协同通路——抑制HIF-1α诱导的HDAC9表达,弥补了现有研究中对两类药物联合作用机制的空白,为KMT2Ar-AML的精准联合治疗提供了关键的理论依据和潜在靶点。
3. 研究思路总结与详细解析
本研究的核心目标是明确维奈克拉(VEN)联合MENIN抑制剂(MEN1i)在KMT2Ar-AML中的协同治疗效应及分子机制,核心科学问题是两类药物协同抗白血病的关键调控通路,技术路线遵循“体外细胞实验验证协同效应→体内动物模型验证疗效→转录组测序筛选差异分子→机制验证与功能研究”的完整闭环,确保研究结论的严谨性与可靠性。
3.1 单药及联合治疗的体外与离体疗效验证
实验目的:验证KMT2Ar-AML细胞对维奈克拉、MENIN抑制剂单药及联合治疗的敏感性,明确协同效应的特异性。
方法细节:选取KMT2Ar-AML细胞系(THP-1、MV4-11、MOLM13)及非KMT2Ar-AML细胞系,通过CCK-8法检测不同浓度维奈克拉、MENIN抑制剂(MI-503、MI-463、VTP-50469)单药及联合处理72小时后的细胞增殖抑制率,使用CalcuSyn软件计算协同指数(CI)评估协同效应;通过流式细胞术检测Annexin V阳性细胞比例,评估不同处理对细胞凋亡的影响;同时纳入原代KMT2Ar-AML细胞、非KMT2Ar-AML细胞及正常骨髓细胞进行离体验证。
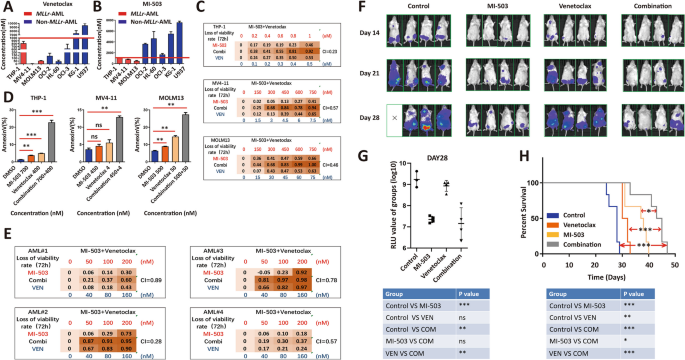
结果解读:实验结果显示,KMT2Ar-AML细胞系对维奈克拉和MENIN抑制剂单药均敏感,联合治疗在KMT2Ar-AML细胞系中呈现显著的增殖抑制协同效应(CI<1),且该协同效应特异性存在于KMT2Ar-AML细胞及原代细胞中,对正常骨髓细胞无显著影响;联合治疗显著增强KMT2Ar-AML细胞的凋亡诱导,Annexin V阳性细胞比例较单药组升高20%-30%(n=3,P<0.01),但对细胞周期分布和细胞分化无明显影响。
产品关联:文献未提及具体实验产品,领域常规使用CCK-8细胞增殖检测试剂盒、Annexin V-FITC/PI凋亡检测试剂盒、流式细胞仪等。
3.2 体内异种移植模型的疗效验证
实验目的:验证维奈克拉联合MENIN抑制剂在体内的抗白血病效应及生存获益。
方法细节:构建MOLM13-Luciferase荧光标记细胞的免疫缺陷小鼠异种移植模型,将小鼠随机分为DMSO对照组、维奈克拉单药组、MI-503单药组及联合治疗组,定期通过活体小动物荧光成像检测小鼠体内肿瘤负荷,记录小鼠生存时间并绘制Kaplan-Meier生存曲线。
结果解读:联合治疗组小鼠的相对荧光强度(RLU)显著低于单药组,28天时肿瘤负荷较单药组降低约50%(n=6,P<0.01);联合治疗组小鼠的生存时间较单药组显著延长,中位生存时间延长约40%(n=6,P<0.001),证实联合治疗在体内具有更强的抗白血病活性,可显著降低肿瘤负荷并改善生存预后。
产品关联:文献未提及具体实验产品,领域常规使用荧光素酶标记细胞系、活体小动物成像系统等。
3.3 协同作用关键分子的筛选与功能验证
实验目的:筛选维奈克拉联合MENIN抑制剂协同作用的关键分子靶点,验证其对KMT2Ar-AML细胞增殖的必要性。
方法细节:对联合治疗及单药治疗的KMT2Ar-AML细胞进行RNA测序,通过差异表达基因分析筛选仅由联合治疗特异性调控的基因,结合功能注释及KMT2Ar-AML相关性筛选出HDAC9;通过实时荧光定量PCR(qRT-PCR)和蛋白质免疫印迹(Western Blot)检测HDAC9的mRNA和蛋白表达水平;通过shRNA敲低HDAC9或使用HDAC9抑制剂TMP-269,检测细胞增殖抑制率的变化,验证HDAC9对KMT2Ar-AML细胞增殖的影响。
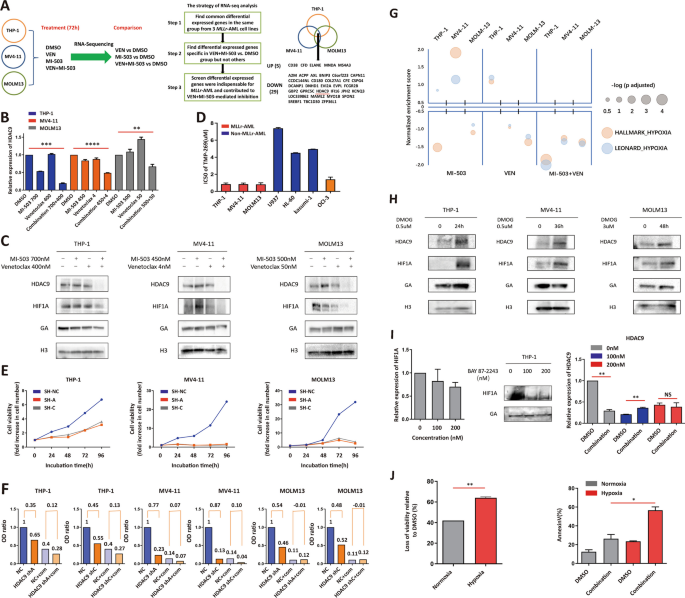
结果解读:RNA测序结果显示HDAC9是唯一被联合治疗特异性下调的基因,qRT-PCR及蛋白质免疫印迹结果证实,联合治疗72小时后KMT2Ar-AML细胞中HDAC9的mRNA和蛋白水平显著降低(n=3,P<0.001),而非KMT2Ar-AML细胞中无此变化;HDAC9敲低或抑制剂处理可显著抑制KMT2Ar-AML细胞增殖,增殖抑制率达30%以上(n=3,P<0.01),且联合治疗的增殖抑制效应在HDAC9敲低细胞中未进一步增强,提示HDAC9是KMT2Ar-AML细胞增殖所必需的,联合治疗通过下调HDAC9表达发挥协同抗白血病效应。
产品关联:文献未提及具体实验产品,领域常规使用RNA测序服务、qRT-PCR试剂盒、蛋白质免疫印迹相关抗体等。
3.4 HIF-1α-HDAC9调控通路的机制验证
实验目的:明确维奈克拉联合MENIN抑制剂下调HDAC9的上游调控通路,解析协同效应的核心分子机制。
方法细节:通过基因集富集分析(GSEA)筛选联合治疗调控的信号通路;使用缺氧诱导剂DMOG处理KMT2Ar-AML细胞,检测HIF-1α和HDAC9的蛋白表达水平;使用HIF-1α抑制剂BAY 87-2243预处理细胞,检测联合治疗对HDAC9表达的影响;在常氧和缺氧条件下,检测联合治疗对细胞活力和凋亡的影响。
结果解读:GSEA分析显示缺氧通路被联合治疗显著抑制;DMOG处理可稳定HIF-1α蛋白并上调HDAC9表达,证实HDAC9是HIF-1α的下游靶基因;HIF-1α抑制剂预处理可部分逆转联合治疗对HDAC9的下调作用(n=3,P<0.05),提示联合治疗通过抑制HIF-1α进而下调HDAC9表达;缺氧条件下联合治疗对KMT2Ar-AML细胞的增殖抑制和凋亡诱导效应较常氧条件下更显著,凋亡率升高约25%(n=3,P<0.001),进一步证实HIF-1α-HDAC9通路是联合治疗协同效应的核心机制。
产品关联:文献未提及具体实验产品,领域常规使用GSEA分析工具、缺氧诱导剂、HIF-1α抑制剂等。
4. Biomarker研究及发现成果解析
Biomarker定位:本文涉及的核心Biomarker为HDAC9,属于表观遗传调控类Biomarker,其筛选与验证遵循“转录组测序筛选联合治疗特异性差异基因→细胞系及原代细胞验证表达特异性→功能实验验证必要性→上游通路验证调控机制”的完整逻辑链条,确保Biomarker的可靠性与临床转化潜力。
研究过程详述:HDAC9的研究样本来源为KMT2Ar-AML细胞系、原代KMT2Ar-AML细胞及异种移植小鼠模型,验证方法包括实时荧光定量PCR检测mRNA表达水平、蛋白质免疫印迹检测蛋白表达水平、shRNA敲低及抑制剂处理验证功能;特异性方面,HDAC9仅在KMT2Ar-AML细胞中被联合治疗特异性下调,非KMT2Ar-AML细胞及正常骨髓细胞中无此变化;敏感性数据显示,HDAC9敲低可使KMT2Ar-AML细胞增殖抑制率提升30%以上(n=3,P<0.01),缺氧条件下联合治疗的凋亡诱导率较常氧条件升高约25%(n=3,P<0.001)。
核心成果提炼:HDAC9作为KMT2Ar-AML细胞增殖的必需分子,其表达受HIF-1α转录调控,维奈克拉联合MENIN抑制剂通过抑制HIF-1α进而下调HDAC9表达,介导协同抗白血病效应;本研究的创新性在于首次在KMT2Ar-AML中发现HIF-1α-HDAC9通路是维奈克拉与MENIN抑制剂协同作用的核心靶点,为KMT2Ar-AML的精准联合治疗提供了新的Biomarker和治疗通路;统计学结果显示,联合治疗组的细胞凋亡率较单药组升高20%-30%(n=3,P<0.01),小鼠中位生存时间延长约40%(n=6,P<0.001),充分证实了该治疗方案的有效性。
