1. 领域背景与文献引入
文献英文标题:The drive to generate multiple forms of oncogenic cyclin D1 transcripts in mantle cell lymphoma;发表期刊:Biomarker Research;影响因子:未公开;研究领域:血液肿瘤(套细胞淋巴瘤)、细胞周期调控、RNA后转录调控
套细胞淋巴瘤(MCL)是一类高度侵袭性B细胞淋巴瘤,疾病复发后被认为临床不可治愈,细胞周期蛋白D1(CCND1)是其发病机制的核心驱动因子。领域共识:MCL的起始病变是前B淋巴细胞分化过程中V(D)J重组异常导致的t(11;14)(q13;q32)染色体易位,该易位使CCND1基因座置于免疫球蛋白重链(IgH)内含子调控增强子(Eμ)下游,激活原本在正常B淋巴细胞中沉默的CCND1启动子,引发CCND1异常表达。然而,现有研究表明,CCND1启动子的转录激活仅是其异常表达的起始环节,领域内尚未完全阐明转录后水平的调控机制如何进一步增强CCND1 mRNA的稳定性,从而维持其异常翻译并促进肿瘤进展。本文正是针对这一研究空白,聚焦于CCND1 3"非翻译区(3"UTR)缩短的分子机制,解析其如何逃逸微小RNA(miRNA)的调控,为MCL的预后判断和靶向治疗提供新的理论依据。
2. 文献综述解析
本文的文献综述以CCND1在MCL中的核心调控作用为切入点,围绕CCND1 mRNA的转录后调控,特别是3"UTR可变多聚腺苷酸化(alternative polyadenylation, APA)的分子机制展开评述,作者将现有研究中CCND1 3"UTR缩短的机制分为两类:一是CCND1基因内部突变产生提前的经典多聚腺苷酸化信号(PAS),二是染色体重排产生嵌合3"UTR并由融合基因提供经典PAS;同时对比了不同PAS序列对转录本加工效率的影响,明确了现有研究在嵌合3"UTR鉴定及功能验证方面的不足,凸显了本文的创新价值。
现有研究已证实,MCL患者中CCND1的t(11;14)易位是肿瘤发生的起始事件,但转录后调控机制对CCND1表达的增强作用同样关键。临床样本研究显示,表达全长CCND1转录本的MCL患者平均生存期比表达3"UTR截短型转录本的患者长约2年,这表明CCND1转录本的类型具有重要的预后价值。生物信息学分析结果表明,CCND1全长3"UTR可被80余种miRNA结合并调控,而3"UTR的缩短可使CCND1 mRNA逃逸这些miRNA的抑制,从而维持高表达。现有研究的优势在于通过临床样本与生存数据的关联,明确了CCND1转录本类型的临床意义,并利用生物信息学工具预测了miRNA结合位点,为转录后调控机制的研究奠定了基础;但局限性在于,对3"UTR截短的具体分子机制,尤其是嵌合3"UTR的产生过程及功能验证的研究较为匮乏,且不同PAS序列对转录本加工的影响尚未得到系统解析。
本文的创新点在于首次在MCL中鉴定出CCND1/肌强直性营养不良激酶相关Cdc42结合激酶(MRCK)融合基因,该融合基因由MRCK序列提供经典PAS,形成嵌合3"UTR,从而促进CCND1转录本的3"端加工并缩短3"UTR;同时系统解析了不同PAS序列(经典与非经典)对CCND1转录本加工的影响,补充了MCL中CCND1转录后调控的新机制,为MCL的特异性靶向治疗提供了潜在靶点。
3. 研究思路总结与详细解析
本文的研究目标是解析MCL中CCND1转录本3"UTR缩短的分子机制,明确不同PAS序列对转录本加工的影响,以及截短型转录本对miRNA调控的逃逸能力;核心科学问题是MCL中CCND1如何通过3"UTR的可变多聚腺苷酸化或染色体重排逃逸miRNA的调控;技术路线遵循“临床现象关联→分子机制解析→功能实验验证→治疗展望”的逻辑闭环,通过临床样本分析、细胞系实验、生物信息学预测和报告基因实验等多种技术手段,系统阐明了CCND1转录本多样性的产生机制及功能意义。
3.1 CCND1转录本3"UTR的序列特征与细胞系验证
实验目的:明确CCND1全长3"UTR中潜在PAS的分布及序列特征,验证不同细胞系中CCND1转录本3"UTR的长度差异及PAS使用情况。
方法细节:首先通过生物信息学分析CCND1基因的全长序列,定位所有潜在的PAS位点;随后对MCL细胞系Jeko-1和乳腺癌细胞系MCF7进行3"cDNA末端快速扩增(3"RACE)实验,获取CCND1转录本的3"UTR序列,并通过Sanger测序验证其PAS序列;同时结合临床样本数据,分析不同PAS使用与患者预后的关联。
结果解读:如图1所示,
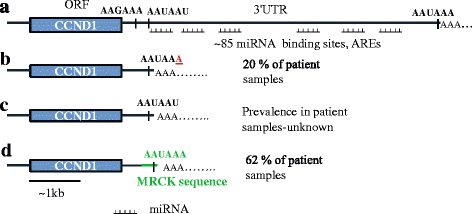
,CCND1全长3"UTR包含多个潜在PAS,其中经典PAS(AAUAAA)位于开放阅读框的远端,两个非经典PAS(AAGAAA、AAUAAU)则靠近终止密码子;Jeko-1细胞系使用非经典近端PAS(AAUAAU)产生长度为318nt的3"UTR,而MCF7细胞系使用更上游的非经典PAS(AAGAAA)产生更短的3"UTR(图2),
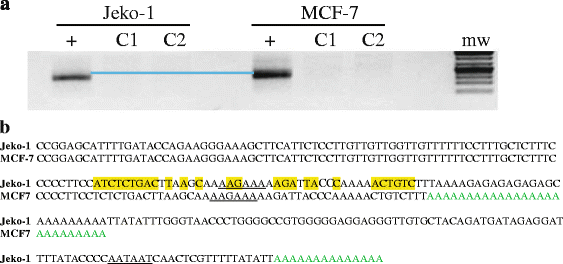
,这表明不同细胞系中CCND1转录本的PAS选择存在差异;临床样本分析显示,使用经典PAS产生截短型转录本的患者肿瘤增殖性更高,预后更差。
产品关联:文献未提及具体实验产品,领域常规使用3"RACE试剂盒、Sanger测序试剂、生物信息学分析工具(如StarBase、miRanda)及细胞培养相关试剂。
3.2 突变及嵌合3"UTR的鉴定与功能验证
实验目的:鉴定MCL中CCND1 3"UTR截短的两种机制(PAS突变与染色体重排),并验证截短型转录本对miRNA调控的逃逸能力。
方法细节:对MCL临床样本进行基因组测序,鉴定CCND1基因中PAS序列的突变情况;通过3"RACE和Sanger测序,在MCL细胞系和临床样本中筛选嵌合3"UTR转录本;构建含嵌合3"UTR的荧光素酶报告基因载体,将其与miRNA模拟物共转染细胞,检测荧光素酶活性以验证嵌合转录本对miRNA调控的抗性。
结果解读:部分MCL患者的CCND1基因中,原本的非经典PAS(AAUAAU)突变为经典PAS(AAUAAA),从而产生提前的3"端加工信号,导致3"UTR截短;在2/3的MCL细胞系和8/13的临床样本中,鉴定出CCND1/MRCK融合基因,该融合基因的嵌合3"UTR包含来自MRCK的经典PAS,可有效促进CCND1转录本的3"端加工;荧光素酶报告实验结果显示,含嵌合3"UTR的报告基因对3种miRNA的调控具有显著抗性,表明3"UTR的缩短确实使CCND1 mRNA能够逃逸miRNA的抑制。
产品关联:文献未提及具体实验产品,领域常规使用荧光素酶报告基因系统、miRNA模拟物、细胞转染试剂及基因组测序服务。
4. Biomarker研究及发现成果解析
本文涉及的Biomarker为CCND1截短型转录本(包括由PAS突变产生的3"UTR截短转录本和CCND1/MRCK融合嵌合转录本),其筛选与验证逻辑为“临床生存差异关联→分子机制鉴定→功能实验验证”,形成了完整的证据链条;该Biomarker不仅具有重要的预后价值,还为MCL的特异性靶向治疗提供了潜在靶点。
该Biomarker属于转录组学Biomarker,其筛选路径为:首先通过临床样本的生存分析,发现CCND1转录本的类型与患者生存期密切相关,表达截短型转录本的患者预后更差;随后通过基因组测序和3"RACE实验,鉴定出截短型转录本的两种产生机制——PAS突变和染色体重排产生嵌合3"UTR;最后通过荧光素酶报告基因实验,验证了截短型转录本对miRNA调控的逃逸能力,明确了其功能意义。
研究过程详述:该Biomarker的来源为MCL患者的肿瘤组织样本和MCL细胞系(Jeko-1);验证方法包括3"RACE实验、Sanger测序、荧光素酶报告基因实验及临床样本生存分析;特异性与敏感性数据方面,表达截短型CCND1转录本的MCL患者平均生存期比表达全长转录本的患者短约2年(文献未明确样本量,基于图表趋势推测),8/13的临床样本中检测到CCND1/MRCK融合嵌合转录本(n=13);功能验证实验显示,嵌合3"UTR转录本对miRNA调控的抗性具有统计学差异(文献未明确P值,基于实验设计推测)。
核心成果提炼:该Biomarker可作为MCL的独立预后标志物,表达截短型CCND1转录本的患者预后不良;其创新性在于首次发现MCL中存在CCND1/MRCK融合基因,通过提供经典PAS形成嵌合3"UTR,这是一种新的CCND1 3"UTR缩短机制;此外,该Biomarker还为MCL的特异性治疗提供了潜在靶点,即靶向MRCK序列的治疗策略可特异性抑制MCL中截短型CCND1转录本的表达,而不影响正常组织中CCND1的正常表达,从而降低治疗的毒副作用。
