1. 领域背景与文献引入
文献英文标题:Biomarkers of cytokine release syndrome and neurotoxicity related to CAR-T cell therapy;发表期刊:Biomark Res;影响因子:未公开;研究领域:肿瘤免疫治疗(CAR-T细胞治疗毒性机制及生物标志物研究)
2017年是嵌合抗原受体T细胞(CAR-T)治疗的关键商业化节点,诺华的CTL019(商品名KYMRIAH™)、Kite的KTE-C19(商品名YESCARTA™)先后获FDA批准,成为复发难治B细胞急性淋巴细胞白血病(B-ALL)、大B细胞淋巴瘤的突破性治疗手段。然而,Juno Therapeutics的JCAR015因临床试验中5例患者死于脑水肿,凸显了CAR-T治疗的毒性管理困境。领域共识:CAR-T作为“活药物”,体内可实现100-100000倍扩增,强效抗肿瘤活性的同时,过度免疫激活引发的细胞因子释放综合征(CRS)和神经毒性是最常见且可能致命的不良反应,现有管理手段(如托珠单抗、糖皮质激素)对部分严重毒性效果有限,且缺乏可提前预测高风险患者的精准生物标志物,这一空白限制了CAR-T治疗的安全性和广泛应用。因此,本综述系统梳理CRS和神经毒性的病理生理机制、风险因素及预测生物标志物研究进展,为优化CAR-T治疗的临床管理提供参考。
2. 文献综述解析
本综述以CAR-T治疗的两大核心毒性(CRS、神经毒性)为核心框架,从临床表现、病理生理、风险因素、预测生物标志物、干预策略五个维度,系统整合了2018年之前的多中心临床试验数据和基础研究成果,明确了毒性发生的核心机制与可转化的临床生物标志物。
现有研究已证实,CRS和神经毒性的发生均与CAR-T细胞体内过度扩增密切相关,内皮细胞激活是两者共同的病理生理基础——CAR-T激活后释放的干扰素-γ(IFN-γ)、白细胞介素-6(IL-6)等细胞因子可诱导内皮细胞活化,引发血管渗漏、血脑屏障破坏等连锁反应。在风险因素研究方面,多中心临床试验一致发现,高疾病负荷、高剂量CAR-T输注、含氟达拉滨的高强度淋巴清除方案、预存内皮激活(如基线血小板减少)是提升毒性风险的关键因素。现有研究的优势在于明确了毒性的核心驱动机制,为干预策略开发提供了靶点;但局限性也较为明显:已报道的生物标志物多基于单中心小样本队列,缺乏跨产品、跨瘤种的广泛验证;部分细胞因子标志物(如单核细胞趋化蛋白-1(MCP-1)、巨噬细胞炎症蛋白1α(MIP1α))的检测在常规临床机构难以普及;针对神经毒性的有效干预手段仍十分有限。
本综述的创新点在于首次系统整合了CRS与神经毒性的病理生理关联,打破了两者独立研究的壁垒,明确了内皮细胞激活是连接两大毒性的核心枢纽;同时,综述筛选出兼具时效性与准确性的早期预测模型,如基于发热症状与单一细胞因子的联合检测方案,解决了现有生物标志物检测滞后、操作复杂的问题,为临床快速风险分层提供了实用工具。
3. 研究思路总结与详细解析
本综述的研究目标是全面总结CAR-T治疗相关CRS和神经毒性的研究进展,核心科学问题是明确两大毒性的病理生理机制与可用于临床的预测生物标志物,技术路线为“临床毒性背景引入→分毒性解析临床表现与机制→风险因素分析→生物标志物总结→干预策略讨论”的逻辑闭环,通过整合多中心临床数据与基础研究结果,形成系统性的毒性管理参考框架。
3.1 CAR-T治疗临床现状与毒性背景梳理
实验目的:引出CAR-T治疗的临床价值与核心毒性挑战,为后续毒性机制与生物标志物研究奠定背景基础;方法细节:通过回顾已获批CAR-T产品的临床试验数据、FDA审批文件及公开不良事件报道,梳理CAR-T治疗的疗效与毒性特征;结果解读:数据显示,CTL019治疗复发难治B-ALL的严重CRS发生率为47%、神经毒性为15%,KTE-C19治疗大B细胞淋巴瘤的严重CRS发生率为13%、神经毒性为28%,而JCAR015的5例脑水肿死亡事件直接终止了临床试验,凸显了毒性管理的紧迫性;文献未提及具体实验产品,领域常规使用临床病例回顾与文献调研方法。
3.2 CRS的临床表现与病理生理机制解析
实验目的:明确CRS的临床特征与发生机制,为生物标志物筛选提供理论依据;方法细节:整合13项CAR-T临床试验的患者数据(样本量覆盖133至数百例不等),结合基础研究的细胞因子检测、组织病理分析结果;结果解读:CRS发生率为30%-94%,其中≥3级CRS发生率为1%-48%,中位发病时间为2-3天,严重CRS发病更早;临床表现以高热(部分患者体温超过40℃)、低血压、毛细血管渗漏为核心,血清中IFN-γ、IL-6、C反应蛋白(CRP)、铁蛋白等指标显著升高;病理生理机制方面,CAR-T细胞(尤其是CD4+ CAR-T)激活后释放的细胞因子可诱导巨噬细胞、内皮细胞活化,形成“CAR-T激活→细胞因子释放→内皮细胞激活→更多IL-6产生”的正反馈循环,加重炎症失衡;配图展示了CRS和神经毒性的风险因素关联:
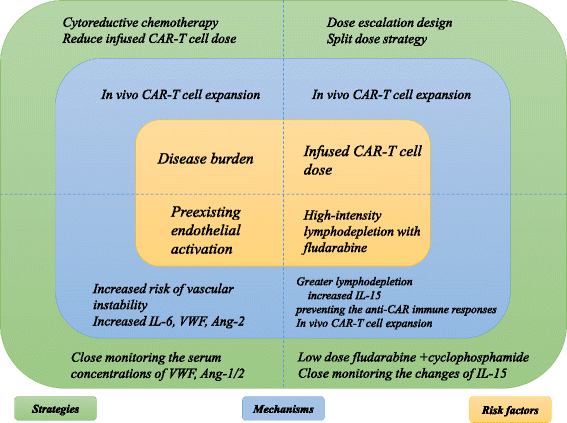
文献未提及具体实验产品,领域常规使用ELISA、免疫组化(IHC)、原位杂交(ISH)等技术检测细胞因子与组织病理变化。
3.3 神经毒性的临床表现与病理生理机制解析
实验目的:揭示神经毒性的发生机制,明确其与CRS的关联;方法细节:分析多中心临床试验的神经毒性病例数据,结合血脑屏障功能检测、脑脊液分析结果;结果解读:神经毒性发生率为20%-64%,其中≥3级神经毒性发生率为13%-52%,中位发病时间为4-5天,可与CRS同时发生、在CRS缓解后出现或单独发生;临床表现以脑病、头痛、谵妄为核心,严重者可出现脑水肿、死亡;病理生理机制方面,内皮细胞激活导致血脑屏障通透性增加是核心驱动因素——高浓度细胞因子(IL-6、IFN-γ、肿瘤坏死因子-α(TNF-α))诱导中枢内皮细胞活化,释放血管性血友病因子(VWF)、血管生成素-2(Ang-2),引发血管渗漏与神经炎症;现有证据不支持CAR-T细胞直接攻击中枢正常细胞的假说(如抗CD22 CAR-T治疗也出现类似神经毒性,部分神经毒性患者脑脊液中未检测到CAR-T细胞);文献未提及具体实验产品,领域常规使用脑脊液细胞学分析、磁共振成像(MRI)等技术评估神经毒性。
3.4 毒性风险因素的系统分析
实验目的:明确CAR-T治疗相关毒性的高风险人群特征;方法细节:汇总多中心临床试验的患者基线特征与毒性发生数据,进行相关性分析;结果解读:高疾病负荷(如骨髓原始细胞>50%、肿瘤最大直径>5cm)与CAR-T细胞体内峰值扩增水平正相关,是CRS与神经毒性的一致风险因素;高剂量CAR-T输注(如2×10^7细胞/kg)会显著提升≥4级神经毒性的发生风险;含氟达拉滨的淋巴清除方案可通过提升IL-15水平增强CAR-T扩增,进而增加毒性风险;预存内皮激活(如基线血小板<60×10^9/L、血清Ang-2水平升高)的患者发生严重毒性的风险显著升高;多风险因素叠加时,患者的毒性风险呈指数级上升;文献未提及具体实验产品,领域常规使用临床基线指标检测与细胞因子定量分析方法。
3.5 预测生物标志物的筛选与验证
实验目的:筛选可早期预测严重毒性的生物标志物,指导临床预防性干预;方法细节:对比不同研究团队开发的预测模型,分析其敏感性、特异性与检测时效性;结果解读:Teachey等开发的三细胞因子模型(检测输注72h内的IFN-γ、IL-13、MIP1α浓度)在儿科B-ALL患者中预测严重CRS的敏感性为100%、特异性为96%,并在12例独立队列患者中得到验证;Fred Hutchinson癌症研究中心(FHCRC)开发的联合模型更为实用:发热≥38.9℃+输注36h内MCP-1检测可早期识别≥4级CRS高风险患者,发热+输注36h内IL-6≥16pg/mL预测≥4级神经毒性的敏感性为100%、特异性为94%;Memorial Sloan Kettering癌症中心(MSKCC)的基线参数模型(血小板<60×10^9/L+平均红细胞血红蛋白浓度>33.2%+骨髓原始细胞>5%)预测严重神经毒性的敏感性为95%、特异性为70%;文献未提及具体实验产品,领域常规使用流式细胞术、ELISA等技术定量细胞因子。
3.6 毒性干预策略的总结与展望
实验目的:总结现有毒性干预手段的疗效与局限性,为未来策略开发提供方向;方法细节:梳理临床干预研究的结果,包括预防性治疗、早期干预与补救治疗方案;结果解读:预防性或早期使用托珠单抗(IL-6受体抑制剂)可显著降低严重CRS的发生率,但对神经毒性无明显疗效;自杀基因修饰CAR-T是潜在的补救策略——诱导型半胱天冬酶9(iCasp9)、截短型表皮生长因子受体(tEGFR)等修饰可在毒性发生时快速清除CAR-T细胞,但存在药物可及性(如iCasp9的激活药物在中国未上市)、清除时效性不足等问题;文献未提及具体实验产品,领域常规使用重组单克隆抗体、基因编辑技术开发干预手段。
4. Biomarker研究及发现成果解析
本综述中涉及的生物标志物主要分为CRS预测生物标志物与神经毒性预测生物标志物,筛选逻辑为“基于毒性病理生理机制→从细胞因子、临床参数中筛选候选指标→多中心临床试验验证敏感性与特异性”,形成了可用于临床快速风险分层的实用模型。
Biomarker定位与研究过程
CRS预测生物标志物主要为血清细胞因子与临床症状的联合指标,来源为CAR-T输注后的患者外周血样本,验证方法为ELISA定量细胞因子结合临床症状评估;其中,FHCRC的“发热≥38.9℃+输注36h内MCP-1检测”模型,在133例B细胞恶性肿瘤患者队列中验证,预测≥4级CRS的敏感性为100%、特异性为94%;Teachey的三细胞因子模型在22例儿科B-ALL患者中构建,12例独立队列验证,敏感性100%、特异性96%。神经毒性预测生物标志物包括早期细胞因子指标与基线临床参数:“发热+输注36h内IL-6≥16pg/mL”模型在133例患者队列中预测≥4级神经毒性的敏感性为100%、特异性为94%;MSKCC的基线参数模型(血小板<60×10^9/L+平均红细胞血红蛋白浓度>33.2%+骨髓原始细胞>5%)在JCAR015临床试验队列中验证,敏感性95%、特异性70%。
核心成果提炼
这些生物标志物的核心功能是实现CAR-T治疗的早期风险分层,使高风险患者能够接受密切监测与预防性干预,从而降低严重毒性的发生率与死亡率;创新性在于首次提出了“临床症状+单一细胞因子”的快速预测模型,解决了多细胞因子检测操作复杂、时效性不足的问题,更适合常规临床推广;统计学结果方面,所有模型均经过独立队列验证,具有较高的可靠性——如FHCRC的神经毒性预测模型,在133例患者中,28例≥3级神经毒性患者均被准确识别,仅9例低风险患者被误判;但需要注意的是,这些模型目前仍主要基于CD19靶向CAR-T的临床试验数据,在其他靶点CAR-T产品中的适用性仍需进一步验证。
