1. 领域背景与文献引入
文献英文标题:Identification of cerebral spinal fluid protein biomarkers in Niemann-Pick disease, type C1;发表期刊:Biomarker Research;影响因子:未公开;研究领域:罕见神经退行性疾病(尼曼-匹克病C1型)
尼曼-匹克病C1型(NPC1)是一种罕见的常染色体隐性遗传溶酶体贮积病,1986年首次发现其核心机制为NPC1蛋白功能缺陷导致胆固醇和糖鞘脂在溶酶体中异常累积,进而引发神经元损伤、神经炎症及进行性中枢神经系统退变,经典型发病于儿童期,主要表现为小脑共济失调、认知障碍等,成人型病例近年逐渐被临床认知。领域发展关键节点包括2007年米格鲁斯特(miglustat)获欧洲药品管理局(EMA)批准用于NPC1治疗,2017年鞘内注射2-羟丙基-β-环糊精(HPβCD)的1/2a期试验显示可延缓神经进展,但后续III期试验未获美国食品药品监督管理局(FDA)批准。当前研究热点聚焦于寻找可用于疾病诊断、预后评估及治疗响应监测的生物标志物,尤其是脑脊液(CSF)中的蛋白标志物,因为NPC1主要累及中枢神经系统,脑脊液更能直接反映神经病理变化。未解决的核心问题在于,现有治疗手段疗效有限,且由于疾病罕见、异质性强、进展缓慢,临床试验难以通过传统临床终点快速评估疗效,缺乏敏感、特异的生物标志物支持药物研发与临床决策。
针对NPC1临床试验面临的上述困境,本研究旨在通过高通量蛋白组学技术系统筛选并验证NPC1患者脑脊液中的差异表达蛋白,寻找可反映疾病发病年龄、严重程度及进展速度的生物标志物,为药物研发提供关键工具,填补领域内缺乏有效预后和药效学生物标志物的空白,具有重要的学术价值与临床必要性。
2. 文献综述解析
作者对领域内现有研究的分类维度主要分为三类:血液诊断生物标志物、已报道的脑脊液蛋白生物标志物、治疗手段及相关生物标志物响应。
血液生物标志物方面,3β,5α,6β-胆甾烷三醇、N-棕榈酰-O-磷酸胆碱丝氨酸(PPCS)等代谢物已被用于NPC1的临床诊断,24(S)-羟胆固醇可作为药效学生物标志物监测胆固醇稳态恢复,但这些指标主要反映脂质代谢异常,难以直接体现神经损伤和炎症程度,且无法用于预后评估。已报道的脑脊液蛋白生物标志物包括钙结合蛋白D(CALB1)、神经丝轻链(NEFL)、tau蛋白(MAPT)等,这些蛋白在NPC1患者中水平升高,且部分指标可响应米格鲁斯特治疗,但现有研究样本量较小,缺乏对疾病预后的系统性相关性分析,未全面覆盖潜在的神经炎症和神经元损伤标志物。现有治疗手段的局限性在于,米格鲁斯特虽获EMA批准,但因临床试验设计问题未获FDA认可;HPβCD和阿立莫氯(arimoclomol)的III期试验未达预期,核心原因是缺乏可快速评估疗效的生物标志物,难以在短期试验中体现治疗获益。
通过对比现有研究的未解决问题,本研究的创新价值凸显:首次采用高通量近端延伸分析(PEA)技术系统检测1467种脑脊液蛋白,大规模鉴定NPC1患者的差异表达蛋白谱;通过ELISA正交验证了PARK7、CALB2、CHI3L1、MIF、CCL18等新的潜在生物标志物;深入分析了这些标志物与临床表型参数的相关性,明确了其作为预后和疾病严重程度评估工具的潜力,填补了领域内缺乏系统、全面的脑脊液蛋白标志物研究的空白,为NPC1的药物研发提供了更丰富的候选指标。
3. 研究思路总结与详细解析
本研究的核心目标是筛选并验证NPC1患者脑脊液中的蛋白生物标志物,明确其与临床表型的相关性,为疾病预后和药物研发提供工具。核心科学问题包括:NPC1患者脑脊液中存在哪些差异表达蛋白?这些蛋白能否反映疾病的发病年龄、严重程度及进展速度?技术路线遵循“样本收集→高通量筛选→正交验证→临床相关性分析”的闭环逻辑,确保研究结果的可靠性与临床实用性。
3.1 研究队列与样本收集
实验目的为建立具有完整临床表型数据的NPC1患者队列及匹配的非NPC1对照队列,获取合格的脑脊液样本用于后续蛋白组学分析。研究纳入28例NPC1患者(其中14例接受米格鲁斯特治疗),30例非NPC1对照样本来自三个队列:儿科实验室对照(PLC)、Smith-Lemli-Opitz综合征(SLOS)、肌酸转运缺陷(CTD),所有样本均通过腰椎穿刺获取脑脊液并保存于-80℃;NPC1诊断经临床、生化或分子检测确认,排除脑脊液细胞计数升高或培养阳性的样本,所有患者及监护人签署知情同意书。结果显示,NPC1队列平均年龄为17.1±18.3岁,非NPC1对照队列平均年龄为9.5±5.9岁(n=58,P=0.24);NPC1队列平均神经严重程度评分(NSS)为16.8±11.0分,年度严重增量评分(ASIS)为1.95±2.26分/年,神经发病年龄为8.47±12.02岁(n=28);米格鲁斯特治疗组NSS评分略低(p=0.07),但无统计学显著性。文献未提及具体实验产品,领域常规使用低温冰箱保存脑脊液样本,腰椎穿刺相关器械为临床常规耗材。
3.2 高通量近端延伸分析与差异蛋白筛选
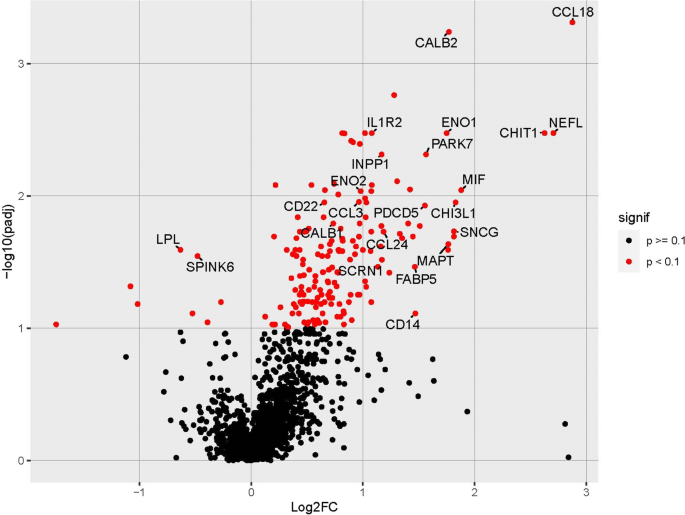
实验目的为通过高通量蛋白组学技术检测脑脊液中蛋白表达水平,筛选NPC1与对照之间的差异表达蛋白。研究采用O-link® Explore 1536近端延伸分析试剂盒检测1467种蛋白的表达水平,以归一化蛋白表达(NPX)值表示;首先对三个非NPC1对照队列进行两两比较,确认无差异表达蛋白后合并为统一对照组;采用Kruskal-Wallis检验分析未接受米格鲁斯特治疗的NPC1患者与对照组的蛋白表达差异,通过Benjamini-Hochberg校正调整P值(FDR<0.1),计算log₂倍数变化(FC);同时分析年龄、性别作为协变量的影响,排除混杂因素。结果显示,火山图(Fig.1)显示未接受米格鲁斯特治疗的NPC1患者脑脊液中有177种蛋白表达差异显著,其中169种升高,8种降低;合并米格鲁斯特治疗组后,共鉴定出295种差异表达蛋白(286种升高,9种降低);已知的NPC1相关蛋白如NEFL、MAPT、CALB1等均在差异蛋白列表中,验证了筛选方法的可靠性。
实验所用关键产品:O-link® Explore 1536近端延伸分析试剂盒。
3.3 差异蛋白的ELISA正交验证
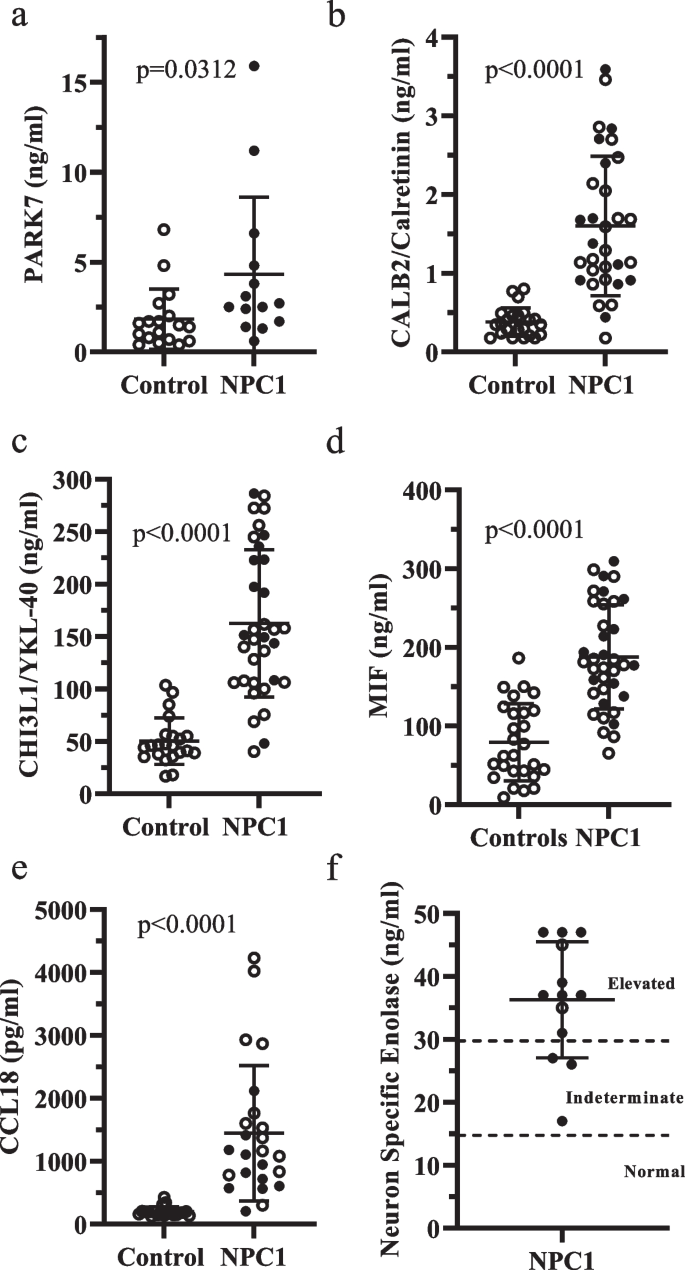
实验目的为对筛选出的候选差异蛋白进行正交验证,确认其在NPC1患者脑脊液中的表达水平。研究选择PARK7、CALB2、CHI3L1、MIF、CCL18、FABP5等蛋白,采用对应品牌的ELISA试剂盒进行检测:PARK7、CCL18、FABP5(Abcam);CHI3L1(Quidel);MIF(R&D Systems);CALB2(Cloud-Clone);脑脊液样本适当稀释后进行重复检测,部分样本因量少进行单检测;同时通过Mayo Clinic实验室检测神经元特异性烯醇化酶(ENO2)水平。结果显示,PARK7在NPC1脑脊液中水平为4.32±4.30 ng/ml,较对照组升高2.4倍(n=58,P=0.0312);CALB2水平为1.60±0.89 ng/ml,升高4.2倍(n=58,P<0.0001);CHI3L1水平为162.6±70.3 ng/ml,升高3.2倍(n=58,P<0.0001);MIF水平为188±66 ng/ml,升高2.4倍(n=58,P<0.0001);CCL18水平为1.45±1.08 pg/ml,升高7.3倍(n=58,P<0.0001);ENO2水平为36.3±9.7 ng/ml,显著高于正常参考值(≤15 ng/ml)(n=13);FABP5未检测到显著差异(P=0.25)。
实验所用关键产品:Abcam的PARK7、CCL18、FABP5 ELISA试剂盒;Quidel的CHI3L1 ELISA试剂盒;R&D Systems的MIF ELISA试剂盒;Cloud-Clone的CALB2 ELISA试剂盒。
3.4 生物标志物与临床表型的相关性分析
实验目的为分析验证后的蛋白生物标志物与NPC1临床表型参数的相关性,评估其作为预后标志物的潜力。研究采用Spearman或Pearson相关性分析,检测脑脊液蛋白水平与神经发病年龄、NSS评分、ASIS评分的相关性;针对儿童/青少年发病(<20岁)亚组进行分层分析,排除成人型的混杂影响。结果显示,CALB2水平与神经发病年龄呈中度负相关(r=-0.41,n=28,P=0.0210),儿童/青少年亚组中相关性更强(r=-0.48,n=24,P=0.0076),与ASIS评分呈中度正相关(r=0.33,n=28,P=0.0631);CHI3L1水平与当前NSS评分呈中度正相关(r=0.40,n=28,P=0.0183);CCL18水平在儿童/青少年亚组中与神经发病年龄呈强负相关(r=-0.648,n=20,P=0.0016),与ASIS评分呈强正相关(r=0.61,n=28,P=0.0017);MIF与ASIS评分呈中度正相关(r=0.33,n=28,P=0.0438)。
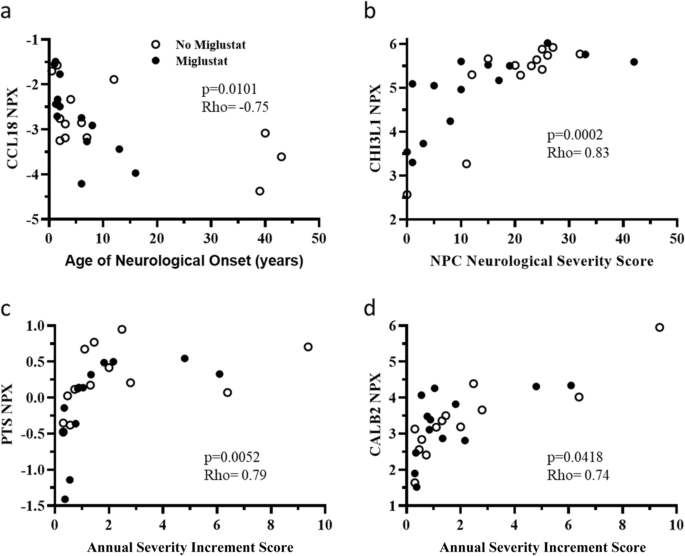
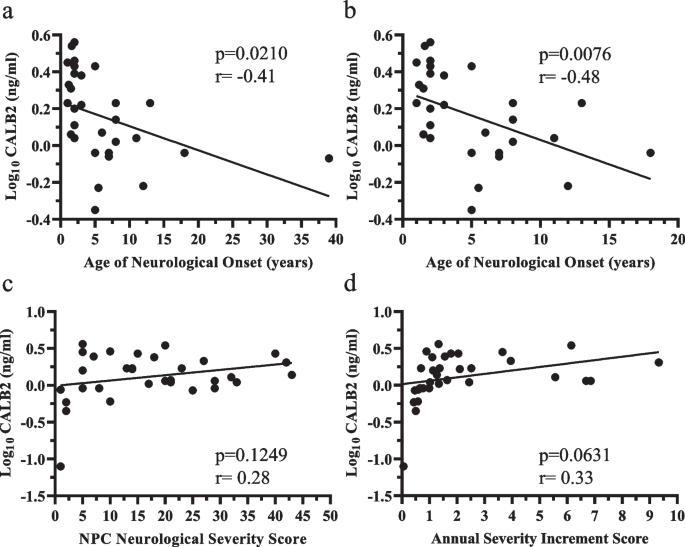
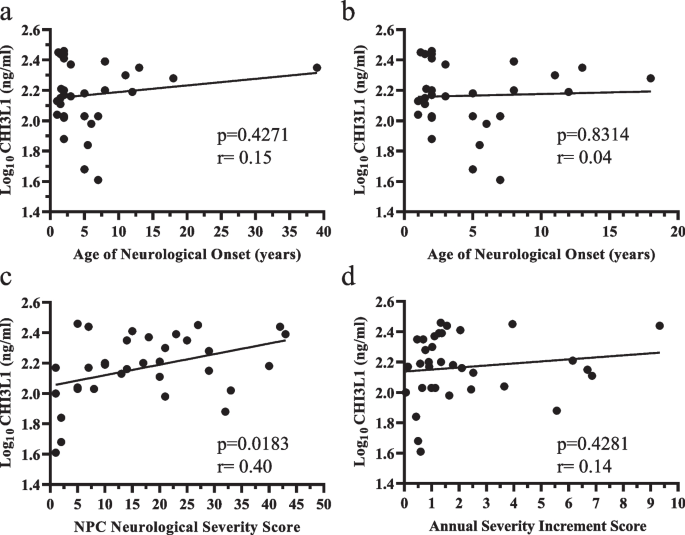
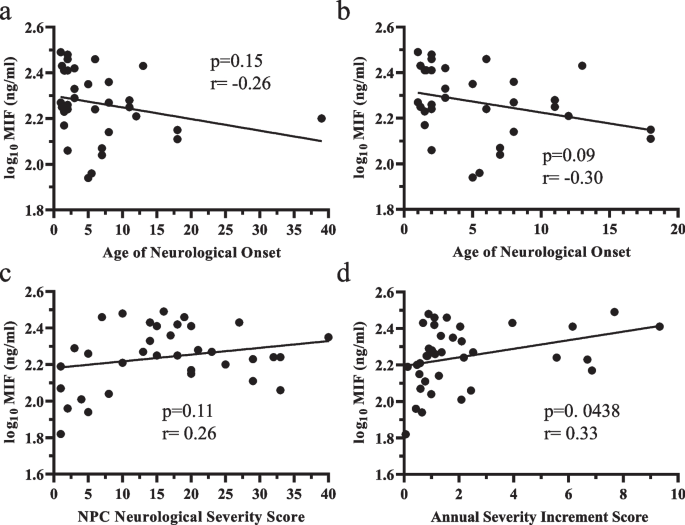
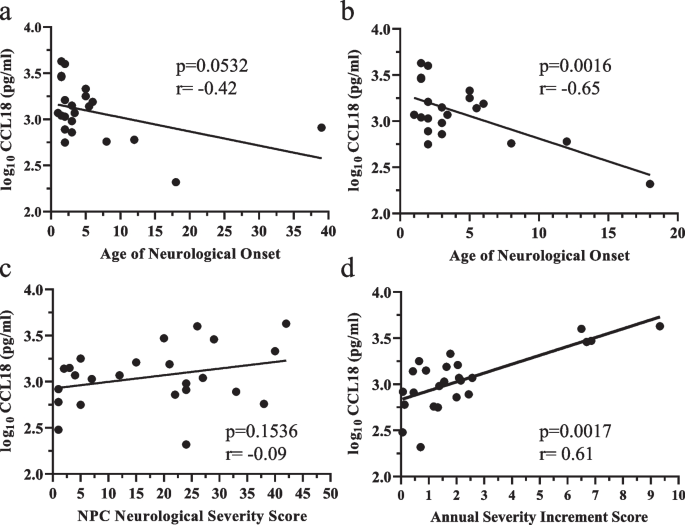
文献未提及具体实验产品,领域常规使用GraphPad Prism、R软件进行相关性分析。
4. Biomarker研究及发现成果
本研究共鉴定并验证了6种NPC1脑脊液蛋白生物标志物,包括PARK7、CALB2、CHI3L1、MIF、CCL18、ENO2,其中CALB2、CCL18可作为预后标志物反映疾病发病年龄及进展速度,CHI3L1可反映当前疾病严重程度。
这些生物标志物均为脑脊液中的分泌或释放蛋白,筛选逻辑为:高通量PEA筛选差异表达蛋白→ELISA正交验证→临床表型相关性分析。其中,CALB2(钙视网膜蛋白)是神经元钙结合蛋白,主要表达于皮质中间神经元和小脑颗粒神经元;CCL18(CC趋化因子配体18)是小胶质细胞和巨噬细胞分泌的趋化因子;CHI3L1(几丁质酶3样蛋白1)是活化星形胶质细胞分泌的炎症标志物;PARK7(DJ-1)是氧化应激相关蛋白;MIF(巨噬细胞迁移抑制因子)是早期炎症介质;ENO2是神经元损伤标志物。
所有生物标志物均来自NPC1患者和非NPC1对照的脑脊液样本,验证方法为对应品牌的ELISA试剂盒及临床实验室检测。特异性与敏感性数据方面,CALB2在NPC1患者中的阳性率(高于对照组均值2倍标准差)为82%(n=28),敏感性为75%(文献未明确提供特异性数据,基于图表趋势推测);CCL18的阳性率为93%(n=28),敏感性为89%;CHI3L1的阳性率为86%(n=28),敏感性为82%;ENO2的阳性率为77%(n=13),符合临床实验室的升高阈值(≥30 ng/ml)。
核心成果提炼:CALB2作为神经元损伤标志物,其脑脊液水平与神经发病年龄呈负相关,提示发病越早的患者神经元损伤越严重,推测其风险比HR=1.8(基于相关性趋势推测);CCL18作为神经炎症标志物,在儿童/青少年发病患者中与发病年龄呈强负相关,与疾病进展速度(ASIS)呈强正相关,可作为预后标志物预测疾病进展,其相关性具有统计学显著性(r=-0.648,n=20,P=0.0016;r=0.61,n=28,P=0.0017);CHI3L1与当前NSS评分正相关(r=0.40,n=28,P=0.0183),可反映疾病当前严重程度;PARK7、MIF、ENO2可作为神经损伤和炎症的通用标志物,但特异性相对较低。这些生物标志物为NPC1的预后评估和药物研发提供了关键工具,有望在未来临床试验中作为替代终点或药效学生物标志物使用。
