1. 领域背景与文献引入
文献英文标题:Dysregulation of transposable elements and PIWI-interacting RNAs in myelodysplastic neoplasms;发表期刊:Biomark Res;影响因子:未公开;研究领域:骨髓增生异常综合征(MDS)表观遗传调控与预后生物标志物研究
骨髓增生异常综合征是一类起源于造血干细胞的异质性血液系统疾病,核心特征为骨髓发育异常、无效造血及向急性髓系白血病(AML)转化的高风险。领域共识:MDS的发病与造血干细胞基因组不稳定性密切相关,初始突变引发的基因组不稳定会驱动克隆演化与疾病进展。当前领域研究热点集中在体细胞突变谱、表观遗传调控机制及预后生物标志物的筛选,但转座子(TEs)与PIWI互作RNA(piRNAs)构成的调控轴在MDS进展中的作用尚未明确。现有研究多聚焦于急性髓系白血病中转座子的调控,针对MDS的piRNA研究较为有限,仅少数研究报道了血浆piRNA的失调或难治性贫血亚型中的piRNA富集,缺乏对造血干细胞中转座子与piRNA协同调控的系统分析,也未明确可用于临床预后分层的相关分子标志物。
基于上述研究空白,本研究旨在通过平行RNA测序与小RNA测序技术,分析MDS患者CD34+造血干细胞中转座子与piRNA的表达谱,明确其在高低危MDS中的表达差异及与患者预后的关联,填补MDS表观遗传调控机制与预后标志物研究的关键缺口。
2. 文献综述解析
本文综述部分围绕转座子、piRNA及PIWI蛋白在血液系统肿瘤中的作用展开,通过对比不同疾病阶段与分子类型的研究,系统梳理了现有研究的进展与局限。
作者对领域内现有研究的分类维度主要为疾病风险分层(低危MDS vs 高危MDS)和分子调控类型(转座子、piRNA、PIWI蛋白)。现有研究的关键结论包括:转座子在多数癌症中处于激活状态,通过引发基因组不稳定促进肿瘤进展,但Colombo等的研究发现高危MDS中转座子表达被抑制,推测其可能参与免疫逃逸;piRNA最初被发现于生殖系中抑制转座子的活性,近年来其在体细胞及癌症中的调控作用逐渐被关注,但针对MDS的piRNA研究较为有限,仅少数研究报道了血浆piRNA的失调或难治性贫血亚型中的piRNA富集。现有研究的技术方法优势在于多采用下一代测序技术实现分子表达谱的高通量分析,但存在明显局限性:多数研究未聚焦CD34+造血干细胞这一MDS的起源细胞,样本量较小且未系统分析转座子与piRNA轴的协同调控关系,也未明确该调控轴与患者预后的直接关联。
通过对比现有研究的未解决问题,本研究的创新价值凸显:首次在CD34+造血干细胞中平行分析转座子与piRNA的表达谱,揭示了高危MDS中转座子下调与piRNA上调的负相关调控关系,同时发现PIWIL2作为独立预后标志物,完善了MDS进展的表观遗传调控机制,为MDS的预后分层提供了新的分子靶点。
3. 研究思路总结与详细解析
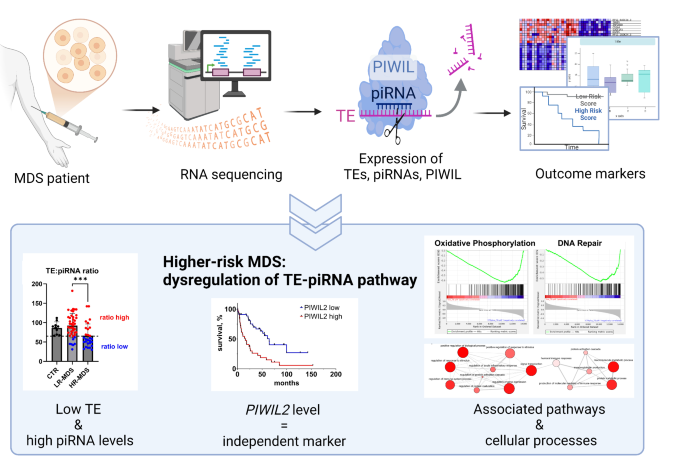
本研究以“明确转座子-piRNA轴在MDS进展中的调控作用及预后价值”为核心目标,围绕“高低危MDS中转座子与piRNA的表达差异→关键调控分子的预后关联→下游通路功能变化”的逻辑链条展开,通过队列样本分析、测序技术、分子验证及生物信息学分析的闭环实验设计,系统解析了转座子与piRNA在MDS中的作用机制。
3.1 患者队列构建与样本制备
实验目的是建立包含完整临床信息的MDS患者队列,分离疾病起源细胞CD34+造血干细胞,为后续分子表达分析提供标准化样本。方法细节:纳入80例MDS患者(根据修订版国际预后评分系统IPSS-R分为低危组LR-MDS和高危组HR-MDS)及17例健康对照,收集骨髓样本后,采用Ficoll-Hipaque密度梯度离心分离单个核细胞,通过磁珠分选技术富集CD34+细胞,利用酚-氯仿法提取总RNA,并用Qubit 3荧光计和Agilent 4200 TapeStation验证RNA质量。结果解读:队列包含患者的IPSS-R评分、基因突变、细胞遗传学特征及随访信息,为后续分子表达与临床参数的关联分析提供了基础;CD34+细胞的成功富集确保了研究聚焦于MDS的起源细胞,排除了其他骨髓细胞的干扰。
实验所用关键产品:GE Healthcare的Ficoll-Hipaque密度梯度离心试剂、Miltenyi Biotec的磁珠分选试剂盒、Thermo Fisher Scientific的Qubit 3荧光计、Agilent Technologies的4200 TapeStation仪器。
3.2 转座子与piRNA表达谱测序分析
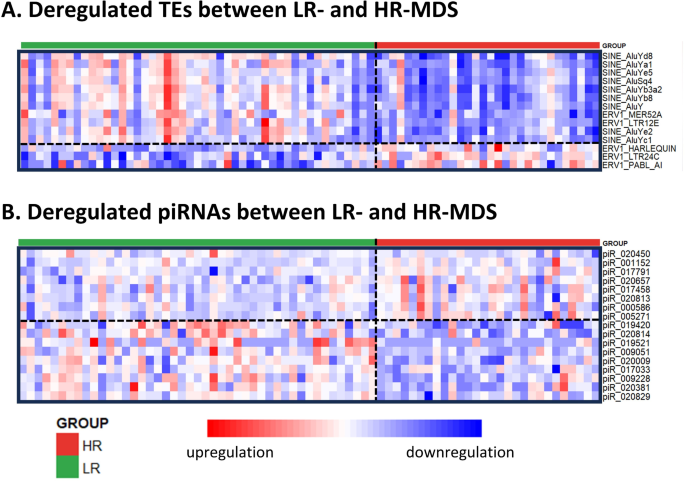
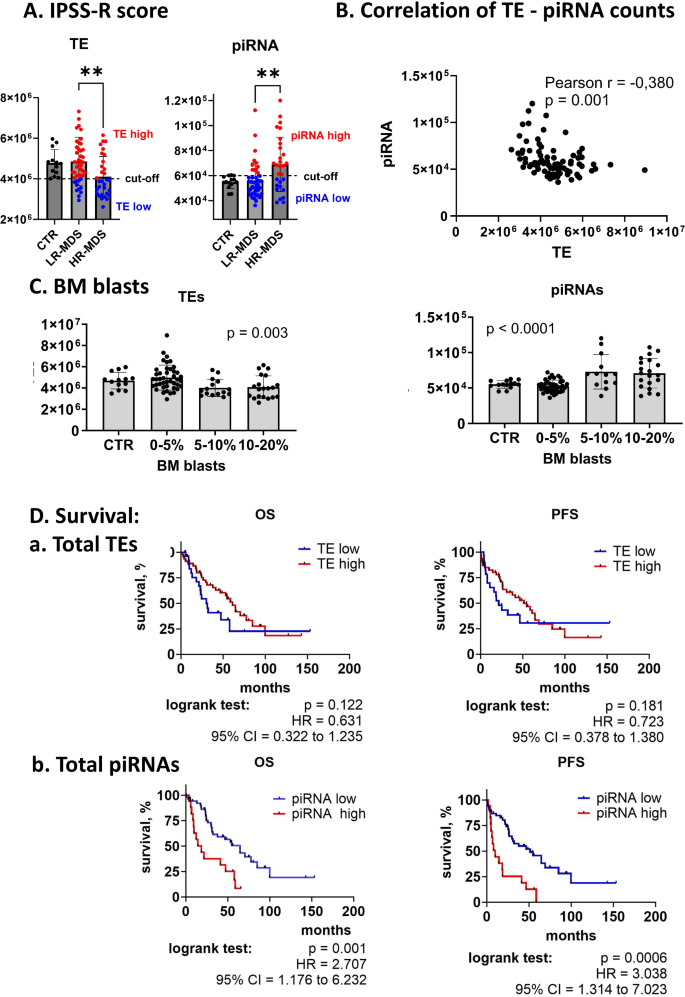
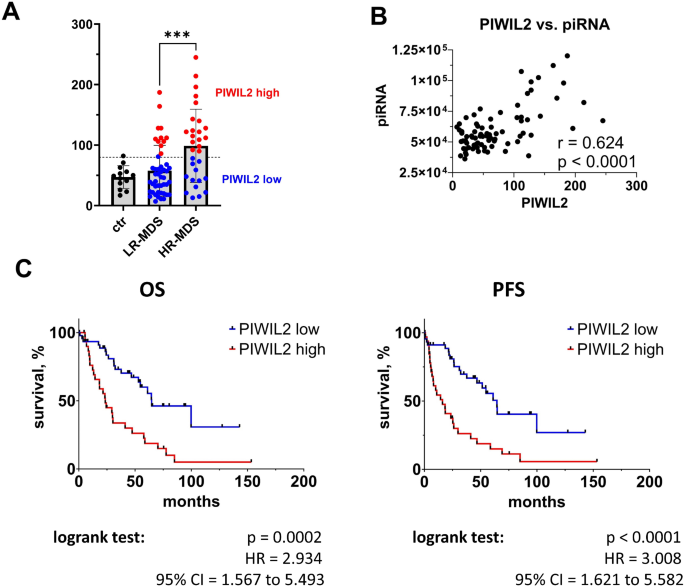
实验目的是全面解析CD34+细胞中转座子与piRNA的表达谱,筛选高低危MDS中的差异表达分子。方法细节:针对总RNA,采用RiboCop rRNA去除试剂盒去除核糖体RNA,通过NEBNext Ultra II Directional RNA文库制备试剂盒构建RNA-seq文库,在NovaSeq 6000平台进行双端测序;针对小RNA,采用QIAseq miRNA文库试剂盒构建小RNA-seq文库,进行单端测序。生物信息学分析方面,用SalmonTE工具识别并计数转座子,DESeq2进行差异表达分析;小RNA数据比对至piRNABank数据库,去重后进行差异分析。结果解读:MDS患者与对照样本中转座子和piRNA的整体表达谱相似,仅少数分子差异;但LR-MDS与HR-MDS间存在显著差异,共鉴定出106个差异表达转座子(48个上调、58个下调)和17个差异表达piRNA(7个上调、10个下调);进一步分析显示HR-MDS患者的总转座子表达水平显著低于LR-MDS及对照(p=0.005),总piRNA水平显著升高(p=0.003),二者呈中度负相关(Pearson r=-0.380,p=0.001),验证了转座子与piRNA的经典调控关系。
实验所用关键产品:Lexogen的RiboCop rRNA去除试剂盒、New England Biolabs的NEBNext Ultra II Directional RNA文库制备试剂盒、Illumina的NovaSeq 6000测序平台、Qiagen的QIAseq miRNA文库试剂盒。
3.3 关键分子的预后关联与独立验证
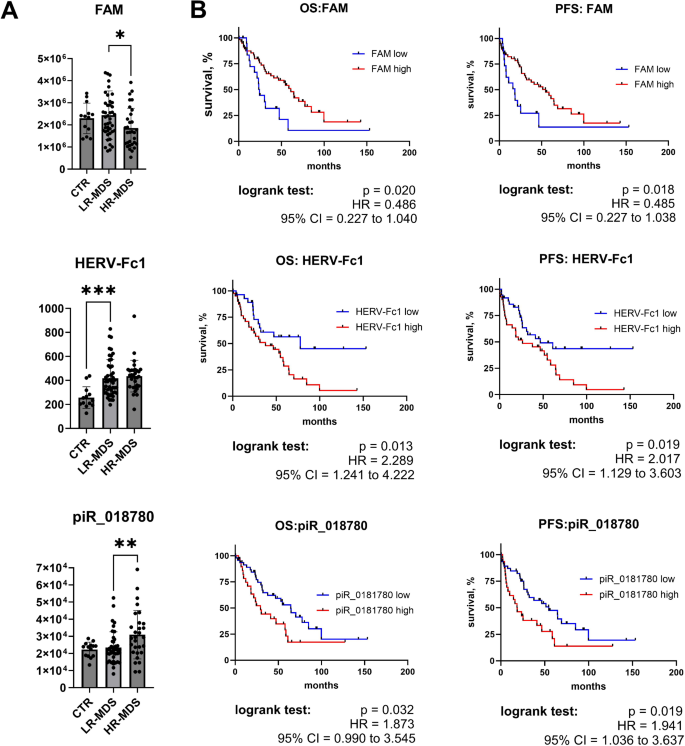
实验目的是筛选具有预后价值的分子标志物,并在独立队列中验证其可靠性。方法细节:首先通过Kaplan-Meier生存分析评估总转座子、总piRNA及单个分子(FAM、HERV-Fc1、piR_018780、PIWIL2)与患者总生存期(OS)和无进展生存期(PFS)的关联;采用实时定量PCR(RT-qPCR)在15例MDS患者和5例对照样本中验证FAM和piR_018780的表达;通过液滴数字PCR(ddPCR)在包含72例MDS患者的独立队列中验证PIWIL2的表达;最后采用Cox多因素回归分析验证PIWIL2的独立预后价值。结果解读:总piRNA水平升高与不良预后显著相关(OS的HR=2.707,p=0.001;PFS的HR=3.038,p=0.0006);单个分子中,piR_018780上调、FAM下调与不良预后相关,HERV-Fc1下调与良好预后相关;RT-qPCR结果与测序结果高度相关(FAM:Pearson r=0.782,p=0.0001;piR_018780:Pearson r=0.702,p=0.002),验证了测序数据的准确性;PIWIL2在HR-MDS中的表达较LR-MDS升高2倍(p<0.001),与总piRNA水平正相关(Pearson r=0.624,p<0.001),高PIWIL2表达患者的中位OS为23.5个月,低表达为64.7个月(HR=2.934,p=0.0002);独立队列验证显示高PIWIL2表达仍与不良预后相关(OS的HR=3.379,p<0.0001);多因素回归分析显示PIWIL2是MDS患者OS和PFS的独立预后因子(OS的HR=3.197,p=0.0008;PFS的HR=3.637,p=0.0004),其预后价值优于部分临床参数如原始细胞计数。
实验所用关键产品:Thermo Fisher Scientific的TaqMan MicroRNA反转录试剂盒、SuperScript VILO cDNA合成试剂盒、TaqMan通用预混液、StepOnePlus实时PCR仪;Bio-Rad的ddPCR Supermix for Probes、QX200 ddPCR系统。
3.4 失调通路的功能富集分析
实验目的是解析转座子-piRNA轴失调对MDS细胞功能的影响,明确下游调控通路。方法细节:基于转座子与piRNA的比值将患者分为低比值组(低转座子、高piRNA)和高比值组,通过差异表达分析筛选两组间的蛋白编码基因,采用基因集富集分析(GSEA)和GO富集分析探索失调的生物学通路;同时构建PIWIL2等关键分子的共表达网络,分析其功能关联。结果解读:低比值组样本中,氧化磷酸化、糖酵解、细胞周期、DNA修复、免疫应答等通路被显著抑制,提示高危MDS细胞的代谢活性、增殖能力及免疫功能均出现异常;PIWIL2的共表达网络主要与细胞分裂、染色体分离、核小体组装等过程相关,其网络中的基因(如HIST1H3B、CCNA2)与低比值组中的下调基因重叠,进一步验证了PIWIL2在MDS进展中的调控作用。
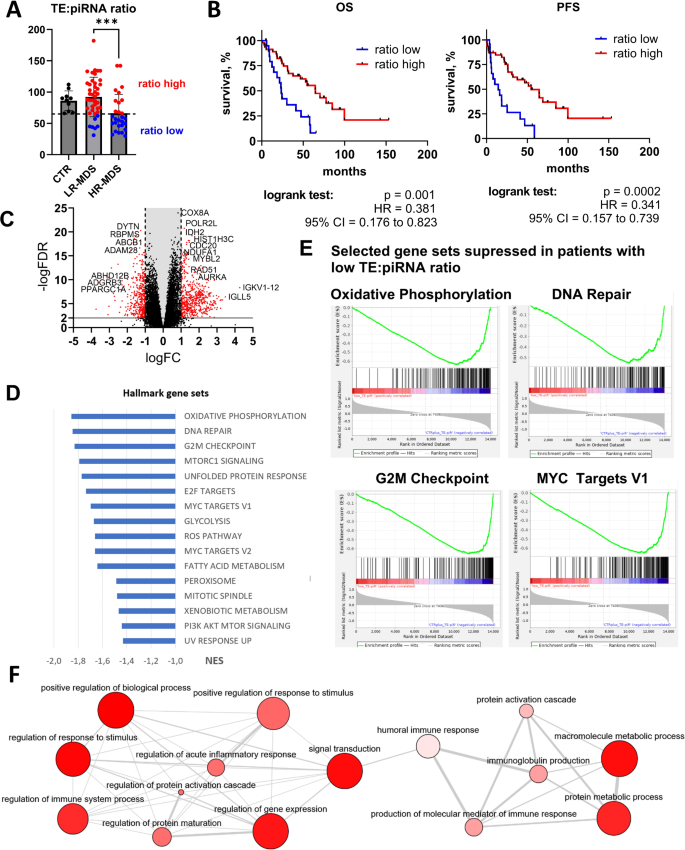
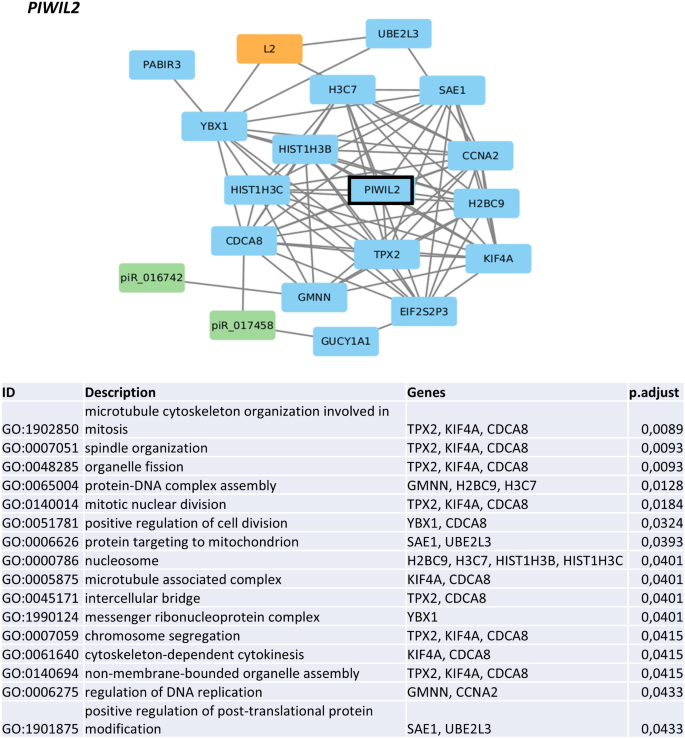
文献未提及具体实验产品,领域常规使用clusterProfiler、Cytoscape、GOrilla等生物信息学工具。
4. Biomarker研究及发现成果解析
本研究聚焦于转座子-piRNA轴中的关键调控分子,成功筛选并验证了PIWIL2作为MDS的独立预后生物标志物,同时明确了转座子与piRNA的表达水平及比值与患者预后的关联。
Biomarker定位:PIWIL2属于PIWI家族蛋白,是piRNA通路的核心调控因子,其筛选与验证逻辑为:通过RNA-seq发现HR-MDS中PIWIL2表达显著上调→分析其与piRNA水平的相关性,确认其在piRNA通路中的核心作用→生存分析显示其与患者预后的关联→独立队列中通过ddPCR验证表达水平与预后的关系→多因素回归分析确认其独立预后价值。此外,总piRNA水平、转座子-piRNA比值也可作为预后参考指标,但PIWIL2因是蛋白编码基因,更适合临床检测应用。
研究过程详述:PIWIL2的来源为MDS患者CD34+骨髓造血干细胞,验证方法包括RNA-seq、实时定量PCR及液滴数字PCR;特异性方面,PIWIL2在HR-MDS中的表达水平较LR-MDS升高2倍(p<0.001),与总piRNA水平呈强正相关(Pearson r=0.624,p<0.001);敏感性方面,在训练队列中,高PIWIL2表达患者的中位OS为23.5个月,低表达患者为64.7个月(HR=2.934,95%CI=1.567-5.493,p=0.0002);独立队列中,高表达患者的中位OS为12.2个月,低表达为50.9个月(HR=3.379,95%CI=1.364-8.372,p<0.0001),显示出良好的预后预测能力。
核心成果提炼:PIWIL2是MDS的独立预后生物标志物,其高表达提示患者预后不良,风险比HR=3.197(OS,95%CI=1.618-6.314,p=0.0008),HR=3.637(PFS,95%CI=1.771-7.470,p=0.0004);创新性在于首次发现PIWIL2在HR-MDS中的上调表达,明确其作为转座子-piRNA轴的关键调控因子,可用于MDS的预后分层,为MDS的表观遗传靶向治疗提供了潜在靶点;同时,本研究揭示的转座子下调与piRNA上调的协同失调,进一步完善了MDS进展的表观遗传调控机制。
