1. 领域背景与文献引入
文献英文标题:X-chromosome-linked miR-542-5p as a key regulator of sex disparity in rats with adjuvant-induced arthritis by promoting Th17 differentiation;发表期刊:Biomark Res;影响因子:未公开;研究领域:类风湿关节炎(自身免疫病)性别差异机制研究
类风湿关节炎(RA)是一种以关节肿胀、畸形、功能障碍为核心特征的多系统炎症性自身免疫病,全球患病率为0.5%-1%,男女患病比例约为1:3,女性患者病情通常更为严重且治疗应答差异显著。领域共识:现有研究已证实性激素波动、X染色体相关基因表达差异参与RA性别差异调控,但青春期前女性RA发病率仍高于男性,提示性激素并非唯一调控因素;X染色体上富集大量免疫相关基因,约15-23%的基因可逃避X染色体失活(XCI),导致性别间基因表达失衡,而X连锁microRNA(miRNA)作为免疫应答的重要调控因子,其在RA性别差异中的具体作用尚未明确。目前仅少数X连锁miRNA如miR-221、miR-222被报道与RA相关,针对miR-542-5p的研究处于空白状态,本研究旨在系统解析miR-542-5p在RA性别差异中的调控作用及分子机制,为RA性别特异性诊疗提供新靶点。
2. 文献综述解析
作者以“RA性别差异的调控层次”为核心分类维度,从性激素与X染色体的基础调控、X连锁miRNA的免疫功能、Th17细胞的病理作用三个层面梳理领域研究进展。现有研究显示,性激素可通过调节免疫细胞活性影响RA病情,但无法解释青春期前女性的高发病率;X染色体上逃避XCI的基因如CD40L、IRAK-1等可增强炎症应答,导致女性免疫反应强度高于男性;X连锁miRNA数量约为Y染色体的58倍,部分miRNA已被证实参与RA滑膜细胞增殖、炎症因子分泌等过程,但缺乏对miR-542-5p的靶向研究;Th17细胞作为RA的关键效应细胞,其分化失衡与病情严重程度正相关,但性别差异的调控通路尚未明确。现有研究的局限性在于未建立X连锁miRNA与Th17分化、RA性别差异的关联机制,本研究首次聚焦miR-542-5p,通过体内外实验证实其通过靶向抑制FOXO1、TEAD1促进Th17分化,进而调控RA性别差异,填补了该领域的研究空白。
3. 研究思路总结与详细解析
本研究以“明确miR-542-5p在RA性别差异中的调控作用及分子机制”为核心目标,围绕“miR-542-5p是否参与RA性别差异调控→其对RA病情的影响→通过何种通路调控性别差异”三个科学问题,构建“临床样本筛选→动物模型功能验证→细胞实验机制探究”的闭环技术路线,系统解析miR-542-5p的调控作用。
3.1 临床样本miR-542-5p表达差异检测
本环节核心目标是明确RA患者与健康人群、RA不同性别间miR-542-5p的表达差异。研究收集47例RA患者和61例健康人外周血样本,分离外周血单个核细胞(PBMCs),采用mirVana™ miRNA分离试剂盒提取总RNA,通过NanoDrop 2000c分光光度计验证RNA质量后,使用miDETECTA Track™ miRNA qRT-PCR试剂盒在BioRad IQ5系统上检测miR-542-5p表达水平,以Rnu6为内参,采用2^(-ΔΔCt)法计算相对表达量。结果显示,RA患者miR-542-5p表达水平显著高于健康人(n=108,P<0.01);RA女性患者miR-542-5p表达显著高于男性患者(n=47,P<0.05),而健康人群中无明显性别差异。
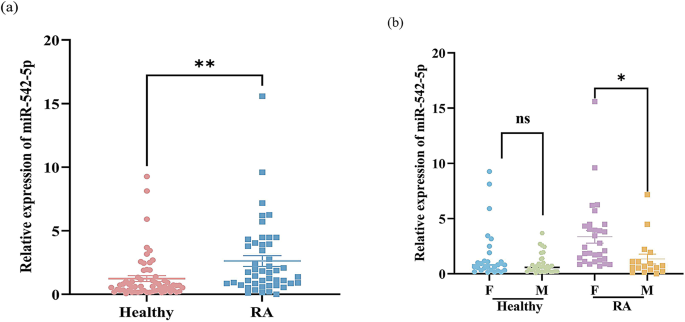
实验所用关键产品:mirVana™ miRNA Isolation Kit(Thermo Fisher)、miDETECTA Track™ miRNA qRT-PCR Starter kit(RiboBio)、NanoDrop 2000c Spectrophotometer(Thermo Fisher)、BioRad IQ5系统。
3.2 AIA大鼠模型miR-542-5p过表达功能验证
本环节核心目标是验证miR-542-5p过表达对RA病情的促进作用。研究构建SD大鼠佐剂诱导关节炎(AIA)模型,将大鼠分为健康对照组、AIA阴性对照组、AIA+甲氨蝶呤(MTX)组、AIA+miR-542-5p agomir组,每组5只;于建模第0天和第10天尾静脉注射agomir(20nmol/只),每3天记录大鼠后爪体积和关节炎评分,第27天处死大鼠取样本检测。结果显示,agomir组大鼠后爪体积、关节炎评分显著高于AIA阴性对照组(n=5,P<0.001);micro-CT扫描显示骨破坏程度更严重,H&E染色可见滑膜细胞增生、骨侵蚀等典型关节炎特征更显著;血清促炎因子TNF-α、IL-1β、IL-6等水平显著升高,抗炎因子IL-4水平显著降低(n=5,P<0.001)。
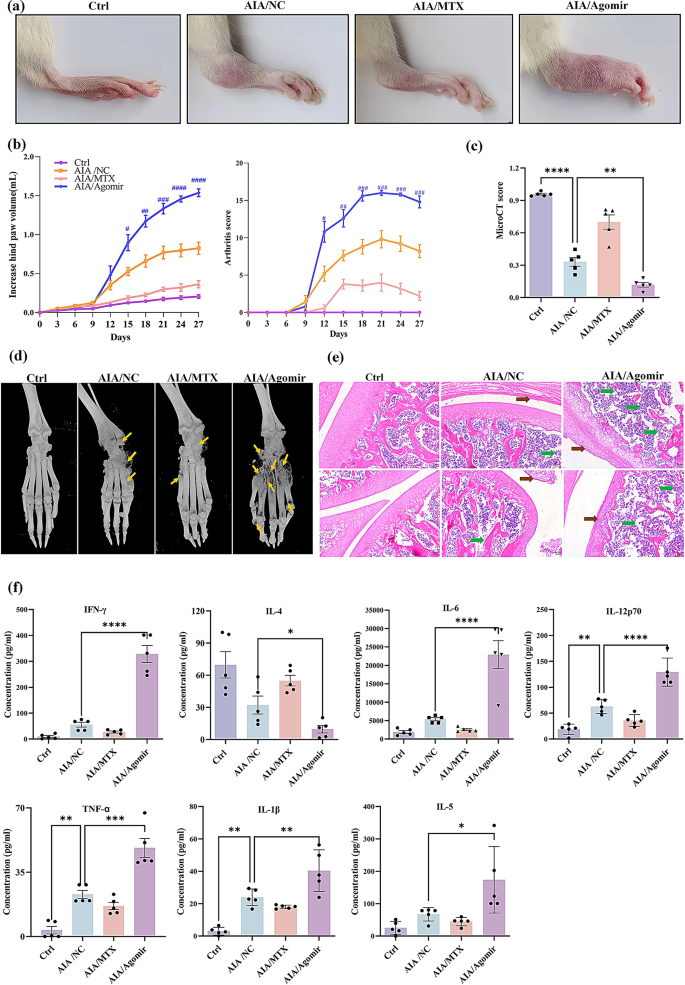
实验所用关键产品:完全弗氏佐剂(CFA)H37Ra、miR-542-5p agomir(RiboBio)、SkyScan 1176 micro-CT扫描仪(Bruker)、Leica DM2500光学显微镜、LEGENDplex™ Rat Inflammatory Panel(Biolegend)。
3.3 AIA大鼠性别差异表型与免疫应答分析
本环节核心目标是明确AIA大鼠的性别差异特征及与miR-542-5p的关联。研究将SD大鼠按性别分为健康对照组、AIA组,每组5只;检测大鼠后爪体积、关节炎评分、micro-CT评分,通过流式细胞术分析T细胞亚群比例,ELISA检测血清细胞因子水平,qRT-PCR检测miR-542-5p表达。结果显示,雌性AIA大鼠后爪体积、关节炎评分、micro-CT评分显著高于雄性AIA大鼠(n=5,P<0.01);H&E染色显示雌性大鼠滑膜增生、中性粒细胞浸润、骨破坏等病理特征更显著;流式细胞术分析发现雌性AIA大鼠Th17细胞比例显著高于雄性(n=5,P<0.01),血清IL-17A、IL-6浓度显著升高(n=5,P<0.0001);雌性AIA大鼠miR-542-5p表达水平显著高于雄性(n=5,P<0.01)。
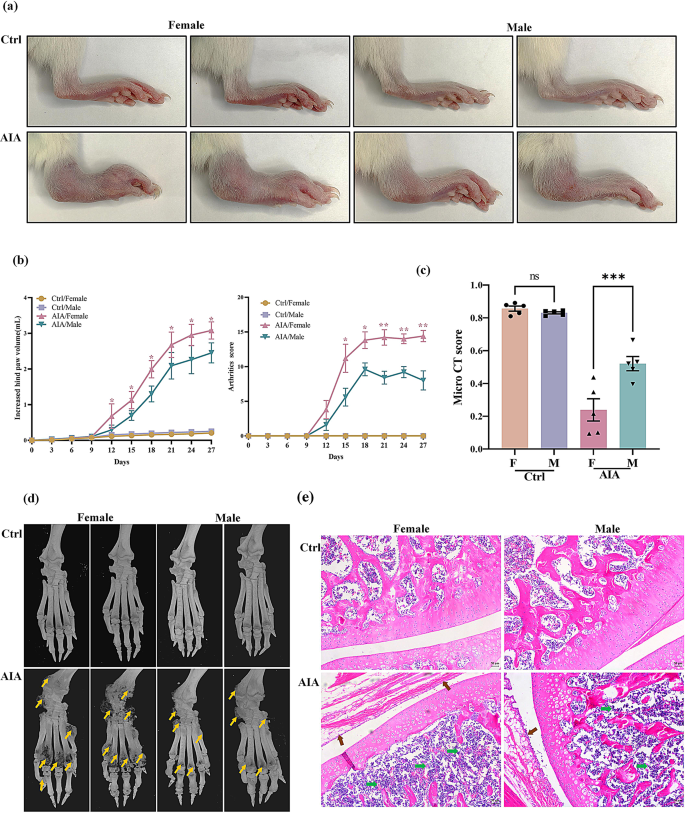
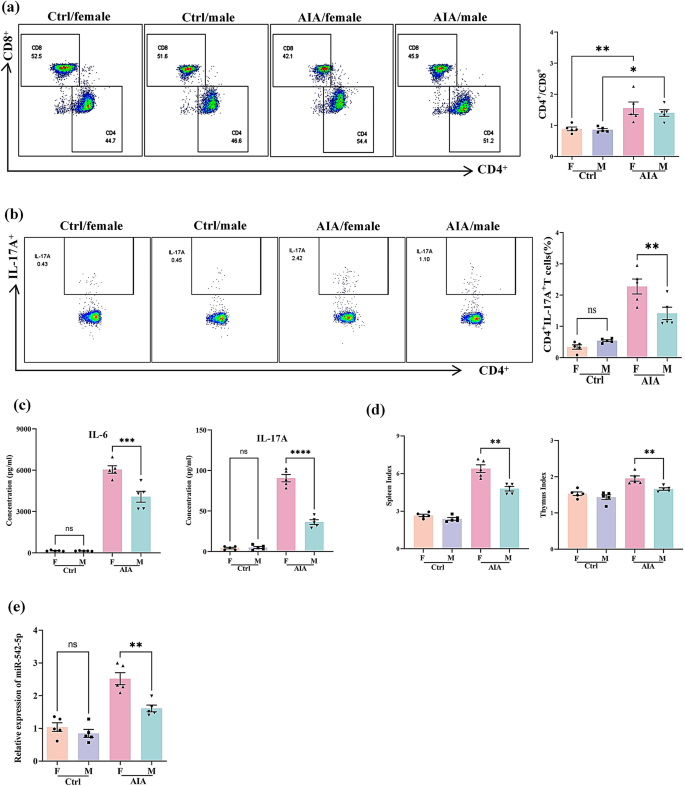
实验所用关键产品:抗大鼠CD45 APC/Cy7、CD3 FITC等流式抗体(BioLegend)、BD FACSAria III细胞分选仪、Naive CD4+T Cell Isolation Kit(Miltenyi Biotech)。
3.4 miR-542-5p对AIA大鼠性别差异的调控验证
本环节核心目标是明确miR-542-5p调控RA性别差异的功能。研究将雌性AIA大鼠分为阴性对照组、miR-542-5p antagomir组,尾静脉注射antagomir(100nmol/只);雄性AIA大鼠分为阴性对照组、miR-542-5p agomir组,尾静脉注射agomir(20nmol/只);检测大鼠病情指标、Th17细胞比例、细胞因子水平。结果显示,雌性antagomir组大鼠后爪体积、关节炎评分显著降低(n=5,P<0.0001),Th17细胞比例、血清IL-17A浓度显著下降(n=5,P<0.001);雄性agomir组大鼠病情加重,Th17细胞比例、促炎因子水平显著升高(n=5,P<0.0001)。
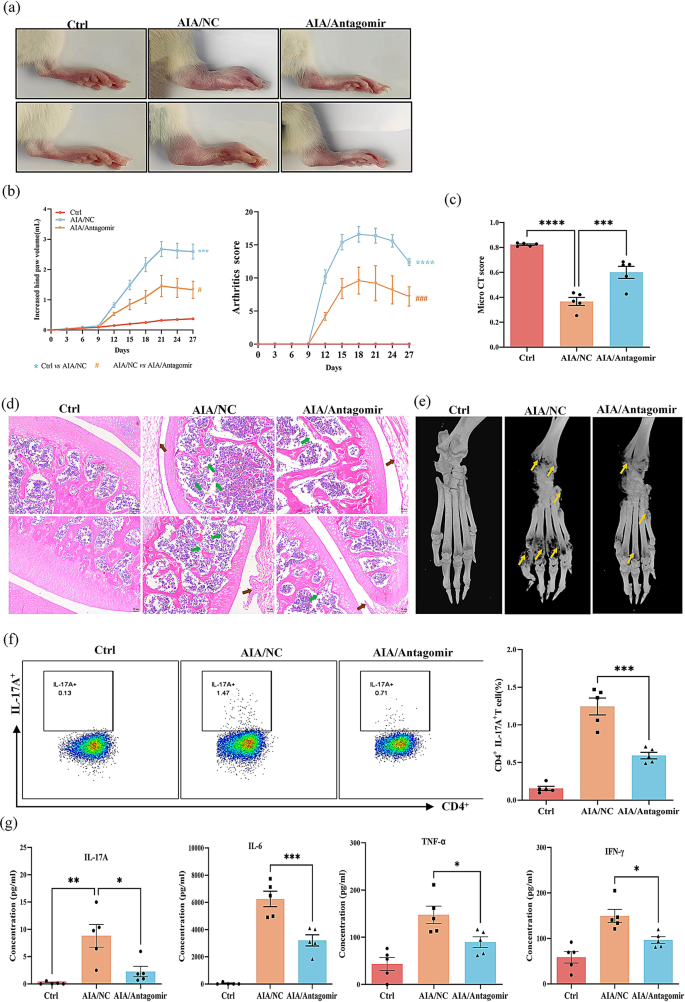
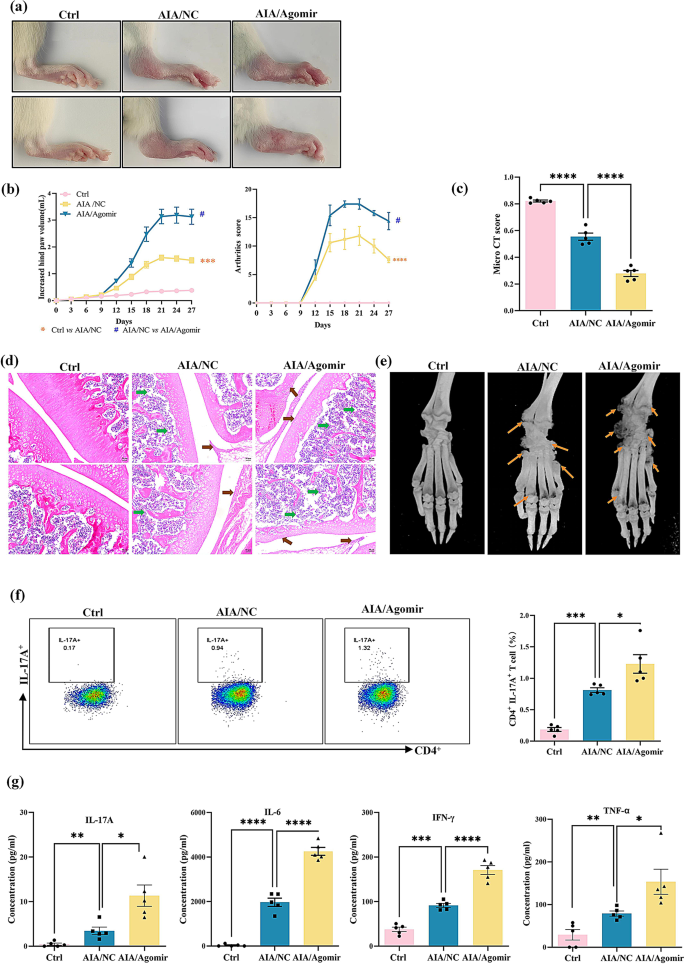
实验所用关键产品:miR-542-5p antagomir(RiboBio)、Lipofectamine RNAiMAX(Invitrogen)、TGF-β(Sinobioogical)、IL-6(Biolegend)等细胞因子。
3.5 miR-542-5p调控Th17分化的机制探究
本环节核心目标是明确miR-542-5p调控Th17分化的分子靶点。研究分离SD大鼠脾脏初始CD4+T细胞,转染miR-542-5p agomir后诱导Th17分化,流式细胞术检测Th17细胞比例,ELISA检测IL-17A浓度;通过生物信息学分析筛选Th17分化调控因子,qRT-PCR验证靶基因表达。结果显示,agomir组miR-542-5p表达水平显著升高(n=3,P<0.0001),Th17细胞比例、IL-17A浓度显著高于对照组(n=3,P<0.001);生物信息学分析结合qRT-PCR验证发现,miR-542-5p可靶向抑制FOXO1、TEAD1表达,抑制miR-542-5p可上调FOXO1、TEAD1表达,进而抑制Th17分化。
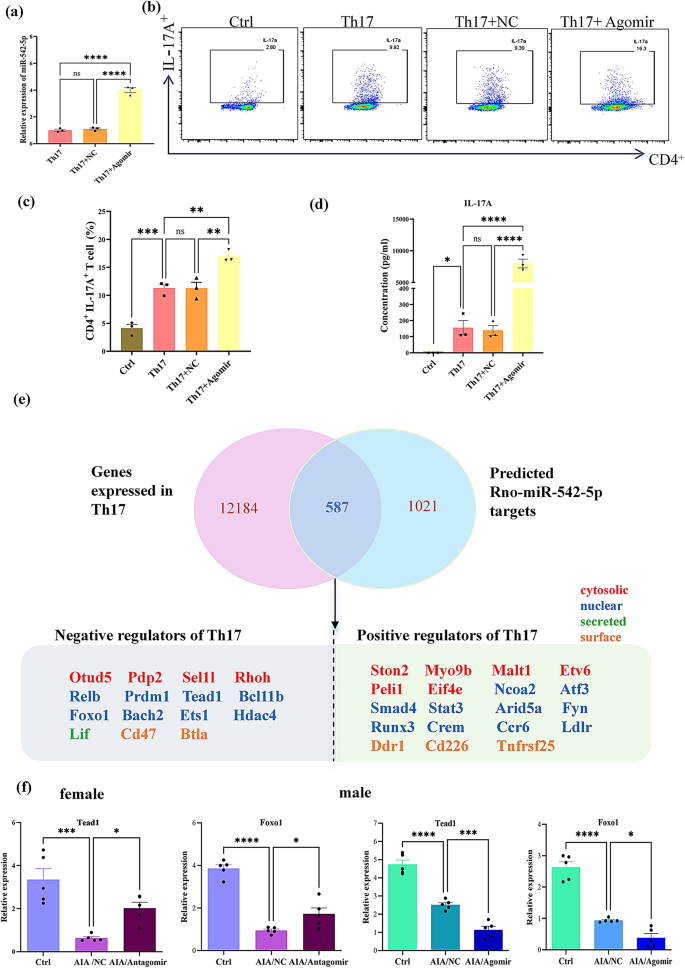
实验所用关键产品:Naive CD4+T Cell Isolation Kit(Miltenyi Biotech)、Lipofectamine RNAiMAX(Invitrogen)、TGF-β(Sinobioogical)、IL-6(Biolegend)等细胞因子。
4. Biomarker研究及发现成果
本研究鉴定的核心Biomarker为X染色体连锁miR-542-5p,筛选逻辑为“临床样本差异表达分析→动物模型功能验证→细胞实验机制探究”的三级验证体系。该Biomarker来源于RA患者和健康人外周血PBMCs、AIA大鼠外周血及脾脏CD4+T细胞,验证方法包括qRT-PCR检测表达水平、动物实验通过agomir/antagomir调控表达验证功能、细胞实验验证对Th17分化的调控作用。特异性方面,RA患者miR-542-5p表达显著高于健康人,RA女性患者表达显著高于男性患者;敏感性方面,动物实验中调控miR-542-5p表达可显著改变RA病情严重程度,细胞实验中可直接调控Th17分化比例。
核心研究成果显示,miR-542-5p是RA性别差异的关键调控因子,通过靶向抑制FOXO1、TEAD1的表达,促进Th17细胞分化,进而加重雌性RA患者的病情;本研究首次明确miR-542-5p作为RA性别特异性诊断标志物和治疗靶点的潜力,为开发RA性别特异性治疗策略提供了分子依据,同时为自身免疫病性别差异的机制研究提供了新的研究范式。目前该Biomarker的临床诊断效能(如ROC曲线AUC值)尚未在大样本中验证,需进一步开展多中心临床研究确认其应用价值。
