1. 领域背景与文献引入
文献英文标题:Consolidative allogeneic hematopoietic stem cell transplantation after chimeric antigen receptor T-cell therapy for relapsed/refractory B-cell acute lymphoblastic leukemia: who? When? Why?;发表期刊:Biomarker Research;影响因子:未公开;研究领域:复发/难治性B细胞急性淋巴细胞白血病(r/r B-ALL)免疫治疗与造血干细胞移植联合策略。
复发/难治性B细胞急性淋巴细胞白血病是成人及儿童急性白血病中预后极差的亚型,患者常伴随高肿瘤负荷、高危基因突变等不良临床特征,传统化疗及靶向治疗难以达到微小残留病(MRD)阴性完全缓解,5年生存率不足20%。2017年,FDA批准首款抗CD19嵌合抗原受体T细胞(CAR-T)产品Tisagenlecleucel用于r/r B-ALL治疗,标志着该领域进入免疫治疗时代,CAR-T细胞治疗可使70%以上的患者获得完全缓解,但疾病复发仍是制约长期生存的核心问题,复发机制包括CAR-T细胞耗竭、CD19阴性白血病克隆逃逸、肿瘤微环境免疫抑制等。目前临床面临的关键空白在于:CAR-T细胞治疗后哪些患者需要接受巩固性异基因造血干细胞移植(allo-HSCT)、最佳治疗窗口如何选择、移植方案如何优化等问题尚未形成统一共识,因此本研究通过系统汇总全球临床研究数据,明确CAR-T后allo-HSCT的获益人群、治疗时机及临床管理策略,为临床决策提供循证依据。
2. 文献综述解析
本文献综述部分以“CAR-T治疗后复发风险分层-allo-HSCT获益关联-治疗时机与方案优化”为核心评述逻辑,将现有研究按患者基线特征、治疗过程参数、预后监测指标三个维度分类整合。现有研究的关键结论显示,抗CD19 CAR-T细胞治疗能显著提升r/r B-ALL患者的缓解率,但单纯CAR-T治疗的12个月无事件生存期仅约50%,成人患者长期生存获益更有限;allo-HSCT作为巩固治疗可将患者复发率从51.3%降至13.3%,但仅特定人群能从中获益。现有研究的技术方法优势在于覆盖了不同CAR-T产品(如CD28共刺激域的KTE-C19、4-1BB共刺激域的CTL019)及东西方多中心临床数据,能全面反映真实世界治疗现状;局限性则体现在多数研究为单中心回顾性分析,缺乏大样本随机对照试验,且不同研究的CAR-T制备工艺、移植预处理方案存在异质性,导致结果可比性受限。本研究的创新价值在于首次系统梳理了CAR-T治疗全流程中的复发预测因素,明确了allo-HSCT的获益人群(具有复杂核型、高危基因、高MRD等风险因素的成人患者)及最佳治疗窗口(MRD阴性缓解后3个月内),并构建了标准化临床管理流程图,填补了r/r B-ALL患者CAR-T治疗后分层管理的循证医学空白。
3. 研究思路总结与详细解析
本研究的整体目标是明确r/r B-ALL患者CAR-T治疗后巩固性allo-HSCT的获益人群、最佳治疗时机及方案,核心科学问题为如何通过风险分层指标指导CAR-T后allo-HSCT的临床决策,技术路线遵循“临床数据汇总→复发风险因素分析→allo-HSCT获益关联验证→治疗策略优化→临床管理建议”的闭环逻辑。
3.1 临床研究数据汇总与筛选
本环节的核心目标是全面收集CAR-T后allo-HSCT的临床证据,为后续分析提供循证基础。研究人员系统检索了全球已发表的r/r B-ALL患者接受抗CD19 CAR-T治疗后行allo-HSCT的临床研究,最终纳入12项符合标准的临床研究,覆盖429例经CAR-T治疗达到完全缓解(CR)或伴不完全血液学恢复的完全缓解(CRi)的患者,其中203例接受巩固性allo-HSCT,226例未接受移植。结果显示,接受allo-HSCT的患者复发率为13.3%(n=203),未接受移植的患者复发率为51.3%(n=226),差异具有统计学意义(P<0.001),提示巩固性allo-HSCT能显著降低r/r B-ALL患者CAR-T治疗后的复发风险。文献未提及具体实验产品,领域常规使用抗CD19 CAR-T细胞产品(如Tisagenlecleucel、Axicabtagene ciloleucel)、异基因造血干细胞移植相关试剂(如预处理化疗药物、免疫抑制剂)。
3.2 复发风险因素分层分析
本环节的核心目标是识别CAR-T治疗后复发的预测指标,为allo-HSCT的获益人群筛选提供依据。研究人员将复发风险因素分为三类:预处理患者特征、淋巴细胞清除方案、CAR-T后监测参数。预处理特征中,具有复杂核型、高危基因(如BCR/ABL1、MLL/AF4、TP53)、骨髓MRD≥5%(流式细胞术检测)、淋巴细胞清除前乳酸脱氢酶(LDH)>210U/L、血小板计数<100,000/μL的患者复发风险显著升高;淋巴细胞清除方案未包含氟达拉滨的患者,CAR-T细胞持久性更短,复发风险更高;CAR-T后监测中,骨髓高通量测序检测到持续白血病克隆、CAR-T细胞拷贝数<30拷贝/μg DNA、B细胞再生障碍(BCA)持续时间<3个月、正常B细胞在63天内恢复的患者,复发风险显著增加。文献未提及具体实验产品,领域常规使用流式细胞术、高通量测序检测MRD和白血病克隆,使用聚合酶链反应(PCR)检测CAR-T细胞拷贝数。
3.3 allo-HSCT获益人群与治疗时机确定
本环节的核心目标是明确能从allo-HSCT中获益的患者人群及最佳移植时机。研究人员通过分层分析发现,具有上述高复发风险因素的患者,尤其是无allo-HSCT史、经CAR-T治疗达到MRD阴性缓解的成人患者,allo-HSCT能显著延长其无事件生存期(EFS)和无白血病生存期(LFS);对于儿童及年轻成人患者,单纯CAR-T治疗即可获得约50%的12个月EFS,allo-HSCT的获益相对有限。治疗时机分析显示,allo-HSCT的最佳窗口为CAR-T治疗后3个月内,延迟至80天以上进行移植会显著增加非复发死亡率,降低生存获益。例如,在陆道培医院的研究中,CAR-T后3个月内行allo-HSCT的患者1年LFS为76.9%,而单纯CAR-T治疗的患者仅为11.6%(n=102,P<0.05)。文献未提及具体实验产品,领域常规使用人类白细胞抗原(HLA)配型技术筛选供者,使用预处理化疗方案(如氟达拉滨+环磷酰胺)进行移植前准备。
3.4 临床管理建议构建
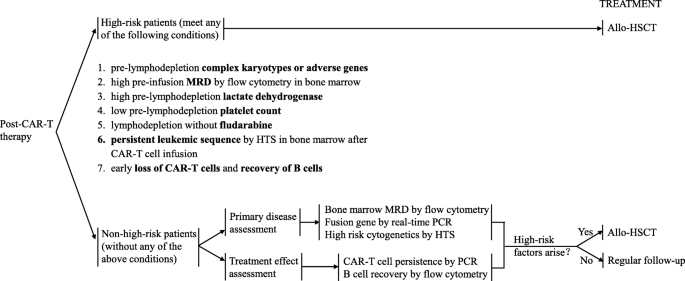
本环节的核心目标是基于研究结果构建r/r B-ALL患者CAR-T治疗后的标准化管理流程。研究人员结合纳入研究的证据及自身中心的临床经验,制定了包含风险分层、供者筛选、治疗监测、移植决策的全流程管理建议:高风险患者在CAR-T治疗前即需筛选合适供者,达到MRD阴性缓解后及时行allo-HSCT;无风险患者定期监测骨髓MRD、CAR-T细胞持久性及B细胞恢复情况,出现复发迹象(如MRD阳性、B细胞早期恢复)时再考虑allo-HSCT。
4. Biomarker研究及发现成果解析
本研究涉及的Biomarker主要为CAR-T治疗全流程中的复发预测指标,筛选逻辑为从患者基线、治疗过程、预后监测三个阶段挖掘与复发风险相关的指标,分为预处理Biomarker、治疗中Biomarker、治疗后Biomarker三类。预处理Biomarker包括复杂核型、高危基因(如BCR/ABL1、TP53)、骨髓MRD≥5%(流式细胞术检测)、LDH>210U/L、血小板计数<100,000/μL;治疗中Biomarker为淋巴细胞清除方案未使用氟达拉滨;治疗后Biomarker包括骨髓高通量测序检测到持续白血病克隆、CAR-T细胞拷贝数<30拷贝/μg DNA、BCA持续时间<3个月、正常B细胞在63天内恢复。研究过程中,通过多中心临床数据关联分析验证了这些Biomarker的预测价值,例如BCA持续时间<3个月的患者,从BCA丢失到CD19阳性复发的中位时间为3.7个月,提示该指标可作为复发的早期预警信号。核心成果方面,这些Biomarker能有效实现CAR-T治疗后患者的风险分层,对于具有高风险Biomarker的患者,巩固性allo-HSCT能将其1年LFS从单纯CAR-T治疗的11.6%提升至76.9%(n=102,P<0.05);其中,正常B细胞恢复这一Biomarker不仅能预测复发,还能为allo-HSCT提供约3.7个月的治疗窗口,帮助临床及时干预。此外,研究首次提出“CAR-T细胞扩增峰值与基线肿瘤负荷的比值>1”是长期生存的独立预测因素,为CAR-T治疗剂量优化提供了新的参考指标。
