1. 领域背景与文献引入
文献英文标题:A meta-analysis of hypoxia inducible factor 1-alpha (HIF1A) gene polymorphisms: association with cancers;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤分子生物学、遗传流行病学。
癌症是全球范围内第二大导致死亡的疾病,其核心特征包括不受控制的细胞增殖、侵袭转移及肿瘤微环境缺氧等。领域共识:肿瘤缺氧是恶性肿瘤进展的关键驱动因素,通过调控下游基因表达影响细胞代谢、血管生成与耐药性。缺氧诱导因子1α(HIF1A)作为缺氧应答的核心转录因子,可调控超过100个参与细胞凋亡、增殖、葡萄糖代谢及血管生成的靶基因,在肿瘤发生发展中发挥关键作用。近年来,全基因组关联研究(GWAS)和病例对照研究表明,HIF1A基因的单核苷酸多态性(SNP)可能与癌症易感性相关,其中rs11549465(1772 C/T)和rs11549467(1790 G/A)是研究最广泛的两个位点。然而,不同研究的结果存在显著异质性,部分研究显示阳性关联,部分则无统计学意义,导致该领域结论尚不明确。因此,亟需通过系统的meta分析整合现有研究数据,明确这两个多态性与癌症风险的关联,为癌症的早期筛查和遗传易感标志物研究提供循证依据。
2. 文献综述解析
本文献综述部分以HIF1A基因多态性与癌症关联的研究进展为核心,按基因多态性位点、研究人群种族及癌症类型的维度对现有研究进行分类评述,重点探讨了现有研究的争议点与局限性,为本次meta分析的开展奠定了逻辑基础。
现有研究的关键结论可分为三类:部分研究发现HIF1A 1772 C/T多态性的T等位基因与肺癌、口腔鳞状细胞癌等风险增加相关;部分研究指出1790 G/A多态性的A等位基因在亚洲人群中与多种癌症风险显著相关;还有部分研究未发现两个多态性与特定癌症的关联。现有研究的技术方法以病例对照研究和GWAS为主,优势在于能够直接关联遗传变异与疾病风险,部分大样本研究具有较高的统计学效力;但局限性也较为明显,包括单个研究的样本量有限,人群种族、癌症类型的异质性大,不同研究的基因分型方法存在差异,导致结果难以统一,且缺乏针对异质性来源的系统分析。本研究的创新价值在于,首次系统整合了截至2014年的22项1772 C/T多态性研究(样本量19024)和19项1790 G/A多态性研究(样本量10654),通过严格的纳入排除标准筛选研究,采用亚组分析按癌症类型和人群种族分层,明确了两个多态性与总体癌症风险的关联,并解析了异质性的主要来源,弥补了现有研究结论不一致的缺陷,为HIF1A多态性作为癌症遗传易感标志物的应用提供了更可靠的循证证据。
3. 研究思路总结与详细解析
本研究的整体研究目标是明确HIF1A基因rs11549465(1772 C/T)和rs11549467(1790 G/A)多态性与癌症风险的关联,核心科学问题是这两个多态性是否可作为癌症的遗传易感生物标志物,技术路线遵循“文献检索与筛选→数据提取→统计学分析→结果解读与验证”的闭环逻辑,通过meta分析整合多中心研究数据,结合亚组分析和异质性检验明确关联的特异性与稳定性。
3.1 文献检索与研究筛选
实验目的是系统检索并筛选符合标准的HIF1A多态性与癌症关联的病例对照研究及GWAS,确保纳入研究的质量与一致性。方法细节:检索PubMed、PubMed Central和Google Scholar数据库,时间范围为过去15年(截至2014年12月),检索词包括HIF1A、GWAS、SNPs、polymorphisms、C1772T、A1790G、case-control study、cancer;由两位研究者独立筛选文献,纳入标准为:病例对照研究或GWAS、研究人群明确、提供等位基因频率数据、发表于英文期刊;排除标准为:非人类研究、综述、编辑评论、未提供完整基因型数据的研究。结果解读:最终纳入22项1772 C/T多态性研究(包含8149例癌症患者和10875例对照)和19项1790 G/A多态性研究(包含4681例患者和5973例对照),涵盖前列腺癌、肺癌、肾细胞癌等10余种癌症类型,研究人群包括白种人、亚洲人及混合人群。
文献未提及具体实验产品,领域常规使用文献检索数据库(如PubMed)及文献管理软件(如EndNote)。
3.2 数据提取与纳入研究特征分析
实验目的是提取纳入研究的关键信息,明确研究特征,为后续meta分析奠定基础。方法细节:从纳入研究中提取作者、发表年份、人群种族、癌症类型、等位基因频率等信息,对癌症类型进行分类,将仅包含单个研究的癌症类型归为“其他癌症”类别。结果解读:纳入的1772 C/T多态性研究涵盖10种癌症,其中前列腺癌、肺癌、肾细胞癌等研究数量较多;1790 G/A多态性研究涵盖11种癌症,肺癌、口腔鳞状细胞癌的研究数据较为丰富;人群分布以亚洲人和白种人为主,混合人群研究数量较少。
文献未提及具体实验产品,领域常规使用Excel等数据处理软件进行数据提取与整理。
3.3 统计学分析与关联验证
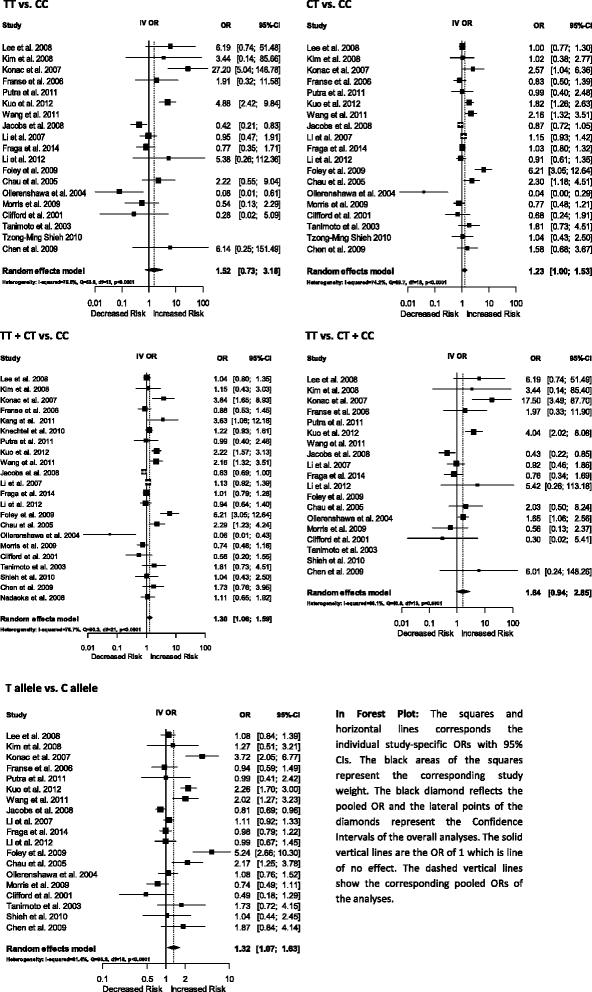
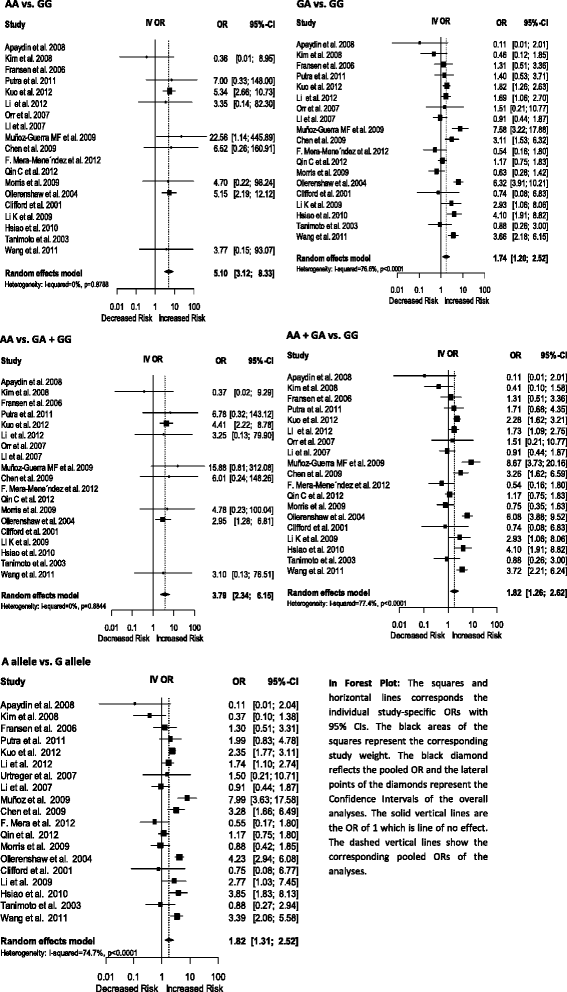
实验目的是通过meta分析计算HIF1A多态性与癌症风险的关联强度,分析异质性来源,明确关联的特异性。方法细节:采用R语言的“meta”包进行统计分析,计算不同遗传模型下的比值比(OR)及95%置信区间(CI),采用随机效应模型(REM)整合数据;通过Q检验和I²指数评估异质性,I²>50%定义为显著异质性;按癌症类型和人群种族进行亚组分析,解析异质性来源;进行Hardy-Weinberg平衡(HWE)检验,对不符合HWE的研究进行敏感性分析。结果解读:对于1772 C/T多态性,T等位基因与总体癌症风险增加显著相关(OR=1.32,95%CI 1.07-1.63,P=0.0098),显性模型(TT+CT vs CC)的OR=1.30(P=0.0115);亚组分析显示,TT基因型与肺癌风险显著增加相关(OR=4.88,P<0.0001),但与肾细胞癌风险降低相关(OR=0.27,P=0.0335);亚洲人群中该多态性与癌症风险显著相关,白种人群中无显著关联。对于1790 G/A多态性,A等位基因与总体癌症风险显著相关(OR=1.82,95%CI 1.31-2.52,P=0.0003),纯合子模型(AA vs GG)的OR=5.10(P<0.0001);亚组分析显示,该多态性与肺癌、口腔鳞状细胞癌风险显著增加相关,且在白种人和亚洲人群中均与癌症风险显著相关。异质性分析显示,癌症类型和人群种族是异质性的主要来源,亚组分析后异质性显著降低。
文献未提及具体实验产品,领域常规使用R语言统计分析软件及对应的meta分析包。
3.4 发表偏倚与敏感性分析
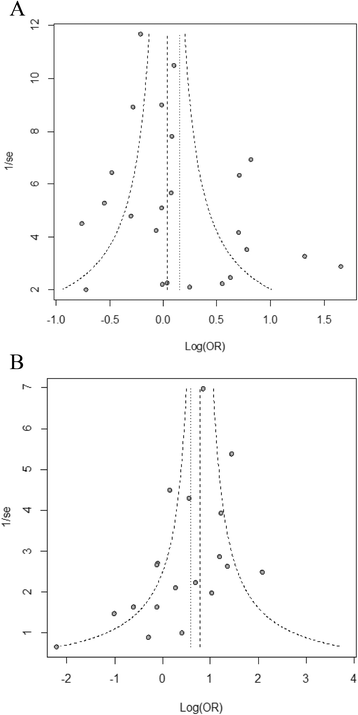
实验目的是评估纳入研究的发表偏倚,验证meta分析结果的稳定性。方法细节:通过漏斗图直观评估发表偏倚,采用Egger检验进行定量分析;排除不符合HWE的研究后进行敏感性分析,观察结果的变化。结果解读:漏斗图显示存在潜在发表偏倚,但Egger检验未发现显著的发表偏倚(1772 C/T:t=1.83,P=0.0847;1790 G/A:t=-1.87,P=0.0787);敏感性分析显示,排除不符合HWE的研究后,结果的统计学显著性未发生改变,表明meta分析结果稳定可靠。
文献未提及具体实验产品,领域常规使用R语言统计分析软件进行发表偏倚检验。
4. Biomarker研究及发现成果
本研究聚焦的Biomarker为HIF1A基因的两个单核苷酸多态性位点:rs11549465(1772 C/T)和rs11549467(1790 G/A),通过系统的meta分析明确了其与癌症风险的关联,为癌症的遗传易感筛查提供了潜在标志物。
Biomarker定位:两个多态性均位于HIF1A基因第12外显子的ODD/pVHL结构域,属于功能型SNP,可能通过改变HIF1A蛋白的稳定性和转录活性影响下游基因表达。筛选与验证逻辑为:基于已发表的病例对照研究和GWAS数据,通过严格的纳入排除标准筛选研究,采用meta分析整合大样本数据,通过亚组分析按癌症类型和人群种族分层验证关联的特异性,通过异质性分析和敏感性分析验证结果的稳定性。
研究过程详述:Biomarker的来源为已发表研究中的人类病例对照样本,验证方法为计算不同遗传模型下的OR及95%CI,评估关联强度;特异性与敏感性数据显示,1772 C/T多态性的T等位基因作为总体癌症风险标志物的OR=1.32(95%CI 1.07-1.63,P=0.0098),在肺癌中的OR=4.88(95%CI 2.42-9.84,P<0.0001);1790 G/A多态性的A等位基因作为总体癌症风险标志物的OR=1.82(95%CI 1.31-2.52,P=0.0003),在口腔鳞状细胞癌中的OR=5.00(95%CI 2.10-11.97,P=0.0003);亚组分析显示,1790 G/A多态性在白种人(AA vs GG OR=5.68,P<0.0001)和亚洲人群(AA vs GG OR=4.76,P<0.0001)中均与癌症风险显著相关。
核心成果提炼:两个多态性均可作为癌症的遗传易感生物标志物,其中1772 C/T多态性的TT基因型是肺癌的高风险标志物,同时是肾细胞癌的低风险标志物;1790 G/A多态性的A等位基因是多种癌症的高风险标志物,尤其在肺癌、口腔鳞状细胞癌及亚洲、白种人群中具有显著的预测价值。本研究的创新性在于首次系统整合大样本数据,明确了两个多态性与癌症风险的关联及异质性来源,为癌症的早期遗传筛查和风险分层提供了循证依据;但研究也存在局限性,如未纳入最新研究数据,未分析基因-环境交互作用,未来需进一步开展功能实验验证多态性的生物学机制。
