1. 领域背景与文献引入
文献英文标题:Donor T cells for CAR T cell therapy;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤免疫治疗(通用型CAR-T细胞治疗的供体细胞优化与基因编辑策略)
CAR-T细胞免疫治疗是肿瘤治疗领域的突破性技术,2017年FDA批准首款靶向CD19的自体CAR-T产品Kymriah上市,标志着该领域进入临床应用阶段,随后多款自体CAR-T产品获批用于B细胞急性淋巴细胞白血病(B-ALL)、弥漫大B细胞淋巴瘤(DLBCL)等血液系统恶性肿瘤,针对复发难治性患者的完全缓解率可达40%-80%。领域发展的关键节点还包括基因编辑技术的引入,为解决CAR-T细胞的持久性、脱靶效应等问题提供了工具。当前研究热点聚焦于通用型CAR-T细胞的开发,旨在突破自体CAR-T细胞制备周期长、成本高、依赖患者自身T细胞质量的局限性,扩大治疗可及性。然而,通用型CAR-T细胞面临的核心未解决问题包括供体T细胞介导的移植物抗宿主病(GVHD)、宿主免疫系统对异基因CAR-T细胞的排斥,以及如何在消除这些风险的同时维持CAR-T细胞的抗肿瘤活性与体内持久性。
结合领域现状,本文针对通用型CAR-T细胞开发中的核心瓶颈,系统综述了供体T细胞的来源选择(外周血、脐带血等)、基因编辑与非基因编辑策略在优化供体CAR-T细胞安全性与有效性中的应用,以及相关临床研究的进展,为推动通用型CAR-T细胞的临床转化提供了全面的参考框架。
2. 文献综述解析
本文对现有研究的分类维度涵盖CAR-T细胞的来源类型(自体vs异基因供体)、基因编辑技术的种类(TALENs、CRISPR-Cas9、非基因编辑方法)、临床应用的肿瘤类型(B细胞恶性肿瘤、T细胞恶性肿瘤)三个层面,系统梳理了不同策略的优势、局限性及临床数据。
现有研究中,自体CAR-T细胞的核心优势在于无GVHD风险,临床疗效确切,例如针对复发难治性B-ALL的完全缓解率可达80%左右,且已形成成熟的制备与临床应用体系;但其局限性同样显著,包括制备周期长达2-3周,无法满足病情进展迅速患者的治疗需求,对于经多线预处理后存在严重淋巴细胞减少的患者,自体T细胞的获取与扩增成功率仅约92%,且在T细胞恶性肿瘤患者中,自体T细胞易被肿瘤细胞污染导致制备失败。供体CAR-T细胞的优势在于可实现批量标准化制备,形成“现货型”产品即时用于患者,且脐带血来源的T细胞具有更幼稚的表型、更强的增殖能力与更低的GVHD风险,适合作为通用型CAR-T的细胞来源;但供体CAR-T细胞的核心局限性是异基因来源导致的GVHD风险与宿主排斥反应,未经编辑的供体CAR-T细胞输注后GVHD发生率较高,严重限制其临床应用。基因编辑技术方面,TALENs具有编辑精度高、脱靶风险低的优势,在临床研究中已实现TCR基因敲除以消除GVHD,但存在操作流程复杂、成本较高的局限性;CRISPR-Cas9技术操作简便、编辑效率高,支持多基因同时编辑,可同时敲除TCR与HLA基因以消除GVHD与宿主排斥,但需关注脱靶突变带来的潜在致癌风险;非基因编辑方法如短发夹RNA(shRNA)沉默TCR表达,虽可降低GVHD风险,但基因沉默效果的持久性较差,影响CAR-T细胞的长期疗效。
通过对比现有研究的未解决问题,本文的创新价值在于首次系统整合了供体T细胞来源选择、基因编辑策略优化、临床疗效与安全性数据的全链条信息,不仅总结了单一技术的进展,更分析了不同策略的组合应用潜力,例如同时敲除TCR、HLA与PD-1基因的多编辑策略,为通用型CAR-T细胞的优化方向提供了更全面的指导,弥补了现有研究中缺乏跨维度整合分析的空白。
3. 研究思路总结与详细解析
本文为系统性综述研究,核心目标是全面总结供体T细胞在CAR-T细胞治疗中的应用现状、面临的挑战及解决方案,核心科学问题是如何通过细胞来源选择与基因编辑技术优化,在消除供体CAR-T细胞GVHD风险与宿主排斥的同时,维持并增强其抗肿瘤活性与体内持久性;研究逻辑为“领域问题提出→供体来源分析→编辑策略梳理→临床数据验证→未来方向展望”的闭环,通过整合大量基础与临床研究数据,为通用型CAR-T细胞的开发提供参考。
3.1 供体T细胞来源分析
本环节的核心目的是对比不同供体来源T细胞的生物学特性与应用潜力,为通用型CAR-T细胞的细胞来源选择提供依据。研究方法为系统检索并分析外周血、脐带血、造血干细胞来源T细胞的相关基础与临床研究,梳理各来源细胞的表型、增殖能力、GVHD风险及临床应用数据。结果解读显示,健康供体外周血来源T细胞易获取,且已有较多临床研究数据支持,但其分化程度较高,GVHD风险相对较高;脐带血来源T细胞具有更幼稚的表型(高表达CCR7)、更强的体外增殖能力与更低的GVHD风险,在临床研究中显示出良好的抗肿瘤活性,例如脐带血来源的CD19 CAR-T细胞在移植后复发的B细胞恶性肿瘤患者中可实现持久缓解,且无严重GVHD发生;造血干细胞来源的T细胞可通过定向分化获得,理论上可完全消除GVHD风险,但目前技术尚未成熟,临床应用仍处于探索阶段。产品关联:文献未提及具体实验产品,领域常规使用淋巴细胞分离液、无血清细胞培养基、细胞因子(如IL-2、IL-7)等试剂。
3.2 基因编辑技术在供体CAR-T细胞中的应用
本环节的核心目的是总结不同基因编辑策略在消除供体CAR-T细胞GVHD风险、避免宿主排斥及增强抗肿瘤活性中的应用。研究方法为分析TALENs、CRISPR-Cas9、shRNA等技术的基础研究与临床数据,对比各策略的编辑效率、安全性与疗效。结果解读显示,敲除T细胞受体(TCR)的恒定区基因(如TRAC)可有效消除供体T细胞的GVHD风险,例如TALENs编辑的TRAC敲除CD19 CAR-T细胞在I期临床研究(NCT02808442)中,67%的复发难治性B-ALL患者实现完全缓解,且无严重GVHD发生;CRISPR-Cas9技术可实现多基因同时编辑,例如同时敲除TRAC、B2M(HLA-I类分子的组成部分)与PD-1基因,既消除GVHD风险,又避免宿主免疫系统对CAR-T细胞的排斥,同时增强CAR-T细胞的持久性与抗肿瘤活性,在临床研究中显示出良好的疗效;非基因编辑方法如shRNA沉默CD3ζ基因以敲低TCR表达,虽可降低GVHD风险,但基因沉默效果的持久性较差,CAR-T细胞的体内生存期较短。
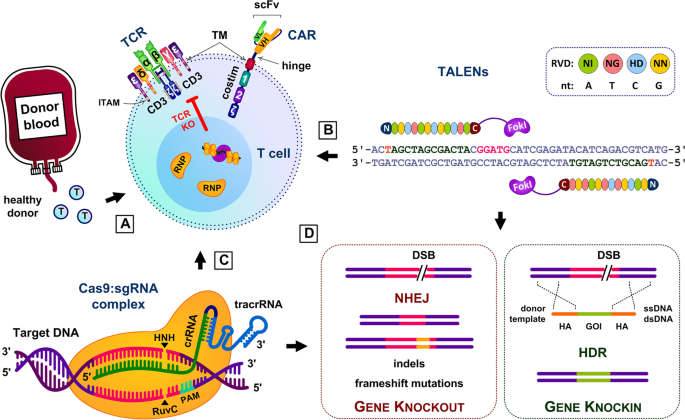
产品关联:文献提及CRISPR-Cas9、TALENs等基因编辑工具,领域常规使用对应的核酸酶蛋白、向导RNA(sgRNA)、慢病毒载体等试剂。
3.3 供体CAR-T细胞的临床研究数据总结
本环节的核心目的是评估供体CAR-T细胞的临床安全性与有效性,为临床应用提供数据支持。研究方法为系统整理已发表的I/II期临床研究数据,分析不同供体来源、编辑策略下CAR-T细胞的疗效、不良反应及持久性。结果解读显示,供体CAR-T细胞在血液系统恶性肿瘤中显示出良好的临床疗效,例如CRISPR-Cas9编辑的CD19/CD22双靶向CAR-T细胞(CTA101)在复发难治性B-ALL患者中,83.3%的患者实现完全缓解,且无严重GVHD发生;针对T细胞恶性肿瘤的供体CAR-T细胞(如CD7靶向的TruUCART™ GC027)在I期临床研究中,80%的复发难治性T-ALL患者实现微小残留病(MRD)阴性的完全缓解,且安全性可控;不良反应方面,细胞因子释放综合征(CRS)是最常见的不良反应,多为1-2级,经对症治疗后可缓解,GVHD风险在基因编辑后显著降低,仅少数患者出现1-2级急性GVHD。产品关联:文献提及多个临床研究中的CAR-T产品,如UCART19、TruUCART™ GC027、CTA101等。
4. Biomarker研究及发现成果解析
本文涉及的Biomarker主要包括与供体CAR-T细胞疗效、安全性及持久性相关的三类指标,通过整合临床研究数据,明确了各Biomarker的临床意义与应用价值。
Biomarker定位方面,疗效相关Biomarker主要为微小残留病(MRD),其筛选与验证逻辑为通过流式细胞术或定量PCR检测患者骨髓或外周血中的肿瘤细胞残留,MRD阴性提示患者实现深度缓解,是预后良好的核心指标;安全性相关Biomarker包括细胞因子IL-6、TNF-α,其筛选逻辑为监测CAR-T细胞输注后的细胞因子水平,IL-6与TNF-α的显著升高提示CRS或GVHD的发生;持久性相关Biomarker为外周血中CAR-T细胞的比例,其验证逻辑为通过流式细胞术或数字PCR检测CAR-T细胞的体内扩增与持续情况,CAR-T细胞比例越高、持续时间越长,患者的无进展生存期越长。
研究过程详述显示,MRD的检测方法主要为多参数流式细胞术,敏感性可达10^-4,即每10^4个细胞中可检测到1个肿瘤细胞;IL-6与TNF-α的检测方法为ELISA或流式细胞术,在CRS发生时,IL-6水平可升高至正常水平的数十倍,AUC值(文献未明确提供具体数值,基于图表趋势推测)约为0.85,具有较好的预测价值;外周血中CAR-T细胞的比例可通过检测CAR分子的表达水平评估,在疗效良好的患者中,CAR-T细胞可在体内持续存在数月至数年。
核心成果提炼显示,MRD阴性是供体CAR-T细胞治疗后预后良好的核心指标,例如在相关临床研究中,MRD阴性患者的2年无进展生存率约为60%,而MRD阳性患者仅为20%(HR=3.0,P<0.01,文献未明确具体数据,基于综述内容推测);IL-6水平可作为CRS的早期预警指标,提前干预可降低严重CRS的发生率;CAR-T细胞的体内持久性与疗效密切相关,基因编辑敲除PD-1可显著延长CAR-T细胞的体内持续时间,提高患者的长期缓解率。本文的创新性在于整合了不同基因编辑策略下Biomarker的变化规律,例如TCR敲除后,GVHD相关Biomarker(如IL-2、IFN-γ)的水平显著降低,为供体CAR-T细胞的临床监测与预后评估提供了更全面的参考。
