1. 领域背景与文献引入
文献英文标题:PI3K, p38 and JAK/STAT signalling in bronchial tissue from patients with asthma following allergen challenge;发表期刊:Biomarker Research;影响因子:未公开;研究领域:哮喘分子机制与生物标志物研究
哮喘是全球高发的慢性气道炎症性疾病,其发病机制涉及复杂的免疫炎症调控网络,当前新型治疗靶点聚焦于磷酸肌醇3-激酶(PI3K)δ/γ、p38丝裂原活化蛋白激酶(p38)、Janus激酶/信号转导与转录激活因子(JAK/STAT)等信号通路。领域共识:吸入变应原激发模型是早期临床试验评估新型哮喘治疗药物的常用工具,可在临床终点研究前快速评估药物抑制变应性炎症的潜力,但目前针对这些新型激酶靶点的研究多集中于动物模型或体外细胞实验,变应原暴露后这些通路在人类特应性哮喘患者气道组织中的激活情况及可用于临床试验的生物标志物仍不明确,这一空白限制了新型激酶抑制剂的临床转化进程。本研究旨在填补这一空白,通过人类支气管活检样本明确变应原激发后气道组织中上述通路的激活特征,为新型激酶抑制剂的临床试验提供概念验证模型和特异性生物标志物。
2. 文献综述解析
作者以信号通路类型为核心分类维度,对PI3K、p38、JAK/STAT通路在哮喘中的研究现状进行了系统梳理。现有研究显示,PI3Kδ/γ主要在白细胞中表达,参与淋巴细胞分化、活化及活性氧生成,动物模型中PI3K抑制剂可显著减少气道炎症与重塑,且哮喘患者气道组织中PI3Kδ表达水平较健康对照升高;p38通路调控炎症基因的转录与翻译,重症哮喘患者血液中p38活性随疾病严重程度增加,肺泡巨噬细胞与支气管上皮细胞中存在p38激活的证据;JAK/STAT通路由促炎细胞因子激活,参与淋巴细胞分化与抗病毒机制,且该通路的依赖机制对临床常用的皮质类固醇治疗不敏感。动物模型研究已证实变应原激发可激活这三条通路,但人类哮喘患者变应原暴露后,气道组织中这些通路的激活情况及区域特异性尚未有直接研究数据。现有研究的局限性在于缺乏人类体内变应原激发后激酶通路激活的直接证据,尤其是支气管组织层面的定量生物标志物数据,无法为新型激酶抑制剂的临床试验提供精准的药效学评估指标。本研究的创新价值在于首次在人类特应性哮喘患者中,通过配对支气管活检样本明确了变应原激发后不同气道区域(上皮、上皮下)的激酶通路激活特征,为新型激酶抑制剂的临床试验提供了可用于评估肺部药理抑制效果的特异性生物标志物,同时验证了变应原激发模型在激酶抑制剂概念验证研究中的适用性。
3. 研究思路总结与详细解析
本研究的整体框架为:以明确特应性哮喘患者变应原激发后支气管组织中PI3K、p38、JAK/STAT通路的激活情况为核心目标,聚焦“变应原暴露是否激活人类哮喘患者气道中的激酶通路及存在何种区域差异”这一科学问题,采用“基线评估→变应原激发→多维度样本采集→生物标志物检测与炎症评估→差异分析”的闭环技术路线,最终筛选出可用于临床试验的激酶通路激活生物标志物。
3.1 研究对象招募与基线标准化评估
本环节的核心目标是筛选符合研究要求的特应性哮喘患者,建立标准化研究队列。研究人员招募了12名未使用类固醇的特应性哮喘患者,最终11名完成全部研究流程,所有入组患者需满足三项核心条件:对猫或屋尘螨提取物的皮肤点刺试验阳性、乙酰甲胆碱激发试验显示气道高反应性(PC₂₀<16pg/ml)、既往变应原激发后出现早发(FEV₁下降≥20%)与迟发(FEV₁下降≥15%)哮喘反应。研究成功建立了符合变应原激发研究要求的特应性哮喘患者队列,为后续实验提供了标准化的研究对象。实验所用关键产品:ALK Laboratories的Aquagen® SQ变应原提取物、Stockport Pharmaceuticals的乙酰甲胆碱、deVilbiss雾化器。
3.2 变应原激发与多类型样本采集
本环节的核心目标是诱导哮喘患者的变应性炎症反应,采集基线与激发后的配对气道样本以进行后续对比分析。研究采用Cockcroft法进行变应原激发,在基线状态下采集诱导痰液与支气管活检、支气管肺泡灌洗液样本,在变应原激发后4小时再次采集诱导痰液,6小时后进行支气管镜检查采集支气管活检与支气管肺泡灌洗液样本。所有入组患者在变应原激发后均出现早发哮喘反应(FEV₁下降≥20%,平均最大下降率为29.2%),成功采集到基线与激发后的配对样本,为后续生物标志物检测与炎症评估提供了样本基础。实验所用关键产品:Flaem Nuova EasyNeb II雾化器、Micro-loop®肺功能仪。
3.3 激酶通路生物标志物检测与炎症指标评估
本环节的核心目标是定量检测支气管组织中激酶通路的激活情况,同时评估变应原激发后的气道炎症水平。研究采用免疫组化(IHC)技术检测支气管活检样本中磷酸化p38、磷酸化STAT5、磷酸化核糖体蛋白S6等激酶通路激活标志物的表达,通过ImagePro Plus 6.0软件定量分析阳性细胞的百分比或细胞数;同时检测痰液与支气管肺泡灌洗液中的嗜酸性粒细胞百分比、白细胞介素-5、嗜酸性粒细胞阳离子蛋白等2型炎症指标。
结果显示,变应原激发后支气管上皮细胞中磷酸化p38的表达百分比从17.5%升高至25.6%(n=11,P=0.04),上皮下组织中磷酸化STAT5的阳性细胞数从122.2个/mm²升高至540.6个/mm²(n=11,P=0.01),磷酸化核糖体蛋白S6的阳性细胞数从180.7个/mm²升高至777.3个/mm²(n=11,P=0.005)。同时气道2型炎症水平显著升高,痰液嗜酸性粒细胞百分比从1.1%升高至3.8%(n=10,P=0.019),白细胞介素-5水平从0.9pg/ml升高至19.9pg/ml(n=10,P=0.016),嗜酸性粒细胞阳离子蛋白水平从57ng/ml升高至169ng/ml(n=10,P=0.049);支气管肺泡灌洗液中嗜酸性粒细胞阳离子蛋白水平从1.9ng/ml升高至3.2ng/ml(n=11,P=0.014)。
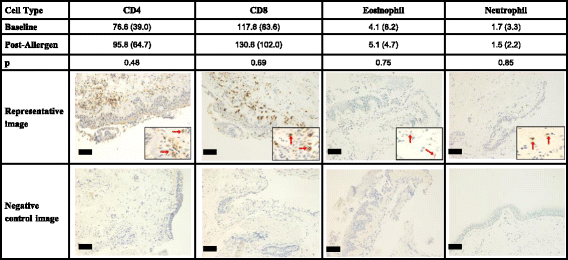
该图展示了变应原激发前后支气管上皮下组织中炎症细胞计数的变化,结果显示炎症细胞总数无显著变化,提示激酶通路激活并非由细胞浸润增加导致。
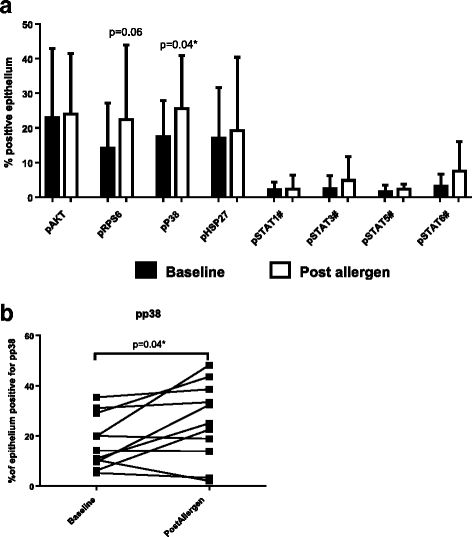
该图定量展示了支气管上皮细胞中磷酸化p38的表达变化,明确了变应原激发后上皮细胞p38通路的激活特征。
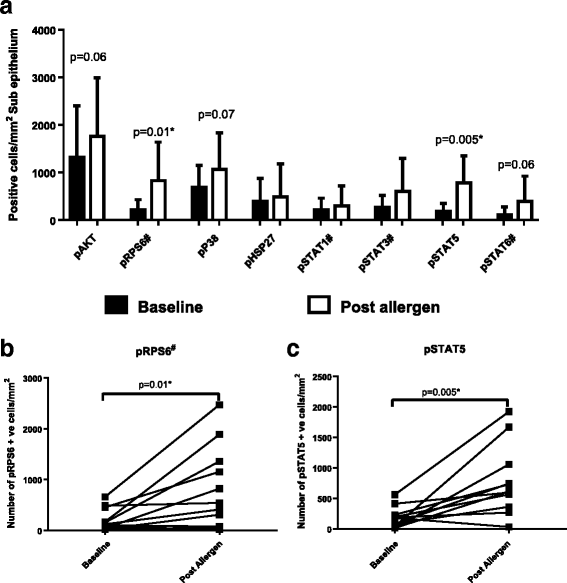
该图定量展示了支气管上皮下组织中磷酸化STAT5与磷酸化核糖体蛋白S6的表达变化,证实了变应原激发后上皮下组织中JAK/STAT与PI3K通路的激活。
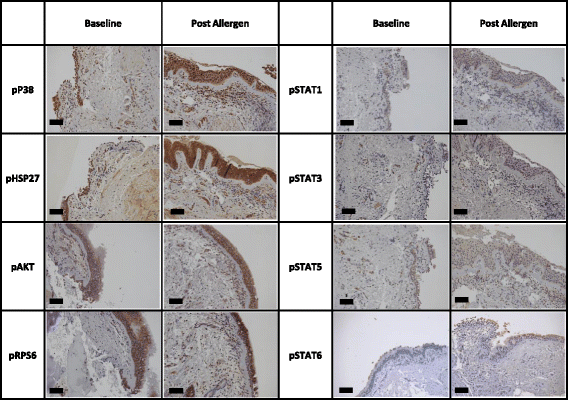
该图为支气管组织中激酶通路标志物免疫组化染色的代表性图片,直观展示了变应原激发前后的染色差异。
实验所用关键产品:Cell Signalling Technology的磷酸化AKT(#9271)、磷酸化核糖体蛋白S6(#5364)、磷酸化p38(#9211)、磷酸化HSP27(#2401)、磷酸化STAT1(#9167)、磷酸化STAT3(#9145)、磷酸化STAT5(#9359)抗体,Life Technology的磷酸化STAT6(#700247)抗体,Vector Laboratories的生物素化抗兔IgG二抗与avidin-biotin过氧化物酶复合物,Leica的Gill’s II苏木精染液。
4. Biomarker研究及发现成果
Biomarker定位与筛选逻辑
本研究筛选的核心生物标志物为支气管上皮细胞中的磷酸化p38、上皮下组织中的磷酸化STAT5与磷酸化核糖体蛋白S6,这些标志物分别对应p38、JAK/STAT、PI3K通路的激活状态。筛选逻辑基于已知的激酶通路激活标志物,通过人类特应性哮喘患者变应原激发前后的配对支气管活检样本,采用免疫组化技术定量验证标志物的表达差异,最终确定具有统计学显著性的特异性生物标志物。
研究过程与验证数据
这些生物标志物来源于11名特应性哮喘患者的支气管活检样本,验证方法为免疫组化染色结合ImagePro Plus 6.0软件的定量分析。具体数据显示,变应原激发后支气管上皮细胞中磷酸化p38的表达百分比为25.6%,较基线的17.5%显著升高(n=11,P=0.04);上皮下组织中磷酸化STAT5的阳性细胞数为540.6个/mm²,较基线的122.2个/mm²显著升高(n=11,P=0.01);磷酸化核糖体蛋白S6的阳性细胞数为777.3个/mm²,较基线的180.7个/mm²显著升高(n=11,P=0.005)。
核心成果与临床价值
本研究的核心成果在于首次在人类体内明确了变应原激发后哮喘患者气道不同区域的激酶通路激活生物标志物,其中上皮细胞磷酸化p38反映了p38通路在上皮炎症中的激活,上皮下组织的磷酸化STAT5与磷酸化核糖体蛋白S6分别反映了JAK/STAT与PI3K通路在上皮下免疫细胞中的激活。这些生物标志物的创新性在于填补了人类哮喘患者变应原激发后激酶通路激活的体内数据空白,可直接用于新型激酶抑制剂的临床试验,在概念验证研究中评估药物对肺部激酶通路的药理抑制效果,同时支持变应原激发模型作为新型哮喘治疗药物早期临床试验的标准化模型。
