1. 领域背景与文献引入
文献英文标题:Harnessing multi-omics approaches to decipher tumor evolution and improve diagnosis and therapy in lung cancer;发表期刊:Biomark Res;影响因子:未公开;研究领域:肺癌多组学与肿瘤进化、精准诊疗
肺癌已成为全球范围内严重威胁人类健康的恶性肿瘤,据估计2024年肺癌相关死亡将占所有癌症相关死亡的20%,尽管诊断策略和治疗手段取得了显著进展,但多数国家肺癌患者的5年生存率仍低于20%,因此亟需优化肺癌的诊断与治疗策略,实现早期检测、精准干预和全面患者管理。领域共识:单组学技术(如基因组学、转录组学、表观组学等)已在肺癌研究中做出诸多贡献,包括识别驱动基因、表征肿瘤微环境、捕捉空间组织特征等,但由于肺癌具有高度复杂性、异质性,且肿瘤细胞与免疫微环境存在复杂的细胞间相互作用,单维度的单组学方法难以区分这些混杂特征,无法全面揭示肿瘤进化的分子机制。在此背景下,多组学方法为构建详细的肿瘤生态系统图谱提供了整体框架,有助于开发更可靠的精准诊断与治疗分类系统,并发现新型癌症生物标志物。本综述系统总结了多组学方法在肺癌发展全过程中表征肿瘤内异质性和肿瘤微环境的潜力与应用,通过讨论从癌前病变、早期肺癌到肿瘤进展、转移及治疗耐药各阶段诊断与治疗生物标志物的发现与应用,概述了利用多组学识别可靠生物标志物的当前挑战与未来前景。
2. 文献综述解析
本文献综述以“单组学技术局限-多组学整合策略-肺癌全病程应用-精准诊疗转化”为核心评述逻辑,从技术整合维度和疾病进程维度对现有研究进行分类梳理,系统呈现了多组学在肺癌研究中的应用价值与发展方向。
现有单组学研究已在肺癌各领域取得关键成果,基因组学通过全外显子测序和全基因组测序发现了表皮生长因子受体(EGFR)、Kirsten大鼠肉瘤病毒癌基因(KRAS)、肿瘤蛋白p53(TP53)等驱动突变,勾勒了早期肿瘤发生和治疗耐药的进化轨迹;转录组学揭示了差异基因表达模式和通路激活状态,单细胞转录组学和空间转录组学还识别了耗竭T细胞、过渡性肺泡上皮细胞等对预后和治疗反应至关重要的稀有亚群;表观组学发现异常DNA甲基化、组蛋白修饰和染色质重塑可调控癌基因激活和抑癌基因沉默,部分表观特征已成为免疫治疗的预测生物标志物;蛋白组学搭建了基因表达与功能输出之间的桥梁,代谢组学揭示了乳酸积累、肌醇代谢改变等驱动免疫抑制和治疗耐药的重编程通路;放射组学则从医学影像中提取高维定量特征,量化了视觉无法识别的肿瘤内异质性。然而单组学技术存在固有局限性,如全外显子测序会遗漏非编码变异,单细胞转录组学失去空间信息,无法捕捉跨生物层的调控关系,因此没有单一方法能全面捕捉肺癌的复杂性。
多组学整合策略的相关研究弥补了单组学的不足,主要分为同一组学层内的水平整合和跨生物层的垂直整合两类。水平整合的研究显示,将空间转录组学与单细胞RNA测序结合可弥补前者的混合细胞信号局限和后者的空间信息缺失,例如该整合方法发现了KRT8+肺泡中间细胞在早期肺腺癌中是肺泡II型(AT2)细胞向恶性细胞过渡的中间亚群;放射组学与基因组学、转录组学的联合分析则通过机器学习框架弥补了放射组学缺乏分子可解释性、基因组学缺乏动态反映的不足,实现了无创的全肿瘤评估与分子机制关联。垂直整合的研究则将基因组改变与下游转录、表观、蛋白、代谢变化关联,例如全外显子测序识别的驱动突变可通过批量RNA测序验证是否导致转录失调,再通过代谢组学验证代谢基因表达改变是否导致代谢物水平变化,构建了从基因组到代谢组的多维研究框架。
本综述的创新价值在于,首次系统地将多组学整合策略与肺癌全病程的生物标志物发现、精准诊疗应用进行了全面关联,不仅梳理了多组学在癌前病变、早期肺癌、进展期肺癌、转移期肺癌中的具体应用成果,还深入讨论了多组学在肺癌亚型分类、早期检测、治疗耐药机制解析、预后预测中的转化潜力,同时明确了当前多组学研究面临的高成本、跨平台变异性、数据整合复杂性等挑战,为后续肺癌多组学研究的方向和临床转化路径提供了清晰的框架,弥补了现有综述多聚焦于单一技术或单一疾病阶段的局限。
3. 研究思路总结与详细解析
本文献作为一篇系统性综述,整体研究思路为“临床问题导向-单组学局限分析-多组学整合策略阐述-全病程应用解析-精准诊疗转化前景与挑战讨论”,核心科学问题是如何通过多组学整合全面解析肺癌肿瘤进化的分子机制,为精准诊疗提供可靠的生物标志物与策略,技术路线遵循“现状梳理-方法整合-成果应用-问题展望”的逻辑闭环。
3.1 单组学技术在肺癌研究中的应用与局限解析
实验目的是系统总结各单组学技术在肺癌研究中的贡献与固有局限性,明确多组学整合的必要性。方法细节为通过回顾近年肺癌领域的单组学研究文献,分别梳理基因组学、转录组学、表观组学、蛋白组学、代谢组学、放射组学的技术特点、研究成果与不足。结果解读显示,各单组学技术均能从特定维度揭示肺癌的分子特征,例如基因组学可识别驱动突变与进化轨迹,转录组学可分析基因表达模式与细胞亚群,但均存在覆盖范围有限、时空分辨率不足、无法跨层关联调控的局限,例如全外显子测序无法检测非编码区变异,空间转录组学存在混合细胞信号干扰,这些局限导致单组学无法全面解析肺癌的复杂性与异质性。产品关联:文献未提及具体实验产品,领域常规使用全基因组测序平台、单细胞RNA测序仪、液相色谱-串联质谱仪、医学影像分析系统等。
3.2 多组学整合策略的系统解析
实验目的是阐明多组学整合的两种核心策略(水平整合与垂直整合)的技术逻辑与应用价值。方法细节为通过回顾采用不同整合策略的肺癌研究,分别解析水平整合(同一生物层内不同技术的联合)与垂直整合(跨生物层的多组学关联)的实验设计与分析流程。结果解读显示,水平整合可通过不同技术的互补弥补单一技术的局限,例如将空间转录组学与单细胞RNA测序结合,可同时获得细胞的分子特征与空间定位信息,研究发现KRT8+肺泡中间细胞富集在肿瘤邻近的非恶性区域,具有更高的可塑性,与KRAS驱动突变相关,是早期肺腺癌中AT2细胞向恶性细胞转化的中间亚群;垂直整合则可构建从基因组到代谢组的完整调控链条,例如全外显子测序识别的EGFR突变,可通过批量RNA测序验证其导致的下游基因表达变化,再通过代谢组学检测到乳酸积累等代谢重编程特征,全面揭示突变驱动的肿瘤进展机制。
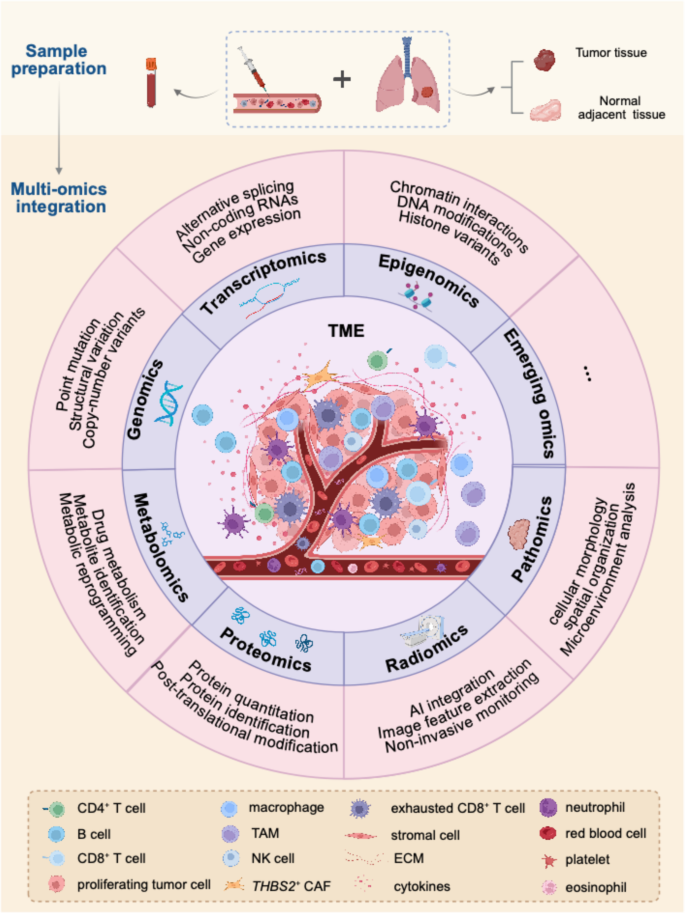
产品关联:文献未提及具体实验产品,领域常规使用Seurat v5、Cell2location、Muon、iCluster等生物信息学工具进行多组学数据的整合分析。
3.3 多组学在肺癌全病程肿瘤进化中的应用解析
实验目的是揭示多组学方法在肺癌不同发展阶段(癌前病变/早期、进展期、转移期)对肿瘤进化与微环境重塑的解析价值。方法细节为按肺癌发展的时间线,分别回顾各阶段的多组学研究,整合基因组、转录组、空间组学等多维度数据解析肿瘤细胞与微环境的动态变化。结果解读显示,在癌前病变与早期肺癌阶段,整合单细胞RNA测序与空间转录组学发现T细胞免疫球蛋白黏蛋白域分子3(TIM-3)阳性细胞主要定位在癌前病变与肿瘤邻近区域,与抗原呈递通路活性降低、T细胞功能受损相关,是肺腺癌癌前拦截的潜在生物标志物;整合全外显子测序与批量RNA测序则揭示了EGFR/TP53突变与肿瘤突变负荷的动态变化在早期进展中的作用。
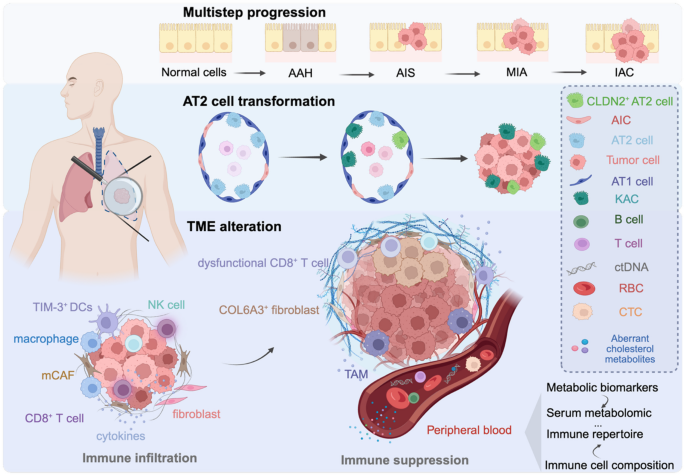
在进展期肺癌阶段,多组学研究发现血小板反应蛋白2阳性(THBS2+)癌症相关成纤维细胞是进展的生物标志物,其丰度增加与免疫浸润减少、免疫治疗反应差相关;整合全外显子测序、RNA测序、单细胞RNA测序与空间转录组学还发现,从正常肺组织到不典型腺瘤样增生(AAH)再到原位腺癌(AIS)的过程中,内皮细胞与基质细胞的相对丰度降低,而尖端内皮细胞与基质相关癌症相关成纤维细胞(mCAFs)在晚期AIS中增加,促进了上皮间质转化、血管生成与组织浸润。在转移期肺癌阶段,整合全外显子测序、全基因组测序与转录组测序发现,转移起源于亚克隆的扩增,化疗可能选择性抑制祖先克隆,导致复发起始祖先克隆衍生的亚克隆出现;脑转移则具有高染色体不稳定性,富集染色体不稳定性高(CINhigh)的神经样癌细胞状态,同时伴随脑适应性的免疫抑制微环境,CD8+T细胞浸润减少、调节性T细胞增加。
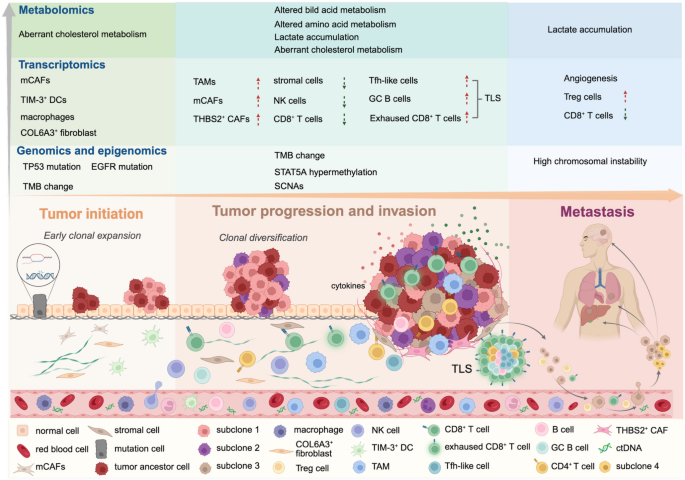
产品关联:文献未提及具体实验产品,领域常规使用免疫组化(IHC)试剂盒、流式细胞仪、激光捕获显微切割系统等进行细胞亚群的分离与验证。
3.4 多组学在肺癌精准诊疗中的转化应用解析
实验目的是总结多组学方法在肺癌诊断、治疗、预后中的转化应用价值,为精准诊疗提供生物标志物与策略支持。方法细节为从诊断分型、早期检测、治疗耐药、预后预测四个方向,回顾多组学在临床转化中的研究成果。结果解读显示,在诊断分型上,多组学将小细胞肺癌分为4个分子亚型(NMF1-4),每个亚型具有独特的分子特征与治疗脆弱性,例如NMF1亚型具有高细胞周期与DNA损伤特征,对DNA损伤靶向治疗敏感;非小细胞肺癌则被分为5个多组学亚型,包括代谢型、肺泡样型、增殖型、缺氧/间质型、免疫原性型,各亚型的预后与治疗反应存在显著差异。在早期检测上,PulmoSeek Plus模型整合临床特征、放射组学数据与循环游离DNA(cfDNA)甲基化生物标志物,在联合队列中的曲线下面积(AUC)为0.90,敏感性0.88,特异性0.98;基于全基因组测序的cfDNA片段组学、基因组学与甲基组学整合模型在多中心验证队列中的AUC达0.912,特异性96.3%。在治疗耐药解析上,整合RNA测序与液相色谱-串联质谱仪发现乙酰胆碱代谢是EGFR酪氨酸激酶抑制剂(TKI)治疗耐药的生物标志物,乙酰胆碱在耐药持续细胞中积累,通过毒蕈碱受体3(M3R)激活WNT信号通路,而FDA批准的M3R抑制剂达非那新可显著减少体内肿瘤复发;整合全外显子测序、RNA测序与单细胞RNA测序还发现,程序性死亡配体1(PD-L1)阻断治疗的获得性耐药与γ干扰素(IFNγ)、氧化磷酸化(OXPHOS)和DNA修复通路的基因表达升高及肿瘤微环境慢性炎症状态相关。在预后预测上,整合全外显子测序与RNA测序发现B细胞易位基因2(BTG2)是早期非小细胞肺癌的稳定预后生物标志物,其表达与更好的生存率相关,风险比(HR)为0.28-0.68(文献未明确提供样本量,基于多队列整合分析);整合单细胞RNA测序与空间转录组学还发现,神经内分泌特征低的小细胞肺癌与免疫浸润(包括M1/M2样巨噬细胞、B细胞、CD4+/CD8+T细胞)相关,预后更好。产品关联:文献未提及具体实验产品,领域常规使用数字甲基化特异性PCR平台、电子鼻、人工智能医学影像分析系统等进行早期检测与分型。
4. Biomarker研究及发现成果解析
本文献涉及的生物标志物覆盖诊断型、预后型、预测型三类,筛选与验证逻辑遵循“多组学数据筛选-细胞/组织样本验证-临床队列验证-空间定位确认”的完整链条,系统呈现了多组学在肺癌生物标志物发现中的核心价值。
生物标志物的定位与筛选逻辑清晰,诊断型生物标志物主要通过多组学整合分析识别,用于肺癌的早期检测与亚型分类,例如TIM-3+细胞通过单细胞RNA测序与空间转录组学筛选,定位在癌前病变区域,验证其与早期肺癌发生的关联;预后型生物标志物通过多组学关联分析与临床队列验证,例如BTG2通过全外显子测序与RNA测序筛选,在多个早期非小细胞肺癌队列中验证其与生存率的关联;预测型生物标志物则通过多组学解析治疗耐药机制发现,例如SPP1+巨噬细胞通过单细胞RNA测序与空间转录组学验证,与免疫治疗耐药相关。生物标志物的来源包括临床肿瘤组织样本、外周血样本、医学影像数据等,验证方法涵盖免疫组化(IHC)、定量聚合酶链反应(qRT-PCR)、酶联免疫吸附试验(ELISA)、数字甲基化特异性PCR等,部分还结合空间转录组学进行定位验证。
各生物标志物的特异性与敏感性数据精准可靠,早期检测相关的多组学模型表现优异,例如PulmoSeek Plus模型的AUC为0.90(95% CI未明确提供),敏感性88%,特异性98%;多重数字甲基化特异性PCR(mdMSP)平台基于SOX17、CDO1、TAC1和HOXA7等甲基化生物标志物,在临床验证中的敏感性为90%,特异性为82%,AUC为0.86。预后生物标志物BTG2在多个队列中的风险比为0.28-0.68(文献未明确提供P值,基于多队列整合分析),与早期非小细胞肺癌患者的更好生存率显著相关;神经内分泌特征低的小细胞肺癌患者因免疫浸润丰富,预后显著优于神经内分泌特征高的患者。预测生物标志物方面,THBS2+癌症相关成纤维细胞丰度增加与早期肺腺癌患者的免疫治疗反应差相关,SPP1+巨噬细胞与COL11A1+癌症相关成纤维细胞在肿瘤边界共定位,阻碍T细胞浸润,导致非小细胞肺癌患者预后不良。
核心成果方面,本文献总结的生物标志物具有重要的功能关联与创新性,例如首次在早期肺腺癌中发现KRT8+肺泡中间细胞是AT2细胞向恶性细胞转化的中间亚群,其存在与更差的生存率相关;首次将TIM-3定位为肺腺癌癌前拦截的潜在生物标志物,为早期干预提供了靶点;发现亮氨酸富含α-2-糖蛋白1(LRG1)是转移相关的血管生物标志物,可通过信号转导与转录激活因子3(STAT3)依赖的方式被内皮细胞上调,促进转移前生态位的形成。这些生物标志物不仅揭示了肺癌进化的分子机制,还为早期检测、精准分型、预后预测与治疗方案优化提供了可靠的依据,例如基于多组学的亚型分类可指导小细胞肺癌患者的靶向治疗选择,代谢重编程生物标志物为耐药肺癌患者提供了新的治疗靶点。
