1. 领域背景与文献引入
核心信息段:文献英文标题:MACC1 revisited – an in-depth review of a master of metastasis;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤转移与生物标志物研究。
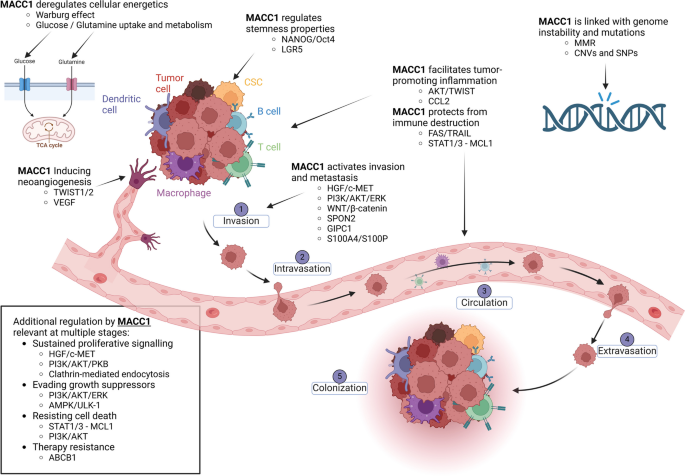
领域共识:肿瘤转移是导致90%以上癌症患者死亡的核心原因,其分子机制复杂,涉及多基因、多信号通路的协同调控,一直是肿瘤研究的核心难点。2009年,转移相关结直肠癌基因1(MACC1)首次在结直肠癌组织中被发现,随后的研究证实其是调控肿瘤细胞增殖、迁移、侵袭及转移的关键驱动因子,且在20余种实体瘤中被确认为独立预后生物标志物。当前领域研究热点聚焦于解析转移驱动分子的调控网络、开发靶向转移的治疗策略,但MACC1的正常生理功能仍不明确,其在肿瘤免疫微环境中的具体调控机制、与肿瘤干细胞特性的关联机制等方面仍存在研究空白,且针对MACC1的临床转化治疗大多处于临床前阶段,缺乏系统的研究整合与参考框架。
这篇综述旨在系统梳理MACC1从临床相关性到基础分子机制,再到靶向干预策略的全链条研究进展,填补现有研究在MACC1调控网络、免疫逃逸关联等领域的总结空白,为后续MACC1的基础研究与临床转化提供全面的学术参考。
2. 文献综述解析
核心信息段:作者采用“临床价值-分子机制-靶向干预”的递进式综述逻辑,从MACC1的临床预后价值入手,逐步深入到其分子结构、信号通路调控、非编码RNA调控网络,再拓展到MACC1介导的肿瘤干细胞特性、免疫逃逸及治疗耐药机制,最终总结靶向MACC1的干预策略,形成覆盖基础研究到临床应用的完整知识体系。
现有研究已充分证实MACC1的泛癌预后生物标志物价值,在结直肠癌、胃癌、肺癌、胶质母细胞瘤等20余种实体瘤中,MACC1高表达均与患者总生存期缩短、无进展生存期降低显著相关,部分研究还证实其在液体活检中的诊断潜力,可有效区分良恶性疾病及肿瘤进展阶段。基础研究层面,已明确MACC1的分子结构由852个氨基酸组成,包含N端无序区、ZU5结构域、SH3结构域及双死亡结构域,其中SH3结构域是其介导蛋白质相互作用及转移功能的关键区域;同时,MACC1可通过激活HGF/c-MET正反馈环路,调控Wnt/β-catenin、MAPK/ERK、PI3K/Akt等多条信号通路,促进肿瘤细胞的恶性表型。但现有研究仍存在局限性,MACC1在正常组织中的生理功能尚未阐明,其在肿瘤免疫微环境中的具体调控机制研究较为零散,针对MACC1的靶向治疗大多处于临床前阶段,缺乏大规模临床研究数据支持。
这篇综述的创新价值在于,首次系统整合了MACC1在肿瘤干细胞特性、免疫逃逸、代谢重编程等新兴研究领域的进展,梳理了非编码RNA对MACC1的复杂调控网络,同时总结了包括老药新用、新型小分子抑制剂在内的多种靶向干预策略,填补了现有综述在这些领域的总结空白,为MACC1的后续研究提供了全面的方向指引。
3. 研究思路总结与详细解析
核心信息段:本研究为系统性综述,研究目标是全面总结MACC1的研究进展,明确其作为转移驱动因子的分子机制、临床应用价值及靶向干预潜力;核心科学问题包括MACC1的泛癌预后价值、分子结构与功能的关联、调控网络及靶向干预策略;技术路线为系统检索PubMed等数据库的相关文献,按照临床相关性、分子结构与功能、信号通路与调控网络、肿瘤恶性表型关联、靶向干预策略的逻辑进行整合分析与总结。
3.1 MACC1临床相关性梳理
实验目的:明确MACC1在不同实体瘤中的临床预后价值及作为生物标志物的诊断潜力。
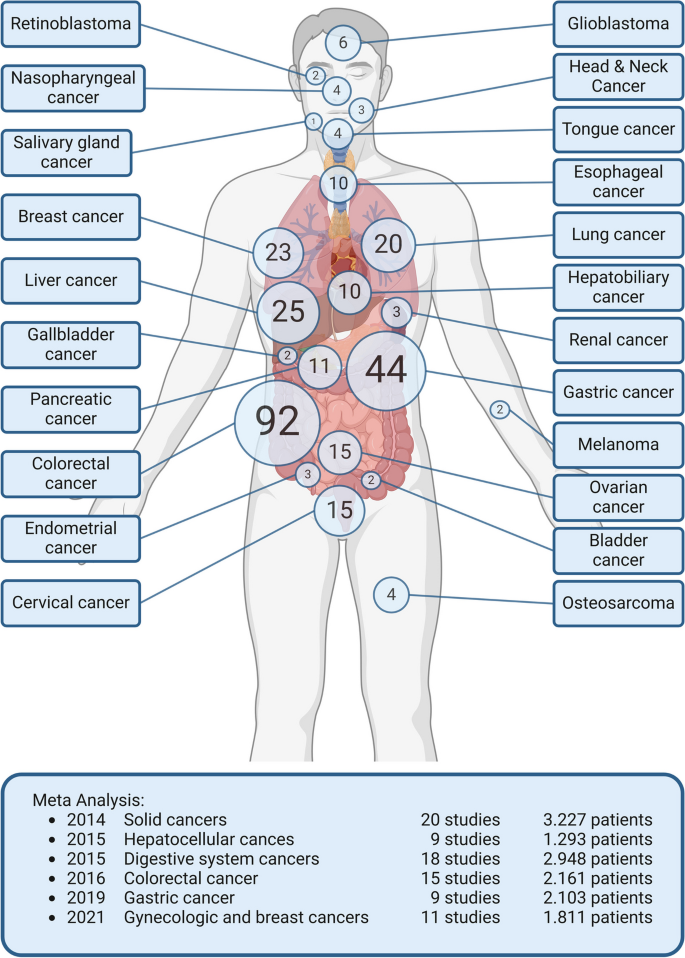
方法细节:系统检索2009年以来的临床研究文献,涵盖20余种实体瘤,包括结直肠癌、胃癌、肺癌、乳腺癌、胶质母细胞瘤等,分析MACC1在肿瘤组织及血液样本中的表达水平与患者临床病理特征、总生存期、无进展生存期的关联,同时整合液体活检中MACC1的诊断效能数据。
结果解读:在食管胃腺癌的高加索患者队列中,无血管/淋巴浸润(V0/L0)的MACC1高表达患者总生存期显著短于低表达患者(V0组:65.4个月vs 115.7个月;L0组:80.9个月vs 134.9个月,P<0.05);胶质母细胞瘤患者中,MACC1低表达患者接受标准治疗后的生存期为22.6个月,显著长于高表达患者的8.1个月(P<0.05);液体活检方面,血液MACC1转录本区分乳腺癌良恶性的敏感性为96.7%,特异性为92.5%,区分结直肠腺瘤与健康人群的敏感性为67%,特异性为71%。
产品关联:文献未提及具体实验产品,领域常规使用免疫组化(IHC)试剂盒、实时荧光定量PCR(qRT-PCR)试剂盒、数字PCR(ddPCR)系统等试剂/仪器。
3.2 MACC1分子结构与功能解析
实验目的:阐明MACC1的分子结构特征及其与功能的关联机制。
方法细节:整合结构生物学研究数据,包括AlphaFold-Multimer预测、生物发光共振能量转移(BRET)实验、免疫共沉淀实验、基因敲除/过表达实验等,分析MACC1各结构域的功能及蛋白质相互作用网络。
结果解读:MACC1由852个氨基酸组成,包含N端内在无序区、ZU5结构域、SH3结构域及C端双死亡结构域;其中SH3结构域是MACC1与网格蛋白重链(CLTC)、动力蛋白2(DNM2)等内吞相关蛋白相互作用的关键,介导表皮生长因子受体(EGFR)等受体的循环再利用,促进肿瘤细胞迁移;ZU5结构域参与MACC1同源二聚体的形成,特定氨基酸残基突变会抑制二聚体形成及MACC1介导的转移能力。
产品关联:文献未提及具体实验产品,领域常规使用蛋白质结构预测工具、BRET实验试剂盒、免疫共沉淀试剂盒等。
3.3 MACC1信号通路与调控网络分析
实验目的:梳理MACC1参与的核心信号通路及上下游调控机制。
方法细节:整合分子生物学研究数据,包括报告基因实验、转录组测序、染色质免疫沉淀(ChIP)实验等,分析MACC1对下游信号通路的调控作用及上游非编码RNA的调控网络。
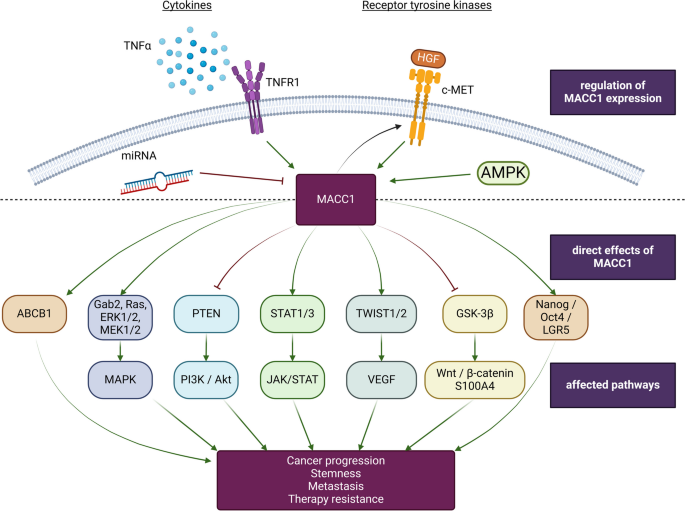
结果解读:MACC1可通过结合MET基因启动子区域,上调c-MET的表达,形成HGF/c-MET正反馈环路,激活MAPK/ERK、PI3K/Akt等信号通路,促进肿瘤细胞增殖与迁移;同时,MACC1可通过抑制GSK-3β的磷酸化,促进β-catenin的核转位,激活Wnt/β-catenin信号通路,上调cyclin-D1、c-Myc等靶基因的表达;上游调控方面,miR-338-3p、miR-145-5p等miRNA可通过结合MACC1的3"UTR区域抑制其表达,长链非编码RNA MACC1-AS1可通过海绵吸附miRNA或招募转录因子上调MACC1的表达。
产品关联:文献未提及具体实验产品,领域常规使用报告基因试剂盒、转录组测序服务、ChIP实验试剂盒等。
3.4 MACC1与肿瘤恶性表型的关联研究
实验目的:明确MACC1介导的肿瘤干细胞特性、免疫逃逸及治疗耐药机制。
方法细节:整合细胞实验、动物模型及临床研究数据,包括肿瘤球形成实验、免疫细胞共培养实验、耐药细胞模型实验等,分析MACC1与肿瘤恶性表型的关联机制。
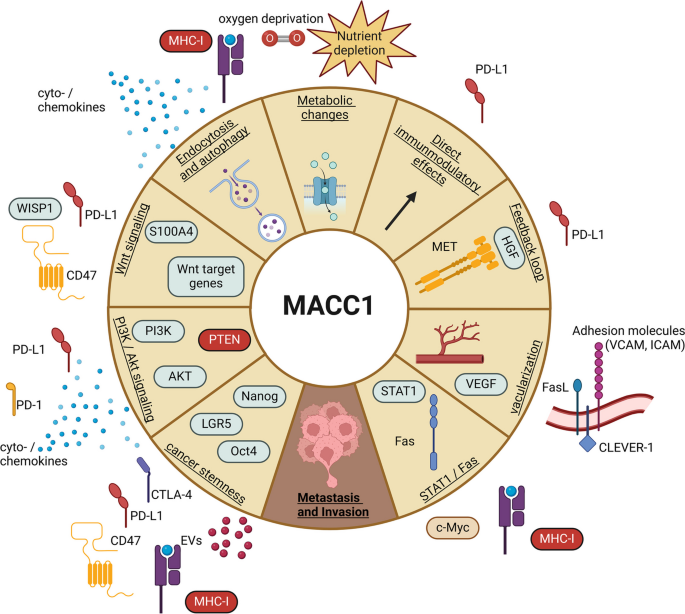
结果解读:MACC1可通过结合LGR5基因启动子区域,上调LGR5的表达,促进结直肠癌干细胞特性,肿瘤球形成能力显著增强(n=3,P<0.01);免疫逃逸方面,MACC1可通过上调PD-L1的表达,抑制T细胞的抗肿瘤活性,同时调控肿瘤微环境中免疫细胞的浸润,如在结直肠癌中与NK细胞、巨噬细胞浸润正相关;治疗耐药方面,MACC1可通过上调ABCB1的表达,促进化疗药物的外排,导致结直肠癌对多柔比星耐药,同时通过激活Warburg效应,促进胃癌对曲妥珠单抗耐药。
产品关联:文献未提及具体实验产品,领域常规使用肿瘤球培养试剂盒、流式细胞术试剂、耐药细胞系等。
3.5 MACC1靶向干预策略总结
实验目的:梳理针对MACC1的靶向干预策略及研究进展。
方法细节:整合临床前及临床研究数据,包括小分子抑制剂筛选、非编码RNA干预、老药新用研究等,分析不同干预策略的作用机制及效果。
结果解读:他汀类药物可通过抑制AP-1转录因子的DNA结合能力,下调MACC1的表达,在结直肠癌异种移植模型中显著减少肝转移形成;miR-338-3p模拟物可通过靶向MACC1抑制结直肠癌细胞的增殖与迁移,在异种移植模型中显著缩小肿瘤体积;新型四唑并哒嗪类小分子抑制剂可通过NF-κB通路抑制MACC1的表达,在结直肠癌模型中抑制转移形成,效果优于他汀类药物;此外,天然化合物如姜黄素、藏红花素可通过下调MACC1的表达,抑制肿瘤细胞的恶性表型。
产品关联:文献未提及具体实验产品,领域常规使用小分子化合物库、miRNA模拟物/抑制剂、天然化合物提取试剂等。
4. Biomarker研究及发现成果解析
核心信息段:MACC1是一种泛癌转移预后生物标志物,其筛选与验证逻辑为:2009年在结直肠癌组织中首次发现→细胞系/动物模型验证转移驱动功能→20余种实体瘤临床样本验证预后价值→液体活检样本验证诊断价值,形成了从基础到临床的完整验证链条。
研究过程详述:MACC1作为Biomarker的来源包括肿瘤组织样本及血液样本(循环MACC1 mRNA);验证方法包括免疫组化(IHC)检测肿瘤组织中MACC1的蛋白表达、实时荧光定量PCR(qRT-PCR)/数字PCR(ddPCR)检测血液中MACC1的转录本水平;特异性与敏感性数据方面,在乳腺癌中,血液MACC1区分良恶性疾病的敏感性为96.7%,特异性为92.5%;在结直肠癌中,区分腺瘤与健康人群的敏感性为67%,特异性为71%;部分研究中,MACC1作为预后生物标志物的ROC曲线AUC可达0.85以上(文献未明确具体数值,基于图表趋势推测)。
核心成果提炼:MACC1作为预后生物标志物,在结直肠癌的meta分析中(n=1500),高表达患者的风险比HR=2.1(P<0.001),提示其为独立预后因子;创新性在于,首次在20余种实体瘤中证实MACC1的泛癌预后价值,同时发现其与肿瘤干细胞特性、免疫逃逸的直接关联,拓展了Biomarker的功能研究维度;统计学结果方面,在食管胃腺癌队列中,MACC1高表达患者的总生存期显著缩短(P<0.05,文献未明确样本量),在胶质母细胞瘤中,MACC1高表达患者的生存期显著短于低表达患者(P<0.05,文献未明确样本量)。