1. 领域背景与文献引入
文献英文标题:Advances in CAR-T therapy for central nervous system tumors;发表期刊:Biomarker Research;影响因子:未公开;研究领域:中枢神经系统肿瘤免疫治疗(CAR-T疗法)
CAR-T疗法作为肿瘤免疫治疗的里程碑突破,自2017年FDA批准首个产品用于急性淋巴细胞白血病以来,在血液系统恶性肿瘤中取得了显著疗效,被认为是部分难治性肿瘤的潜在治愈手段。然而,其在实体瘤尤其是中枢神经系统肿瘤中的应用仍面临诸多挑战,血脑屏障的存在阻碍CAR-T细胞有效浸润肿瘤组织,肿瘤微环境的免疫抑制特性导致CAR-T细胞功能耗竭,抗原表达异质性引发治疗后肿瘤逃逸,以及治疗相关神经毒性风险高等问题,限制了CAR-T疗法在该领域的临床转化。当前研究热点聚焦于突破血脑屏障的递送策略、改造CAR-T细胞以克服免疫抑制、设计多靶点CAR-T解决抗原异质性等方向,但缺乏针对中枢神经系统不同类型肿瘤CAR-T治疗进展的系统性整合分析。在此背景下,该文献系统综述了胶质瘤、髓母细胞瘤、中枢神经系统淋巴造血肿瘤的CAR-T治疗研究进展,梳理了现有挑战并提出优化策略,为该领域的后续研究提供了全面参考。
2. 文献综述解析
该文献以中枢神经系统肿瘤CAR-T治疗的四大核心挑战为切入点,按肿瘤类型(胶质瘤、髓母细胞瘤、中枢神经系统淋巴造血肿瘤)和靶点类型分类,系统整合了临床前与临床研究数据,同时提出了五大优化策略,构建了涵盖“挑战-进展-优化”的完整综述框架。
现有研究已证实CAR-T疗法在血液肿瘤中的显著疗效,但在中枢神经系统肿瘤中,血脑屏障的物理与生化屏障作用导致系统递送的CAR-T细胞难以有效到达肿瘤部位,即使局部递送也面临肿瘤微环境中免疫抑制细胞(如肿瘤相关巨噬细胞、调节性T细胞、髓源性抑制细胞)的功能抑制,同时抗原表达异质性使得单一靶点CAR-T治疗后易出现肿瘤复发,治疗相关的神经毒性(如免疫效应细胞相关神经毒性综合征ICANS)发生率可达33%,严重时可危及生命。技术方法上,局部递送途径(脑室内、瘤内注射)可提高CAR-T细胞在脑内的浓度,多靶点CAR-T设计可降低抗原逃逸风险,但这些策略仍处于临床前或早期临床研究阶段,缺乏大规模临床数据支持。
与现有综述多聚焦单一肿瘤类型或靶点不同,该文献首次系统覆盖了中枢神经系统三大类肿瘤的CAR-T治疗进展,从靶点分子机制、临床前实验数据到临床研究结果进行了全面分析,同时创新性地提出了包括免疫检查点联合、细胞因子分泌改造、干细胞样T细胞应用、多靶点优化、递送途径改进在内的五大增强CAR-T疗效的策略,填补了该领域系统性综述的空白,为后续研究提供了清晰的方向指引。
3. 研究思路总结与详细解析
该文献的研究目标是系统梳理中枢神经系统肿瘤CAR-T治疗的研究进展、核心挑战及优化策略,核心科学问题是如何突破血脑屏障、免疫抑制微环境、抗原异质性及治疗毒性四大障碍,技术路线遵循“挑战分析→分肿瘤类型靶点研究进展综述→优化策略提出”的逻辑闭环,全面呈现了该领域的研究现状与未来方向。
3.1 中枢神经系统肿瘤CAR-T治疗挑战分析
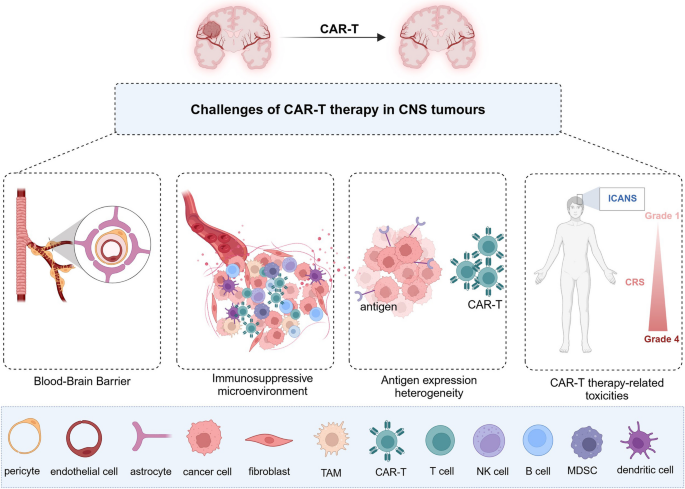
实验目的:明确CAR-T疗法应用于中枢神经系统肿瘤的核心障碍及机制;
方法细节:从血脑屏障的结构组成与功能特性、肿瘤免疫抑制微环境的细胞与分子组成、抗原表达异质性的产生机制、治疗相关毒性的发生机制四个层面,结合基础研究与临床数据进行系统性分析;
结果解读:血脑屏障由内皮细胞、基底膜和星形胶质细胞足突组成,紧密连接与外排蛋白(如P-糖蛋白)共同限制CAR-T细胞的脑内浸润;肿瘤免疫抑制微环境中,肿瘤相关巨噬细胞可极化为M2型促进免疫抑制,调节性T细胞通过分泌细胞因子抑制CAR-T细胞活性,髓源性抑制细胞可通过多种途径抑制免疫细胞功能;抗原异质性表现为同一肿瘤内不同细胞的抗原表达差异,以及治疗后抗原阴性肿瘤细胞的增殖;治疗毒性方面,细胞因子释放综合征(CRS)主要由单核细胞释放的细胞因子引发,而免疫效应细胞相关神经毒性综合征(ICANS)与脑脊液中高浓度细胞因子及血脑屏障破坏相关,严重病例的死亡率约为3%;
产品关联:文献未提及具体实验产品,领域常规使用流式细胞仪、免疫组化(IHC)试剂盒、实时荧光定量PCR(qRT-PCR)试剂、细胞因子检测ELISA试剂盒等。
3.2 胶质瘤CAR-T治疗靶点研究进展解析
实验目的:总结不同靶点CAR-T细胞在胶质瘤治疗中的临床前与临床研究效果及机制;
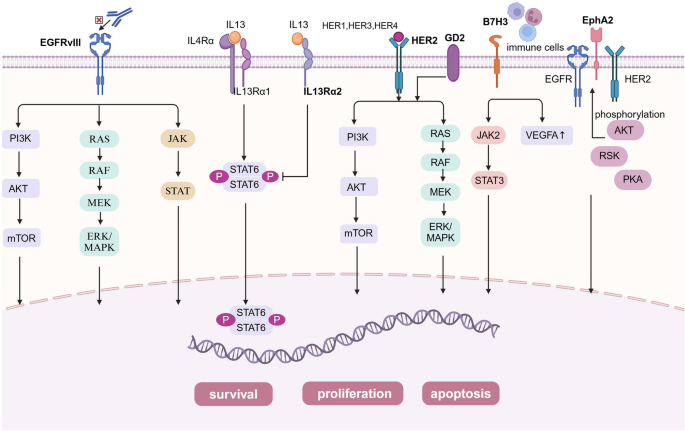
方法细节:针对EGFRvIII/EGFR、IL13Rα2、HER2、GD2、B7H3等关键靶点,分别梳理其在胶质瘤中的表达特性、信号通路机制,以及对应的CAR-T细胞临床前细胞系/动物模型实验结果和临床I/II期研究数据;
结果解读:EGFRvIII作为胶质瘤特异性突变抗原,其CAR-T细胞在I期临床中对10例复发胶质瘤患者的中位生存期约为8个月,但治疗后肿瘤微环境中免疫抑制分子(如IDO1、FoxP3)表达上调,引发适应性免疫逃逸;IL13Rα2 CAR-T细胞通过局部递送(瘤内或脑室内注射)在I期临床中使58例患者中的50%达到疾病稳定或改善,中位总生存期为8个月;HER2 CAR-T细胞在儿童中枢神经系统肿瘤的I期临床中展现良好耐受性,部分患者出现肿瘤缩小;GD2 CAR-T细胞在H3K27M突变弥漫中线胶质瘤的临床前模型中可显著清除肿瘤,I期临床中部分患者获得神经功能改善;B7H3 CAR-T细胞在胶质瘤和髓母细胞瘤中均显示出抗肿瘤活性,I期临床中部分患者实现肿瘤缩小甚至完全缓解;
产品关联:文献未提及具体实验产品,领域常规使用CAR-T细胞制备试剂盒、胶质瘤细胞系(如U251)、免疫缺陷动物模型(如NSG小鼠)等。
3.3 髓母细胞瘤与中枢神经系统淋巴造血肿瘤CAR-T研究解析
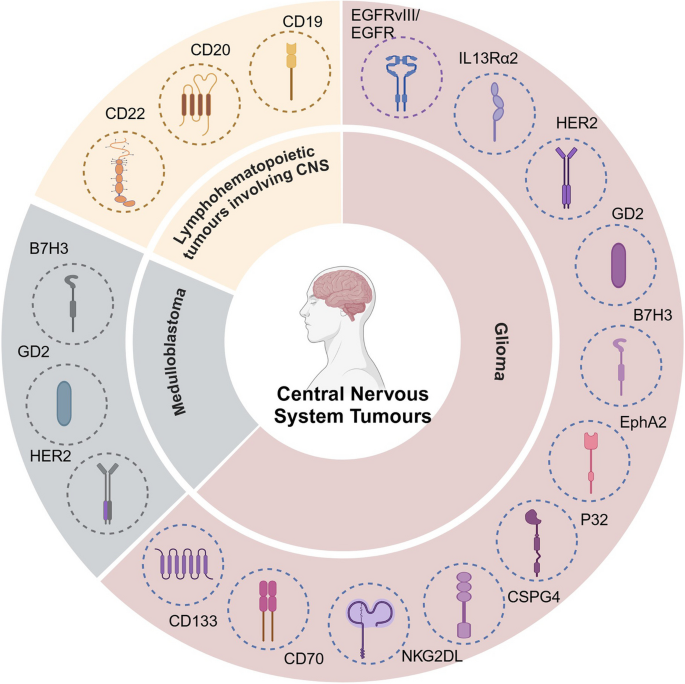
实验目的:分析CAR-T疗法在髓母细胞瘤及中枢神经系统淋巴造血肿瘤中的应用潜力与临床效果;
方法细节:髓母细胞瘤部分聚焦HER2、GD2、B7H3靶点的临床前研究数据,包括细胞系杀伤实验、动物模型肿瘤清除效果;中枢神经系统淋巴造血肿瘤部分总结CD19、CD20、CD22靶点CAR-T在中枢神经系统淋巴瘤、急性淋巴细胞白血病中的临床研究结果,包括缓解率、生存期及毒性反应;
结果解读:髓母细胞瘤中,B7H3 CAR-T细胞可穿透血脑屏障,在动物模型中显著延长小鼠生存期;GD2 CAR-T细胞在髓母细胞瘤临床前模型中显示出抗肿瘤活性,且通过引入自杀基因(诱导型caspase 9)提高了治疗安全性;中枢神经系统淋巴瘤中,CD19 CAR-T疗法的完全缓解率可达55.6%,中位无进展生存期为122天,但约56%的患者出现ICANS;CD19 CAR-T治疗中枢神经系统急性淋巴细胞白血病的中枢缓解率为85.4%,中位总生存期为16.0个月;
产品关联:文献未提及具体实验产品,领域常规使用流式细胞术检测CAR-T细胞在脑脊液中的浸润、ELISA检测细胞因子水平、MRI评估肿瘤大小变化等。
3.4 CAR-T治疗中枢神经系统肿瘤的优化策略解析
实验目的:提出增强CAR-T细胞在中枢神经系统肿瘤中疗效的可行策略;
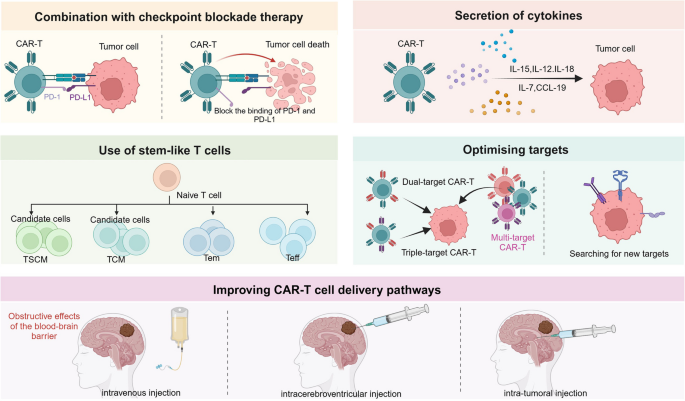
方法细节:从免疫检查点联合阻断、CAR-T细胞分泌细胞因子改造、采用干细胞样T细胞制备CAR-T、设计多靶点CAR-T、优化递送途径五个方面,结合现有研究数据分析各策略的作用机制与应用潜力;
结果解读:通过CRISPR-Cas9敲除CAR-T细胞的PD-1基因,可增强其在胶质瘤模型中的抗肿瘤活性;改造CAR-T细胞使其分泌IL-15、IL-18等细胞因子,可延长CAR-T细胞的体内存活时间并增强其功能;采用干细胞样T细胞(TSCM)制备的CAR-T细胞,可降低CRS和ICANS的发生率,同时提高抗肿瘤持久性;多靶点CAR-T细胞(如同时靶向EGFRvIII和IL13Rα2)可克服抗原异质性引发的治疗逃逸;局部递送途径(脑室内、瘤内注射)可显著提高CAR-T细胞在脑内的浓度,减少系统性毒性;
产品关联:文献未提及具体实验产品,领域常规使用CRISPR-Cas9基因编辑系统、细胞因子重组蛋白、干细胞分离试剂盒等。
4. Biomarker研究及发现成果解析
该文献涉及的Biomarker均为肿瘤表面抗原,属于CAR-T治疗的靶点型Biomarker,其筛选与验证遵循“数据库/临床样本筛选→临床前模型验证→临床研究验证”的完整逻辑链条,为中枢神经系统肿瘤CAR-T治疗的靶点选择提供了全面依据。
Biomarker定位:文献中涉及的Biomarker类型包括肿瘤特异性抗原(如EGFRvIII)和肿瘤相关抗原(如HER2、B7H3、GD2、CD19等),筛选逻辑为基于肿瘤组织与正常组织的表达差异,优先选择在肿瘤中高表达、正常组织中低表达或不表达的抗原,随后通过细胞系、动物模型验证其作为CAR-T靶点的可行性,最终进入临床研究评估治疗效果。
研究过程详述:这些Biomarker的来源包括胶质瘤、髓母细胞瘤、中枢神经系统淋巴瘤的临床组织样本、细胞培养上清及脑脊液样本;验证方法涵盖免疫组化(IHC)检测抗原在肿瘤组织中的表达水平、流式细胞术分析CAR-T细胞与肿瘤细胞的结合活性、细胞毒性实验检测CAR-T细胞对肿瘤细胞的杀伤能力,以及临床研究评估患者的治疗响应率;特异性与敏感性数据方面,EGFRvIII在胶质瘤中的特异性表达率约为30%,正常组织中几乎不表达;IL13Rα2在高级别胶质瘤中的表达率约为70%,正常脑组织中无表达;HER2在胶质瘤中的表达率约为80%,正常神经组织中表达受限;GD2在髓母细胞瘤中的表达率约为80%,正常组织中仅在特定神经细胞中低表达;B7H3在儿童中枢神经系统肿瘤中高表达,正常组织中表达极低;CD19在B细胞淋巴瘤中的阳性率约为90%,正常B细胞中表达但CAR-T治疗可通过淋巴清除预处理降低正常细胞损伤。
核心成果提炼:这些Biomarker作为CAR-T治疗靶点,在临床前研究中均展现出显著的抗肿瘤活性,部分已进入I/II期临床研究阶段;创新性在于首次系统总结了不同中枢神经系统肿瘤类型的潜在CAR-T靶点及其临床转化潜力,为后续靶点选择提供了参考;统计学结果方面,IL13Rα2 CAR-T局部递送的I期临床中,58例患者的中位总生存期为8个月(n=58);CD19 CAR-T治疗中枢神经系统淋巴瘤的完全缓解率为55.6%(n=9,P值未明确);GD2 CAR-T治疗H3K27M突变弥漫中线胶质瘤的I期临床中,部分患者的神经功能改善持续时间可达5个月(n=11)。
