1. 领域背景与文献引入
文献英文标题:Evaluation of two high-throughput proteomic technologies for plasma biomarker discovery in immunotherapy-treated melanoma patients;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤免疫治疗与液体活检生物标志物研究
肿瘤免疫治疗是恶性肿瘤治疗领域的革命性突破,2011年首个CTLA-4抑制剂伊匹木单抗获批用于黑色素瘤治疗,开启了免疫检查点抑制剂的临床应用时代;2014年PD-1抑制剂帕博利珠单抗、纳武利尤单抗相继获批,进一步提升了晚期黑色素瘤患者的生存率;随后免疫检查点抑制剂联合治疗方案的获批,将晚期黑色素瘤患者的客观响应率提升至约60%,但仍有40%的患者对治疗无响应,且联合治疗伴随严重的免疫相关毒性,因此亟需可靠的生物标志物用于患者分层与治疗监测。液体活检作为微创的检测手段,其循环蛋白、循环肿瘤DNA等生物标志物是当前研究热点,但现有高通量蛋白组学检测技术在抗体/适体特异性、检测动态范围等方面存在差异,导致生物标志物发现的一致性差,成为领域内未解决的核心问题。本研究针对这一空白,系统对比两种常用高通量蛋白组学技术在黑色素瘤免疫治疗患者血浆生物标志物发现中的性能,为技术选择与生物标志物验证提供实验依据。
2. 文献综述解析
作者按蛋白组学技术的原理将现有研究分为三类:基于质谱的无偏蛋白鉴定技术、基于微球的多重抗体检测技术、基于适体的蛋白结合检测技术。现有研究中,质谱技术能实现准确的蛋白鉴定,但受血浆中高丰度蛋白的干扰,检测灵敏度与通量受限;基于微球的多重检测技术通量高、操作简便,但存在抗体交叉反应、部分低丰度蛋白检测灵敏度不足的局限性;基于适体的检测技术具有更宽的动态范围,适体的化学稳定性优于抗体,但适体与靶蛋白的结合特异性仍需进一步验证,且临床样本中的应用数据有限。作者指出,当前领域内缺乏直接对比这两种常用技术在免疫治疗患者临床样本中性能的研究,导致生物标志物发现的结果难以重复,因此本研究的创新价值在于首次在黑色素瘤免疫治疗队列中,系统评估两种技术的蛋白定量一致性、检测灵敏度及生物标志物筛选能力,为临床生物标志物研究的技术选择提供直接实验证据。
3. 研究思路总结与详细解析
本研究的整体目标是对比基于微球的Eve Technologies Discovery检测与基于适体的SomaLogic SOMAscan检测在黑色素瘤免疫治疗患者血浆生物标志物发现中的性能,核心科学问题是不同蛋白检测技术的特异性、动态范围差异对临床样本蛋白定量及生物标志物筛选的影响,技术路线遵循“临床样本收集→两种高通量技术平行检测→靶向验证实验→多维度数据分析→结论总结”的闭环逻辑。
3.1 临床样本收集与治疗响应分组
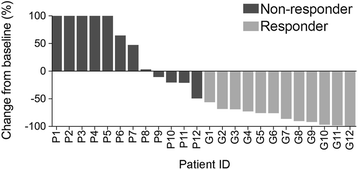
实验目的是获取标准化的黑色素瘤免疫治疗患者血浆样本,并明确患者的治疗响应状态,为后续技术性能评估提供临床背景。方法细节为收集24例2014年7月至2015年12月在Westmead Hospital和Melanoma Institute Australia接受帕博利珠单抗联合伊匹木单抗治疗的转移性黑色素瘤患者的外周血样本,分别在治疗前(基线)和治疗早期(1-6周)采集,经离心分离血浆后分装保存于-80℃;在治疗12周后,根据实体肿瘤疗效评价标准(RECIST 1.1)将患者分为响应组(完全响应/部分响应,n=12)和非响应组(疾病稳定/疾病进展,n=12),同时收集患者的临床病理特征数据。结果解读显示两组患者在年龄、性别分布上无显著差异,但基线乳酸脱氢酶(LDH)水平和美国癌症联合委员会(AJCC)分期存在显著差异,响应组患者的LDH水平更趋于正常、AJCC分期更早,符合已知的免疫治疗响应预后因素。
实验所用关键产品:BD Vacutainer Blood Collection Tubes。
3.2 两种高通量蛋白组学技术平行检测
实验目的是系统对比微球检测与适体检测在临床血浆样本中的蛋白检测范围、定量一致性及技术性能差异。方法细节为采用Eve Technologies 65-plex Discovery微球检测(基于Luminex平台,覆盖65种细胞因子/趋化因子)和SomaLogic SOMAscan适体检测(覆盖1310种蛋白)对所有47份血浆样本(23份基线、24份治疗早期)进行检测;Discovery检测中,血浆样本与预包被抗体的微球孵育后,加入生物素化检测抗体和PE标记的链霉亲和素,通过Bio-Rad BioPlex 200分析仪检测荧光信号;SOMAscan检测中,血浆样本与SOMAmer适体孵育后,对结合的适体进行生物素化,经链霉亲和素微球捕获后,通过微阵列芯片检测荧光信号。结果解读显示Discovery检测的荧光强度范围为46.26至13069相对荧光单位(RFU),中位值为184.7 RFU,但有15种细胞因子在75%以上的样本中荧光信号低于标准曲线,无法计算绝对浓度;SOMAscan检测的荧光强度范围为45.33至238857 RFU,中位值为1254 RFU,动态范围达8个数量级。两种技术共覆盖49种相同蛋白,其荧光强度的整体相关性较弱(Spearman相关系数r=0.3165,P=0.0267),仅12种蛋白的检测结果存在显著正相关;进一步分析显示,相关性差的蛋白要么在Discovery检测中荧光强度较低(P<0.01),要么在SOMAscan检测中荧光强度范围受限。
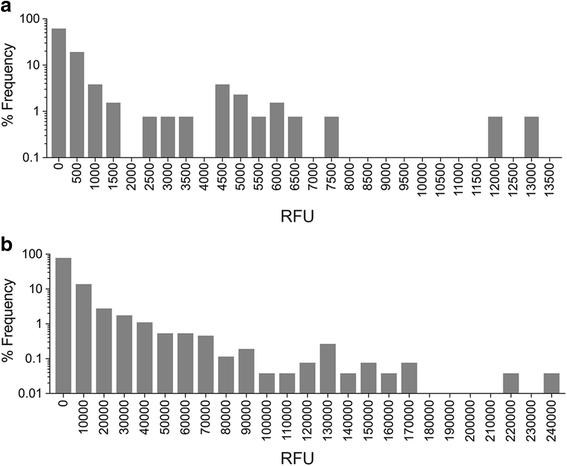
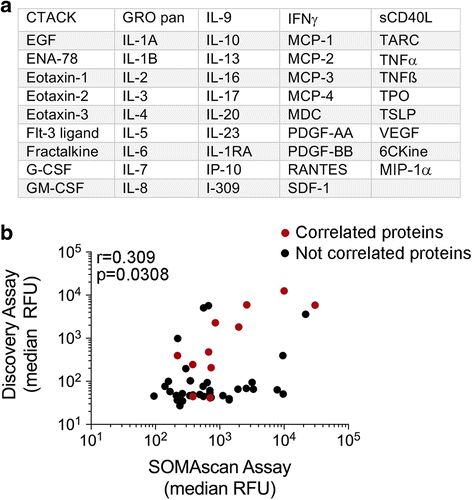
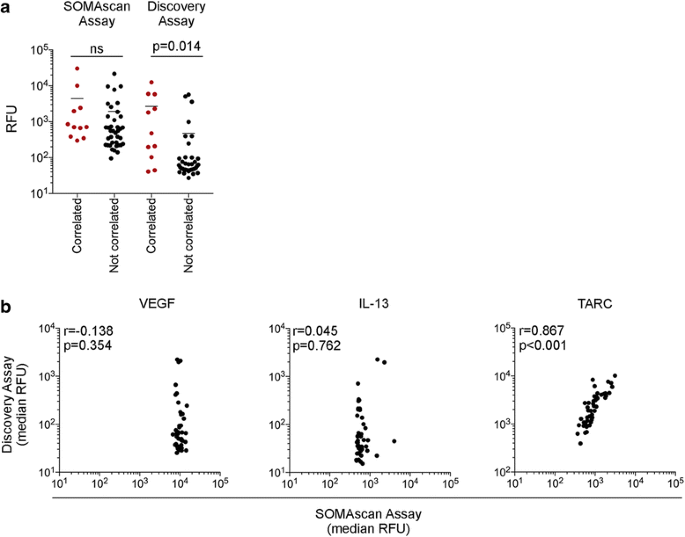
实验所用关键产品:Eve Technologies Discovery assay(货号HD65)、SomaLogic SOMAscan assay、Bio-Rad BioPlex 200 bead analyzer。
3.3 微球检测技术的验证与相关性分析
实验目的是验证基于微球的检测技术内部的一致性,进一步明确不同技术间差异的来源。方法细节为选取IL-1α、IL-1RA、TNFα、IL-6四种蛋白,采用Millipore Milliplex微球检测(同样基于Luminex平台)对28份血浆样本进行检测,对比三种技术的荧光强度及绝对浓度的相关性。结果解读显示Milliplex与Discovery检测的荧光强度高度相关,TNFα在三种技术中的检测结果均存在显著正相关,而IL-1RA、IL-1α、IL-6仅在两种微球检测技术中存在显著正相关,与SOMAscan检测的相关性较差;在绝对浓度层面,TNFα、IL-1RA、IL-6在两种微球检测中的结果显著相关,而IL-1α因在Milliplex检测中多数样本信号低于标准曲线,无法计算绝对浓度,导致相关性无统计学意义。
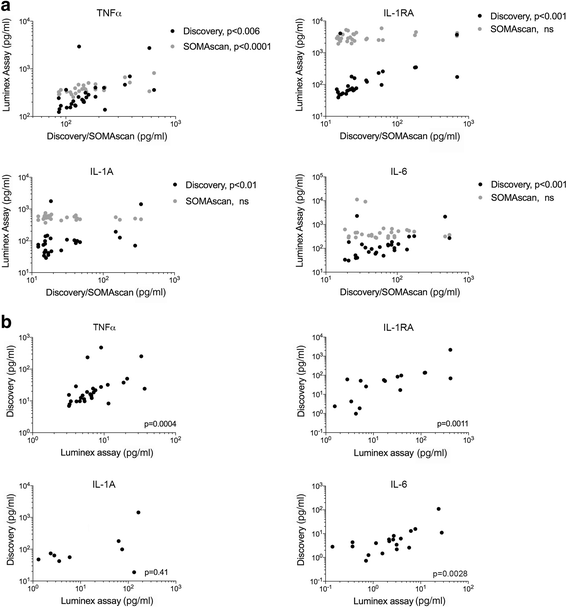
实验所用关键产品:Millipore Milliplex assay(货号HCYTOMAG-60 K)、Eppendorf epMotion 5075 robotic liquid handling workstation、Bio-Rad BioPlex Systems 100。
3.4 免疫治疗响应相关差异蛋白筛选
实验目的是对比两种技术在筛选免疫治疗响应相关血浆生物标志物中的能力。方法细节为采用limmaGP软件分析响应组与非响应组在基线和治疗早期样本中的蛋白表达差异,并通过主成分分析(PCA)验证差异蛋白的分组能力。结果解读显示SOMAscan检测在治疗早期样本中筛选出178种差异表达蛋白(q<0.25,P<0.05),其中175种在非响应组中的表达水平更高,PCA分析显示这些差异蛋白能有效区分响应组与非响应组;而Discovery检测在基线和治疗早期样本中均未发现显著差异的蛋白;此外,SOMAscan检测还发现32种在治疗后非响应组中上调的蛋白,PCA分析显示这些蛋白也能部分区分两组,而Discovery检测未发现相关差异。
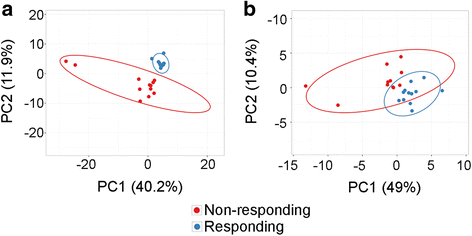
4. Biomarker研究及发现成果
本研究未最终鉴定出经独立验证的黑色素瘤免疫治疗响应特异性生物标志物,而是聚焦于生物标志物发现技术的性能评估,明确了两种常用高通量蛋白组学技术在临床样本应用中的局限性,为后续生物标志物研究的技术选择提供关键参考。
Biomarker定位:本研究通过SOMAscan检测筛选出178种治疗早期差异表达蛋白及32种治疗后上调蛋白,属于循环蛋白类潜在生物标志物,筛选逻辑为“免疫治疗患者血浆样本采集→高通量蛋白组学检测→差异表达分析→PCA验证”,但所有候选生物标志物均未经过独立临床队列的验证,其临床应用价值仍需进一步确认。
研究过程详述:候选生物标志物的来源为24例转移性黑色素瘤患者的基线和治疗早期血浆样本,验证方法仅采用Milliplex微球技术对4种蛋白进行了技术重复性验证,未对候选生物标志物的临床特异性与敏感性进行评估;SOMAscan筛选出的差异蛋白中,未提供具体的ROC曲线、敏感性、特异性等临床性能数据,仅通过PCA分析显示其具有分组能力,样本量为n=24(响应组n=12,非响应组n=12)。
核心成果提炼:本研究的核心成果并非鉴定新的生物标志物,而是明确了两种常用高通量蛋白组学技术在临床样本检测中的关键局限性:基于微球的Discovery检测存在部分低丰度蛋白检测灵敏度不足的问题,导致无法计算绝对浓度;基于适体的SOMAscan检测虽然动态范围更广,但与微球技术的蛋白定量一致性差,主要源于适体与抗体的结合特异性差异;SOMAscan筛选出的潜在生物标志物需通过更特异性的检测技术及更大样本量的临床队列进行验证。本研究无统计学数据支持候选生物标志物的临床诊断或预后价值,仅为生物标志物发现技术的优化提供了实验依据。
