1. 领域背景与文献引入
文献英文标题:Tolerability to romidepsin in patients with relapsed/refractory T-cell lymphoma;发表期刊:Biomarker Research;影响因子:未公开;研究领域:淋巴瘤(T细胞淋巴瘤)治疗与安全性研究。
领域共识:T细胞淋巴瘤是一类异质性极高的非霍奇金淋巴瘤,主要分为皮肤T细胞淋巴瘤(CTCL)和外周T细胞淋巴瘤(PTCL)两大亚型。CTCL多呈惰性进展,但晚期患者预后极差,常伴随难以耐受的皮肤瘙痒、反复感染等并发症;PTCL则为侵袭性淋巴瘤,疾病进展迅速,复发难治性患者的5年生存率不足30%。2009年,美国FDA批准1类选择性组蛋白去乙酰化酶(HDAC)抑制剂罗米地辛用于既往接受过至少一种系统治疗的CTCL患者,2011年进一步获批用于PTCL患者,成为复发难治性T细胞淋巴瘤的重要治疗选择。然而,既往研究虽已证实罗米地辛的临床疗效,但对PTCL与CTCL患者接受罗米地辛治疗的不良事件谱差异、早期治疗中断的核心原因,以及患者基线特征对耐受性的影响缺乏系统分析,这一研究空白限制了临床对高风险患者的精准管理。本研究旨在通过汇总两项关键注册试验的安全性数据,明确不同亚型患者的耐受性差异,为临床优化罗米地辛的治疗策略提供依据。
2. 文献综述解析
作者通过时间线与研究阶段的维度,系统回顾了罗米地辛在T细胞淋巴瘤中的研发历程与前期研究成果,明确了现有研究的价值与局限性。
前期研究显示,美国国家癌症研究所(NCI)的1期试验首次证实罗米地辛在T细胞淋巴瘤中的抗肿瘤活性,随后的2期试验进一步验证了其疗效。两项关键注册试验中,GPI-04-0001研究针对复发难治性CTCL患者,客观缓解率(ORR)达34%,其中完全缓解率6%,中位缓解持续时间15个月;GPI-06-0002研究针对复发难治性PTCL患者,ORR为25%,其中确认/未确认完全缓解率15%,中位缓解持续时间28个月,显示罗米地辛可为两类患者带来持久临床获益。安全性方面,既往研究仅提及常见不良事件包括胃肠道反应、乏力等,但未系统对比PTCL与CTCL患者的不良事件严重程度、时间分布差异,也未深入分析患者基线特征(如预处理强度、是否接受过单抗治疗)对耐受性的影响,无法为临床识别高风险患者、制定个体化监测方案提供足够依据。本研究的创新价值在于首次系统对比了复发难治性PTCL与CTCL患者接受罗米地辛治疗的不良事件谱差异,明确了早期治疗中断的核心原因,以及预处理史对毒性反应的影响,填补了既往研究在安全性精细化分析方面的空白。
3. 研究思路总结与详细解析
本研究的核心目标是系统对比复发难治性PTCL与CTCL患者接受罗米地辛治疗的不良事件特征,分析早期治疗中断的原因及患者基线特征对耐受性的影响,为临床优化治疗管理提供循证依据。研究采用回顾性汇总分析设计,纳入两项关键注册试验中所有接受至少一剂罗米地辛的患者,通过整合安全性数据,从不良事件发生率、严重程度、时间分布、患者亚组差异等维度展开分析,形成“数据整合→特征对比→亚组分析→临床建议”的完整逻辑链条。
3.1 研究对象与治疗方案解析
实验目的:明确研究纳入人群的基线特征与统一的治疗方案,为安全性分析提供标准化基础。方法细节:纳入GPI-04-0001(CTCL)与GPI-06-0002(PTCL)两项试验中所有接受≥1剂罗米地辛的患者,治疗方案为罗米地辛14mg/m²,4小时静脉输注,每28天周期的第1、8、15天给药,最多治疗6周期,疾病稳定的患者可延长治疗直至疾病进展或满足其他停药标准。结果解读:两组患者均为复发难治性晚期病例,PTCL患者中位接受2线既往系统治疗,CTCL患者中位接受3线,超过70%的患者处于疾病晚期(PTCL为III-IV期,CTCL为IIB-IVA期),且多数患者接受过既往化疗,为后续安全性分析的可比性奠定了基础。产品关联:文献未提及具体实验产品,领域常规使用的试剂包括用于不良事件评估的《常见不良事件评价标准(CTCAE)》,以及血常规、心电图检测等临床常规设备。
3.2 罗米地辛治疗暴露与早期停药分析
实验目的:分析两类患者的治疗持续时间与早期停药原因,明确罗米地辛的实际临床暴露情况。方法细节:统计患者的中位治疗时间、早期(1-2周期)停药比例及原因,分析完成至少6周期治疗的患者比例。结果解读:PTCL患者的中位治疗时间为1.4个月,CTCL患者为3.5个月;PTCL患者中55%在1-2周期内停药,CTCL患者中27%早期停药,早期停药的主要原因包括疾病进展、不良事件、知情同意撤回等,其中因不良事件停药的PTCL患者有16例,CTCL患者有11例。尽管早期停药比例较高,仍有28%的PTCL患者和36%的CTCL患者完成了至少6周期的治疗,提示部分患者可耐受长期治疗。
3.3 常见不良事件发生率与严重程度分析
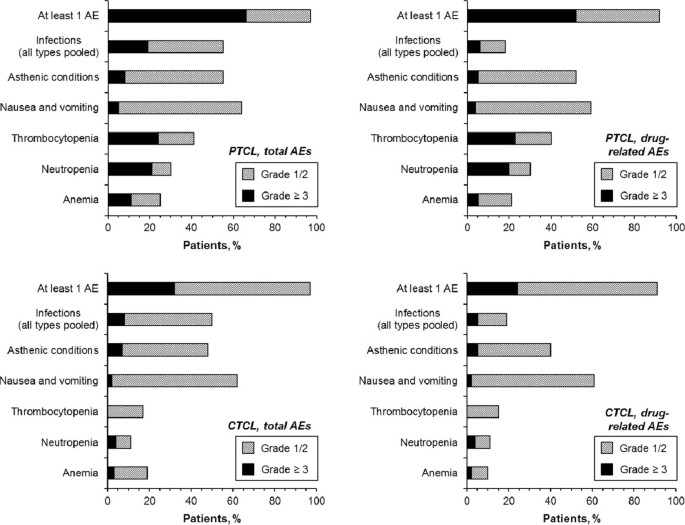
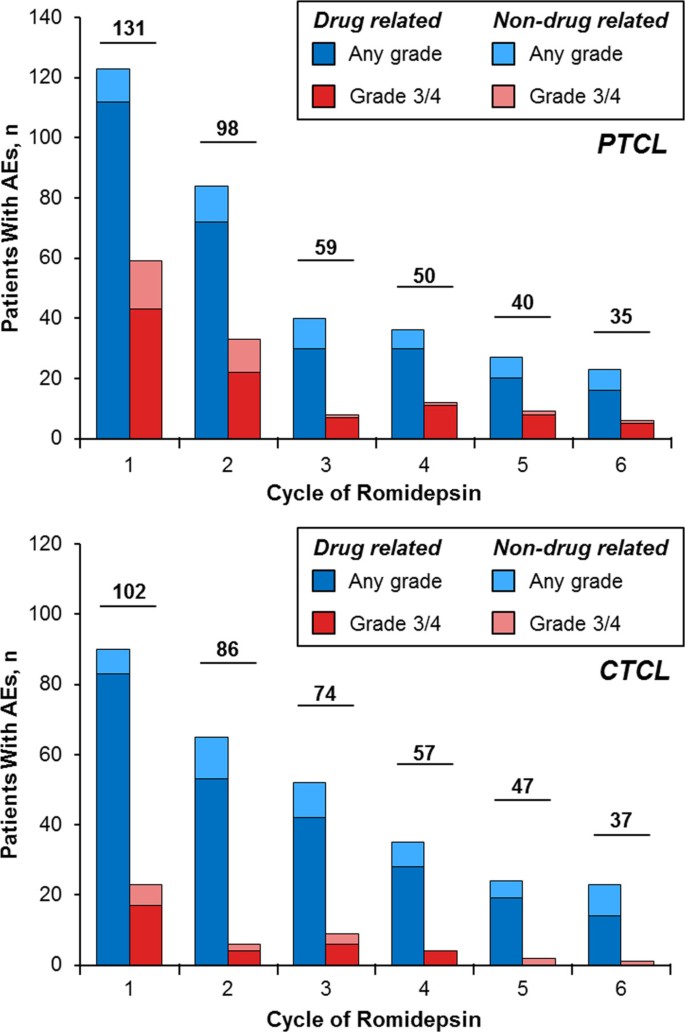
实验目的:对比PTCL与CTCL患者的不良事件谱差异,明确两类患者的耐受性特征。方法细节:统计所有等级及3级以上不良事件的发生率,重点分析血液学毒性、胃肠道反应、感染等常见不良事件的差异。结果解读:两类患者的常见不良事件谱相似,恶心/呕吐是最常见的不良事件及药物相关不良事件(所有等级)。但PTCL患者的3级以上不良事件发生率更高(66% vs 52%),血液学毒性更为显著,其中3级以上血小板减少、中性粒细胞减少、贫血的发生率分别为24%、21%、11%,远高于CTCL患者的0%、4%、3%;PTCL患者的3级以上感染发生率为19%,也显著高于CTCL患者的8%。此外,两类患者的3级以上不良事件及因不良事件停药的高峰均出现在治疗的1-2周期。
3.4 患者基线特征对毒性反应的影响分析
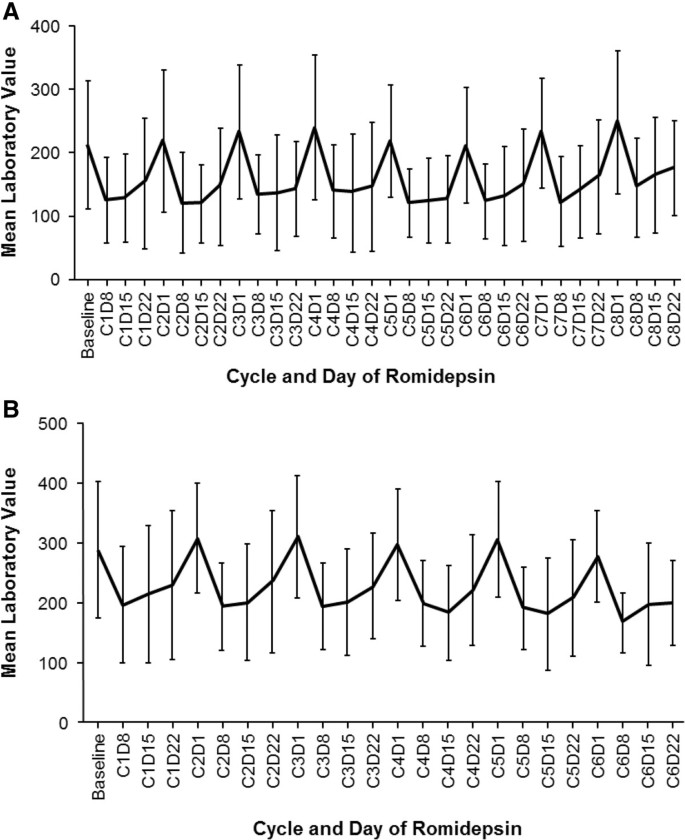
实验目的:明确患者基线特征(如PTCL亚型、预处理史、是否接受过单抗治疗)对罗米地辛耐受性的影响,识别高风险人群。方法细节:按PTCL亚型、年龄、国际预后指数(IPI)评分、既往治疗类型与次数、骨髓受累情况进行亚组分析,对比不同亚组的3级以上治疗相关不良事件发生率,采用Fisher精确检验进行统计学验证。结果解读:PTCL患者中,接受过既往单抗治疗(主要为阿仑单抗或利妥昔单抗)的患者,3级以上感染(20% vs 4%)和中性粒细胞减少(50% vs 14%)的发生率显著更高;接受≥3线既往系统治疗的患者,3级以上血小板减少的发生率为38%,显著高于接受<3线治疗的患者(15%,P<0.05)。此外,多数患者的血小板计数在治疗周期间可恢复,与罗米地辛诱导血小板减少的机制(巨核细胞出芽缺陷而非直接骨髓抑制)一致。
3.5 严重不良事件与治疗调整分析
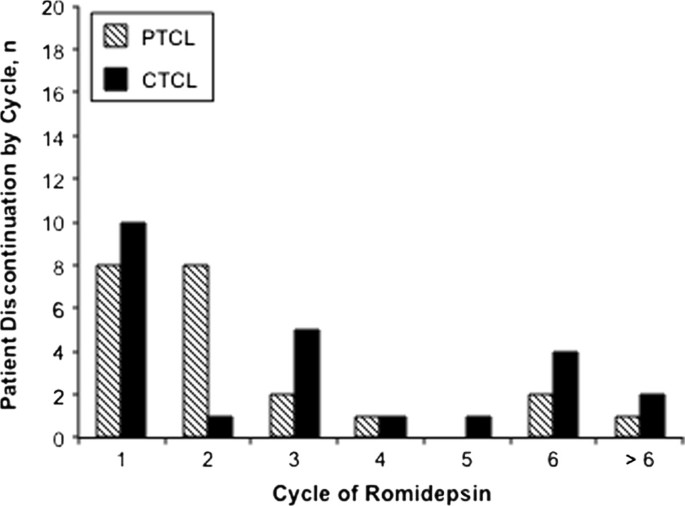
实验目的:分析严重不良事件的类型、治疗调整情况及因不良事件停药的时间分布,为临床管理提供具体建议。方法细节:统计严重不良事件的发生率、住院原因,剂量中断与减少的比例及原因,分析因不良事件停药的周期分布。结果解读:感染是两类患者最常见的严重不良事件及住院原因。PTCL患者中47%出现剂量中断,11%出现剂量减少,主要原因包括血小板减少(18%)、感染(12%)、中性粒细胞减少(11%);CTCL患者中34%出现剂量中断,14%出现剂量减少,主要原因包括感染(13%)、中性粒细胞减少(3%)、乏力(3%)。因不良事件停药的患者中,PTCL患者的多数停药发生在1-2周期,CTCL患者中42%的停药发生在第1周期,提示早期密切监测的重要性。
4. Biomarker研究及发现成果解析
本研究未涉及分子生物标志物的筛选与验证,但通过亚组分析明确了可预测罗米地辛耐受性的临床特征标志物,为临床识别高风险患者提供了循证依据。
Biomarker定位:研究聚焦于临床特征标志物,通过患者基线特征与毒性反应的关联分析,筛选出可预测罗米地辛耐受性的因素,验证逻辑为“基线特征收集→亚组毒性对比→统计学验证”。研究过程详述:标志物来源为患者的基线临床数据,包括疾病亚型、既往治疗史(单抗治疗史、预处理线数),验证方法为亚组不良事件发生率对比,采用Fisher精确检验进行统计学分析。其中,PTCL亚型可作为严重血液学毒性与感染的预测标志物,PTCL患者的3级以上血液学毒性发生率显著高于CTCL患者;接受过既往单抗治疗的PTCL患者,3级以上感染发生率为20%(n=18),显著高于未接受单抗治疗的患者(4%,n=112,P<0.05);接受≥3线既往治疗的PTCL患者,3级以上血小板减少发生率为38%(n=26),显著高于接受<3线治疗的患者(15%,n=104,P<0.05)。核心成果提炼:这些临床特征标志物可有效预测罗米地辛的耐受性,其中PTCL亚型提示更高的严重血液学毒性与感染风险,既往单抗治疗史与多线预处理提示PTCL患者更高的感染与血小板减少风险,为临床制定个体化监测方案提供了依据。推测:针对这些高风险患者,可考虑在治疗早期加强血常规、感染指标监测,或采用更低的初始剂量(10或12mg/m²),以降低不良事件发生率,提高治疗依从性。
