1. 领域背景与文献引入
文献英文标题:Analyzing PKC Gamma (+ 19,506 A/G) polymorphism as a promising genetic marker for HCV-induced hepatocellular carcinoma;发表期刊:Biomarker Research;影响因子:未公开;研究领域:病毒诱导肝细胞癌的遗传标志物研究
肝细胞癌(HCC)是全球范围内的重大健康问题,丙型肝炎病毒(HCV)感染是诱发HCC的主要危险因素之一。领域共识:HCC预后较差的核心原因是早期诊断困难,传统化疗手段对晚期患者的疗效有限。目前全基因组关联研究(GWAS)已鉴定出IL-28B、PNPLA3等多个与HCC相关的单核苷酸多态性(SNP),但现有生物标志物仍无法满足早期精准诊断的临床需求。蛋白激酶Cγ(PKCγ)属于经典PKC亚类,已被证实参与多种肿瘤的发生发展过程,但关于其SNP与HCV诱导HCC的关联研究尚未见报道,这一研究空白凸显了本研究的学术必要性,旨在探索PKCγ的错义SNP与HCV诱导HCC的关联,为疾病早期诊断提供新的遗传标志物。
2. 文献综述解析
作者按“遗传变异与肿瘤关联研究现状→PKC家族与肿瘤的研究进展→PKCγ SNP研究空白”的逻辑维度梳理领域研究。现有研究的支持观点包括SNP作为遗传标志物在肿瘤易感性评估、预后判断中的重要价值,例如GWAS已成功鉴定多个与HCC发病相关的SNP位点;技术方法优势在于生物信息学工具可高效筛选致病性SNP,结合分子动力学模拟能精准解析变异对蛋白结构与功能的影响;但局限性在于多数研究仅停留在生物信息学预测层面,缺乏大样本临床验证数据,且针对PKCγ SNP与HCV诱导HCC的关联研究完全处于空白状态。本研究的创新价值在于首次聚焦PKCγ的错义SNP,通过“生物信息学筛选-分子动力学模拟-临床样本验证”的完整链条,明确了rs1331262028这一SNP与HCV诱导HCC的关联,填补了该领域的研究空白,为HCC早期诊断提供了新的潜在遗传标志物。
3. 研究思路总结与详细解析
本研究的核心目标是鉴定PKCγ中与HCV诱导HCC相关的致病性错义SNP,并验证其作为遗传标志物的临床潜力;核心科学问题是PKCγ的SNP如何通过影响蛋白结构与功能参与HCV诱导HCC的发生过程;技术路线遵循“生物信息学筛选致病性SNP→分子动力学模拟解析结构变化→临床样本验证关联及功能”的闭环逻辑。
3.1 致病性错义SNP的生物信息学筛选
实验目的是从PKCγ的所有错义SNP中筛选出具有致病性的变异位点。方法细节为从ENSEMBL基因组浏览器获取PKCγ的蛋白序列及错义SNP数据集,使用PredictSNP2、CADD、DANN、FATHMM、FunSeq2和GWAVA共6种生物信息学工具联合筛选,保留被所有工具预测为致病性的SNP,同时通过InterPro分析PKCγ的蛋白结构域,定位位于功能关键域的SNP位点。结果解读显示,共检索到429个PKCγ的错义SNP,最终筛选出5个被所有工具预测为致病性的位点,其中rs1331262028(K359R)因位于PKCγ的激酶催化域(该域的SNP被证实与肿瘤发生风险升高相关)被选为核心研究位点。
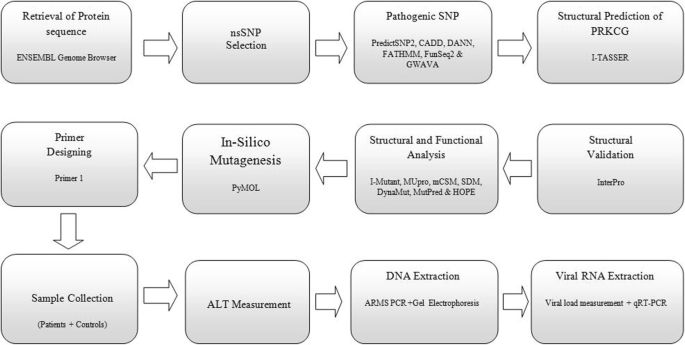
文献未提及具体实验产品,领域常规使用生物信息学在线分析工具及蛋白结构预测软件。
3.2 变异对蛋白结构与稳定性的模拟分析
实验目的是解析rs1331262028变异对PKCγ蛋白结构、功能及稳定性的影响。方法细节为使用I-TASSER预测PKCγ的三维结构,通过I-Mutant、MUpro、mCSM、SDM和DynaMut共5种工具分析蛋白稳定性变化,利用GROMACS软件进行分子动力学模拟,对比野生型与突变型蛋白的均方根偏差(RMSD)、均方根波动(RMSF)、回转半径(Rg)及氢键数量等指标。结果解读显示,I-TASSER构建的模型3(C-score=-2.53)被选为最优三维结构,结构可视化显示K359R变异位于激酶域的关键位置;稳定性分析中,I-Mutant、MUpro、mCSM和SDM预测蛋白稳定性降低(DDG值分别为-0.23、-0.11、-0.073和-0.040 kcal/mol),仅DynaMut预测稳定性升高(DDG值为0.161 kcal/mol);分子动力学模拟结果显示,突变型蛋白的RMSD、RMSF、Rg值与野生型存在显著差异,表明变异导致蛋白构象稳定性下降,而氢键数量无显著变化(文献未明确提供具体数据,基于图表趋势推测)。
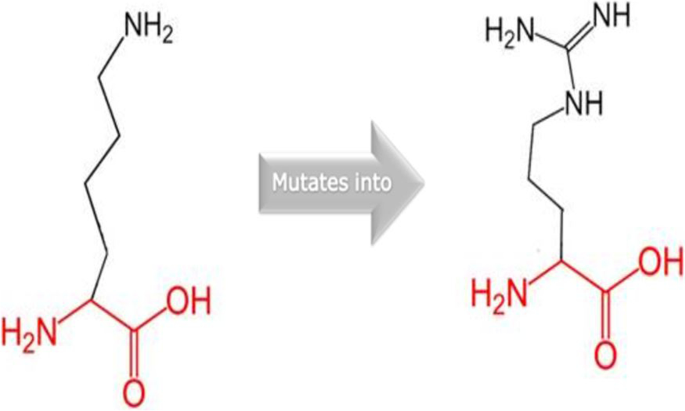
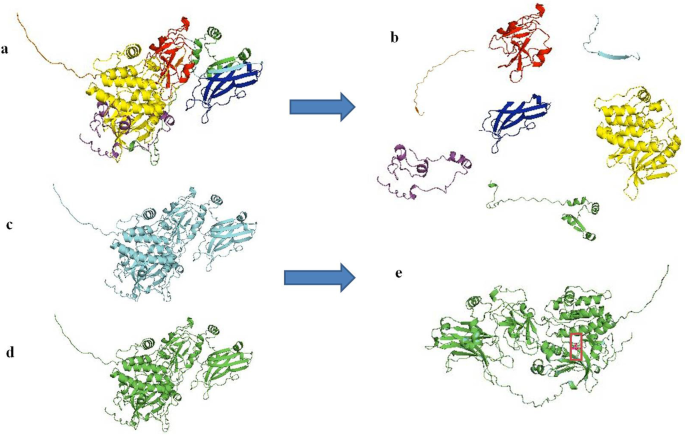
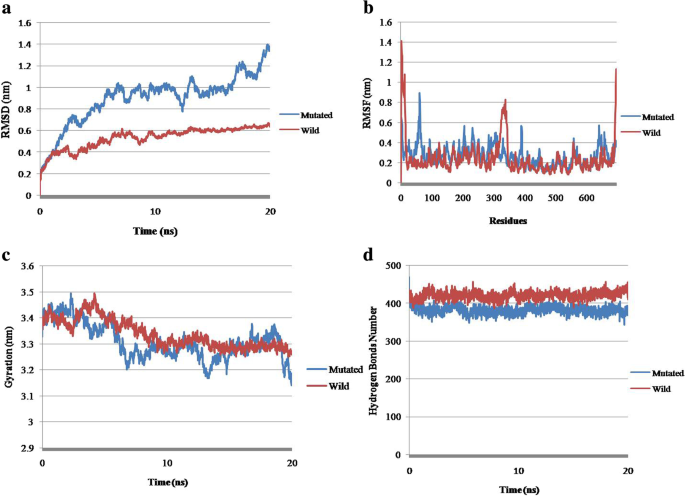
文献未提及具体实验产品,领域常规使用蛋白结构预测工具及分子动力学模拟软件。
3.3 临床样本的基因型与功能验证
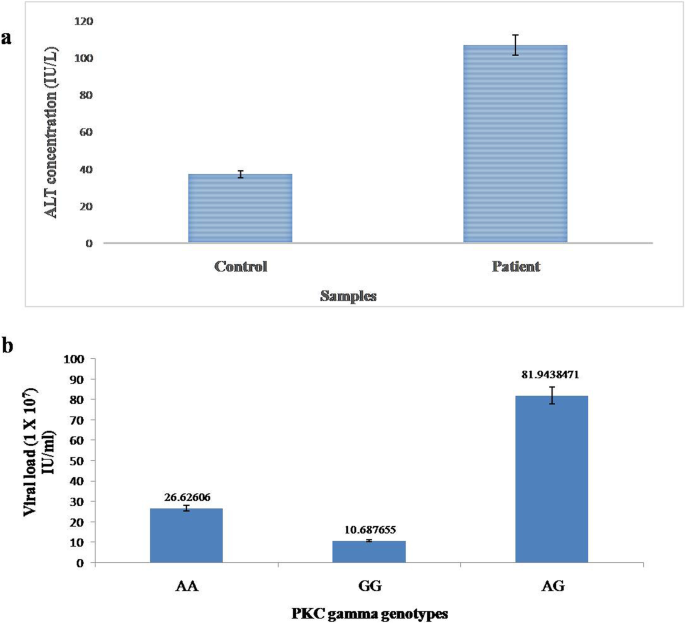
实验目的是验证rs1331262028与HCV诱导HCC的关联,分析其与临床指标的相关性。方法细节为收集100例HCV诱导HCC患者和100例HCV阴性健康对照的血液样本,采用酚-氯仿法提取基因组DNA,通过扩增阻滞突变系统PCR(ARMS-PCR)进行基因型分析;使用Merck的谷丙转氨酶(ALT)试剂盒检测血液ALT水平,采用FavorPrep™ Viral DNA/RNA Kit提取病毒RNA,通过实时定量反转录PCR(qRT-PCR)检测病毒载量。结果解读显示,基因型分析中野生型纯合子AA与HCC的关联最强,比值比(OR)为5.194,相对风险(RR)为2.287(n=200,P<0.0001);患者的平均ALT水平为107 U/L,显著高于对照组(n=200,P<0.05);AG基因型患者的病毒载量显著高于AA和GG基因型(n=100,P<0.05)。
实验所用关键产品:Merck的ALT试剂盒、Becton, Dickinson and Company的EDTA采血管、FavorPrep™ Viral DNA/RNA Kit(货号FAVNK 001–1)、SOLIS BIODYNE的FIREScript® RT cDNA合成试剂盒(货号06–15-0000S)。
4. Biomarker研究及发现成果解析
Biomarker定位:本研究鉴定的核心Biomarker为PKCγ基因的SNP rs1331262028(K359R),属于遗传生物标志物,筛选与验证逻辑遵循“生物信息学多工具联合筛选致病性SNP→分子动力学模拟验证蛋白结构影响→临床大样本验证疾病关联”的完整链条。
研究过程详述:该Biomarker来源于人类基因组的PRKCG基因,通过临床血液样本进行验证,采用ARMS-PCR技术进行基因型检测,qRT-PCR检测病毒载量,ALT检测评估肝功能损伤程度;特异性与敏感性方面,野生型AA基因型的OR为5.194(95%置信区间未明确提供),敏感性数据未明确提供;核心成果显示,该SNP的野生型纯合子AA与HCV诱导HCC的发病风险显著相关(RR=2.287,n=200,P<0.0001),AG基因型与患者体内更高的HCV病毒载量相关;创新性在于首次发现PKCγ的SNP与HCV诱导HCC的关联,为该疾病的早期诊断提供了新的潜在遗传标志物,经进一步临床验证后可用于疾病风险筛查与管理。
