1. 领域背景与文献引入
文献英文标题:Potential non-invasive biomarkers in tumor immune checkpoint inhibitor therapy: response and prognosis prediction;发表期刊:Biomark Res;影响因子:未公开;研究领域:肿瘤免疫治疗生物标志物研究。
领域共识:2010年伊匹木单抗(ipilimumab)获批用于转移性黑色素瘤治疗,标志着免疫检查点抑制剂(ICI)时代正式开启,此后PD-1/PD-L1等抑制剂陆续获批,显著改善了黑色素瘤、非小细胞肺癌等多种恶性肿瘤患者的生存预后。ICI通过阻断肿瘤微环境中的免疫抑制信号通路,恢复T细胞的细胞毒活性以实现抗肿瘤免疫应答,相较于化疗具有更好的靶向性和更少的全身不良反应,相较于靶向治疗适用人群更广泛。然而,仅15%-60%的肿瘤患者能从ICI治疗中获得显著响应,且现有临床常用的疗效预测生物标志物如PD-L1免疫组化、组织肿瘤突变负荷(tTMB)等多为侵入性检测,存在肿瘤异质性导致的采样偏差、无法动态监测治疗反应等局限性。当前领域的核心问题是缺乏精准、便捷、可动态监测的非侵入性生物标志物,以筛选最可能从ICI治疗中获益的患者,避免无效治疗和医疗资源浪费。
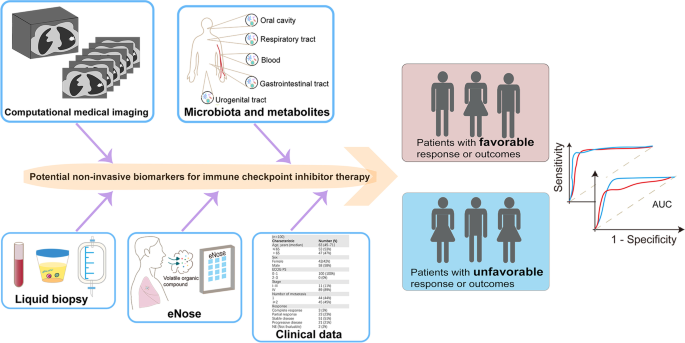
针对这一研究空白,本文系统综述了近年肿瘤ICI治疗领域中具有临床应用潜力的非侵入性生物标志物,涵盖医学影像组学、液体活检、微生物组及代谢物、电子鼻、临床特征等多个维度,为临床精准筛选ICI获益人群、优化治疗决策提供了全面的参考依据。
2. 文献综述解析
本文以非侵入性生物标志物的类型为分类维度,系统梳理了肿瘤ICI治疗疗效预测标志物的最新研究进展,对比了不同类型标志物的临床应用潜力、优势与局限性,明确了领域内尚未解决的核心问题,为未来非侵入性生物标志物的研发与临床转化指明了方向。
现有研究中,医学影像组学结合人工智能(AI)技术可通过分析CT、PET、MRI等影像特征,非侵入性预测PD-L1表达、肿瘤浸润淋巴细胞(TILs)水平及患者生存预后,部分模型的预测效能可媲美侵入性检测;液体活检标志物包括循环肿瘤细胞(CTC)、循环免疫细胞、细胞游离DNA(cfDNA)、血清蛋白质组、外泌体等,能从细胞、分子层面反映肿瘤负荷与宿主免疫状态,其中血液肿瘤突变负荷(bTMB)已在多项临床试验中验证其对ICI疗效的预测价值;肠道微生物组组成及代谢物如短链脂肪酸(SCFA)可通过调控宿主免疫影响ICI响应,为完全无创的疗效预测提供了新方向;电子鼻技术通过分析呼出气中的挥发性有机化合物,可快速预测ICI治疗响应;性别、体成分等临床特征也被证实与ICI疗效相关,为临床初步筛选提供了便捷指标。现有研究的优势在于非侵入性检测可降低患者采样风险、实现动态监测,部分标志物已展现出良好的临床转化潜力;局限性在于多数研究为回顾性设计,样本量有限,不同研究的检测方法、cutoff值未标准化,导致队列间结果异质性较大,部分标志物的预测机制尚未完全阐明。
与现有研究多聚焦单一类型非侵入性标志物不同,本文全面整合了近年各类型非侵入性生物标志物的研究证据,对比了不同标志物的优劣与适用场景,指出了领域内亟需解决的检测技术标准化、多中心验证、机制研究等核心问题,弥补了领域内缺乏系统综述非侵入性ICI疗效预测生物标志物的空白,为后续的研究与临床转化提供了系统的参考框架。
3. 研究思路总结与详细解析
本文的研究目标是系统梳理肿瘤ICI治疗中具有临床应用潜力的非侵入性生物标志物,核心科学问题是如何利用非侵入性检测手段精准预测ICI的疗效与预后,技术路线为按非侵入性生物标志物的类型分类,分别综述各类型标志物的研究进展、临床证据、优势与挑战,最后总结未来研究方向与临床转化策略。
3.1 医学影像组学生物标志物研究
实验目的:综述医学影像组学结合AI技术在ICI疗效预测中的研究进展与临床应用潜力。
方法细节:系统检索近年基于CT、PET、MRI等医学影像的ICI疗效预测研究,按影像类型、AI算法、研究设计、样本量等维度整理分析,重点关注经过多中心验证的研究结果。
结果解读:基于PET/CT的AI模型可非侵入性预测非小细胞肺癌(NSCLC)患者的PD-L1表达,其中深度学习评分(DLS)区分PD-L1阳性与阴性患者的AUC≥0.82,且其预测无进展生存(PFS)和总生存(OS)的效能与PD-L1免疫组化相当;扩散MRI可预测胶质母细胞瘤患者ICI治疗后的OS,治疗后相对表观扩散系数(rADC)≥1.63的患者中位OS为10.3个月,显著高于rADC<1.63的患者(6.1个月,HR=0.41,P=0.02);基于CT影像的放射组学标志物可区分“热肿瘤”与“冷肿瘤”,高评分患者的中位OS为24.3个月,显著高于低评分患者(11.5个月,P=0.0081)。
产品关联:文献未提及具体实验产品,领域常规使用的有PET/CT成像系统、MRI成像系统、AI影像分析平台等。
3.2 液体活检生物标志物研究
实验目的:综述液体活检各类型标志物在ICI疗效预测中的研究证据与临床价值。
方法细节:系统检索近年基于血液样本的ICI疗效预测研究,按标志物类型(CTC、循环免疫细胞、cfDNA、蛋白质组、外泌体)整理分析,重点关注具有统计学显著性的预测指标与cutoff值。
结果解读:CTC的存在与NSCLC患者ICI无持久响应相关,治疗前CTC阳性患者的无持久响应风险是阴性患者的3.57倍(P=0.02);循环免疫细胞中,PD-1+CD8+T细胞的Ki67水平与肿瘤负荷的比值>1.94的患者,ICI治疗后的客观缓解率(ORR)、PFS、OS均显著更优(P<0.05);bTMB≥16的NSCLC患者接受阿替利珠单抗治疗的ORR为35.7%,显著高于bTMB<16的患者(5.5%,n=152,P<0.0001);血清白血病抑制因子(LIF)低水平患者的持久临床获益(DCB)率为41.7%,显著高于高水平患者(6.4%,P<0.0001);基线循环外泌体PD-L1水平高的转移性黑色素瘤患者ICI预后更差,治疗后3-6周外泌体PD-L1水平升高>2.43倍的患者预后更优(P<0.05)。
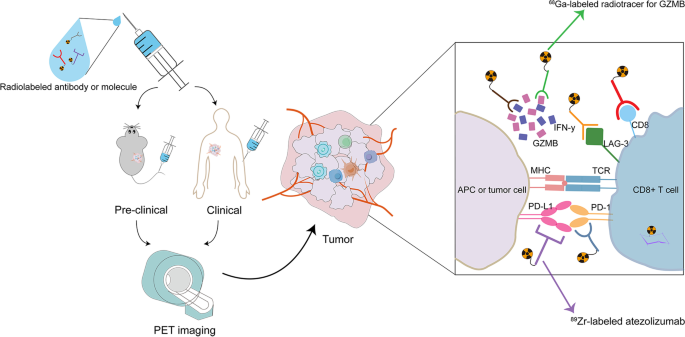
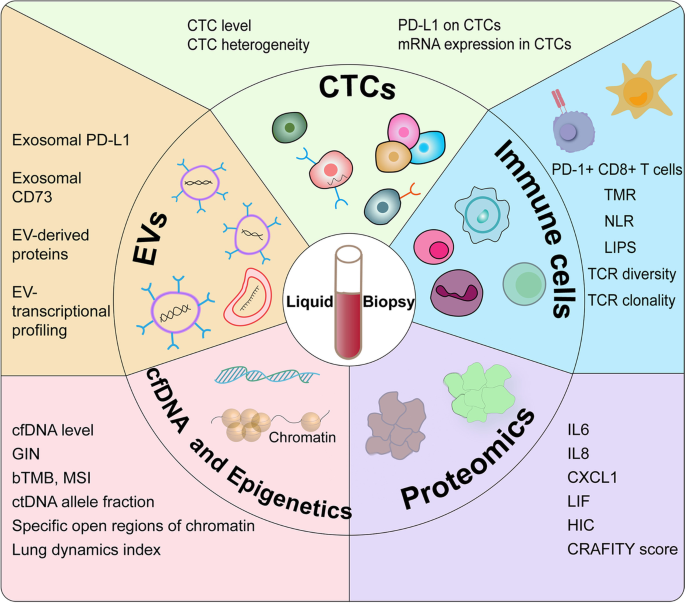
产品关联:文献未提及具体实验产品,领域常规使用的有流式细胞仪、二代测序平台、蛋白质组学分析系统、外泌体分离检测试剂盒等。
3.3 微生物组及代谢物生物标志物研究
实验目的:综述肠道微生物组及代谢物在ICI疗效预测中的研究进展与作用机制。
方法细节:系统检索近年关于微生物组与ICI疗效的研究,按微生物种类、代谢物类型、研究队列整理分析,重点关注菌群组成与ICI响应的相关性。
结果解读:黑色素瘤患者中,基线粪便样本中Ruminococcaceae丰度高的患者ICI响应更好(n=43,P<0.01);SCFA水平与ICI响应的相关性存在肿瘤类型差异,实体瘤患者中响应者的粪便和血清SCFA水平显著高于非响应者(P<0.05),但多发性骨髓瘤患者中低水平丁酸盐和丙酸盐与更长PFS相关(P=0.0015、P=0.0029)。
产品关联:文献未提及具体实验产品,领域常规使用的有粪便菌群测序平台、代谢物检测质谱仪等。
3.4 电子鼻及临床特征相关生物标志物研究
实验目的:综述电子鼻技术及临床特征在ICI疗效预测中的应用价值。
方法细节:系统检索近年关于电子鼻、性别、体成分与ICI疗效的研究,按检测方法、临床特征类型整理分析。
结果解读:电子鼻分析NSCLC患者呼出气成分,预测3个月ICI响应的AUC在训练队列达0.89,验证队列达0.85;meta分析显示,男性ICI治疗的OS HR为0.72,女性为0.86,性别差异具有统计学显著性(n=11351,P=0.0019);转移性黑色素瘤患者中,肥胖男性的PFS和OS显著优于正常BMI男性(HR=0.75、HR=0.64,P<0.05)。
产品关联:文献未提及具体实验产品,领域常规使用的有电子鼻检测系统、体成分分析仪等。
4. Biomarker研究及发现成果解析
本文系统总结了五大类肿瘤ICI治疗的非侵入性生物标志物,涵盖从影像到分子、从宿主到菌群的多个维度,明确了各标志物的预测效能、适用场景与局限性,为临床精准筛选ICI获益患者提供了全面的生物标志物选择框架。
Biomarker定位
本文涉及的非侵入性生物标志物分为五大类:医学影像组学生物标志物、液体活检生物标志物、微生物组及代谢物生物标志物、电子鼻生物标志物、临床特征生物标志物。筛选与验证逻辑为:基于临床队列研究,部分标志物经过多中心回顾性或前瞻性队列验证,部分经过临床试验验证,其中bTMB、影像组学DLS评分等已展现出较高的临床转化潜力。
研究过程详述
医学影像组学生物标志物基于CT、PET、MRI的影像特征,结合AI算法构建预测模型,例如PET/CT的DLS评分预测PD-L1表达的AUC在训练队列达0.86(n=99,95%CI 0.79-0.94),验证队列达0.81(n=48,95%CI 0.68-0.92);液体活检生物标志物中,CTC的存在可独立预测NSCLC患者ICI无持久响应(P=0.02),bTMB≥16的NSCLC患者ORR为35.7%(n=152,P<0.0001),TMR(调节性T细胞与Lox-1+PMN-MDSCs的比值)>0.39的NSCLC患者PFS显著更长(中位103天vs35天,n=34,P=0.0079);微生物组生物标志物中,黑色素瘤患者基线Ruminococcaceae丰度高与更好的ICI响应相关(n=43,P<0.01),实体瘤患者响应者的SCFA水平更高(P<0.05);电子鼻生物标志物预测NSCLC患者ICI响应的AUC达0.89;临床特征中,男性ICI治疗的OS获益更显著(HR=0.72,n=11351,P=0.0019),肥胖男性黑色素瘤患者的PFS和OS更优(HR=0.75、HR=0.64,P<0.05)。
核心成果提炼
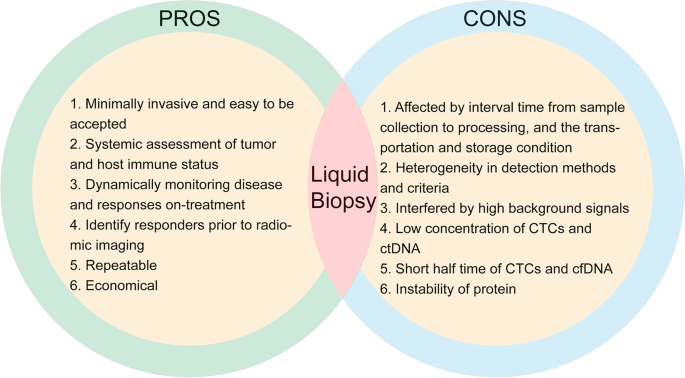
这些非侵入性生物标志物各有独特优势,医学影像组学可可视化肿瘤微环境与免疫状态,液体活检可动态监测肿瘤与免疫的实时变化,微生物组提供了完全无创的预测维度,电子鼻实现了快速便捷检测,临床特征易获取可用于初步筛选。创新性在于本文首次全面整合了近年各类型非侵入性ICI疗效预测生物标志物的研究证据,对比了不同标志物的优劣与适用场景,指出了领域内亟需解决的检测技术标准化、多中心验证、机制研究等核心问题。统计学结果方面,各标志物的预测效能均经过统计学验证,如影像组学模型的AUC值、液体活检标志物的ORR与生存差异的P值、微生物组丰度差异的P值等,部分标志物的统计学显著性较高(P<0.0001)。
