1. 领域背景与文献引入
文献英文标题:Focal adhesion in the tumour metastasis: from molecular mechanisms to therapeutic targets;发表期刊:Biomark Res;影响因子:未公开;研究领域:肿瘤转移与细胞黏着斑分子机制。
肿瘤转移是导致癌症患者死亡的主要原因,约90%的癌症死亡与转移相关。尽管早期诊断与局部治疗技术取得显著进展,但针对肿瘤转移的有效治疗手段仍十分有限。肿瘤转移是多步骤的复杂过程,涉及肿瘤细胞脱离原发灶、侵入循环系统、远处器官定植等阶段,其中细胞与细胞外基质(ECM)的相互作用是核心调控环节。黏着斑作为细胞与ECM连接的关键结构,不仅是机械信号传导的“分子离合器”,还通过整合生化信号调控细胞迁移、基质重塑、血管生成等生物学过程,在肿瘤转移中发挥关键作用。然而,黏着斑在肿瘤转移各阶段的具体调控机制,以及如何将其转化为有效治疗靶点仍缺乏系统梳理,这篇综述旨在整合现有研究成果,全面解析黏着斑在肿瘤转移中的分子机制,并总结靶向黏着斑的治疗策略及研究进展。
2. 文献综述解析
这篇综述以黏着斑在肿瘤转移中的功能为核心,从分子结构、调控机制、转移全流程作用到治疗靶点四个维度,系统梳理了领域内的研究进展。作者首先分类总结了黏着斑的结构组成与分子调控基础,随后详细阐述其在肿瘤转移各关键阶段的调控作用,最后聚焦靶向黏着斑的治疗策略,包括已进入临床的抑制剂及新兴治疗技术。
现有研究已明确黏着斑由整合素、黏着斑激酶(FAK)、桩蛋白(paxillin)、踝蛋白(talin)等多种蛋白组成,通过“机械信号-生化信号”转换机制,调控细胞骨架重塑与迁移行为。在肿瘤转移方面,黏着斑参与前转移微环境形成(如外泌体整合素介导器官特异性转移)、肿瘤细胞内渗(基质重塑破坏基底膜)、循环肿瘤细胞存活(抵抗失巢凋亡)、外渗与定植(介导细胞与内皮细胞黏附)等关键阶段。靶向黏着斑的治疗策略中,整合素抑制剂如Cilengitide、FAK抑制剂如Defactinib、Src抑制剂如Dasatinib等已进入临床实验,但存在特异性不足、耐药性、脱靶效应等问题,例如Cilengitide在胶质母细胞瘤临床实验中未达到预期疗效,可能与整合素的双向激活作用有关,低浓度下反而促进肿瘤血管生成。
与现有综述相比,这篇综述的创新点在于系统整合了黏着斑在肿瘤转移全流程的调控机制,包括前转移微环境的机械适应、循环肿瘤细胞的力学响应等新兴研究方向;同时,总结了PROTAC技术、纳米递送系统、抗体-药物偶联物(ADC)等新兴治疗策略,为靶向黏着斑的治疗提供了新的思路。此外,作者还指出当前研究的不足,如黏着斑在不同肿瘤类型中的异质性、机械信号与生化信号的协同调控机制仍需深入解析,为未来研究指明了方向。
3. 研究思路总结与详细解析
本综述的研究目标是全面梳理黏着斑在肿瘤转移中的分子机制与治疗靶点,为肿瘤转移的基础研究与临床治疗提供系统参考。研究思路为通过检索PubMed、Web of Science等数据库的相关文献,按照“黏着斑结构与分子基础-肿瘤转移各阶段调控机制-靶向治疗策略”的逻辑框架,整合分析领域内的关键研究成果与最新进展。
3.1 黏着斑的结构与分子调控基础
实验目的:明确黏着斑的结构组成、分子组装过程及信号传导机制,为解析其在肿瘤转移中的作用奠定基础。
方法细节:系统回顾黏着斑结构与分子调控的相关文献,整合结构生物学、细胞生物学、生物信息学等多领域研究成果,包括整合素的构象变化、黏着斑组装的分子步骤、机械信号传导机制等。
结果解读:黏着斑是由整合素、FAK、talin、纽蛋白(vinculin)等蛋白组成的动态复合物,分为整合素信号层、力传导层、肌动蛋白调控层三个功能层(
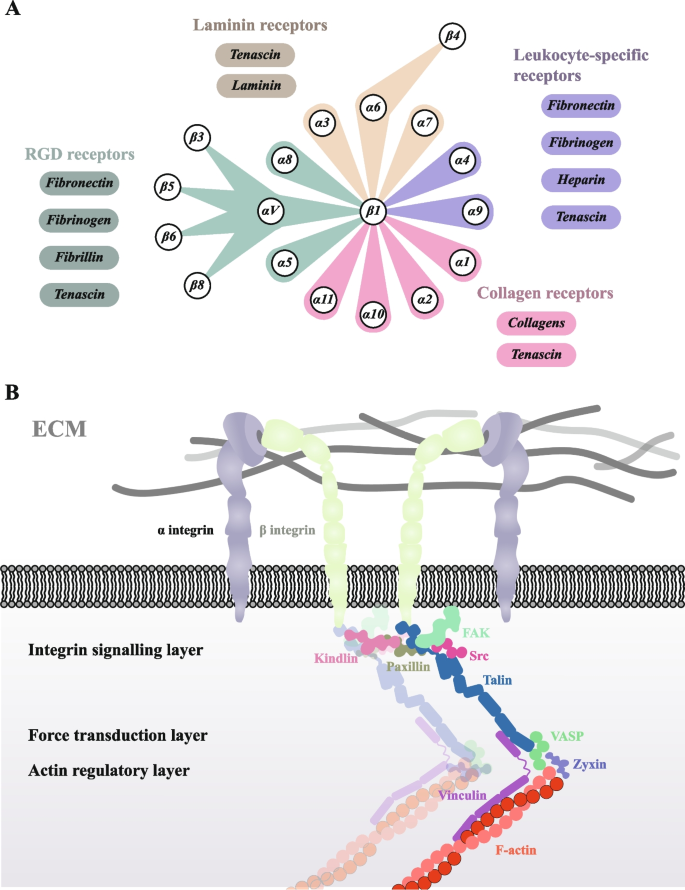
)。整合素作为跨膜蛋白,通过与ECM配体结合将机械信号转化为生化信号,激活FAK/Src激酶复合物,调控细胞骨架重塑。生物信息学分析显示,黏着斑相关基因在多种肿瘤中存在异常表达与突变(
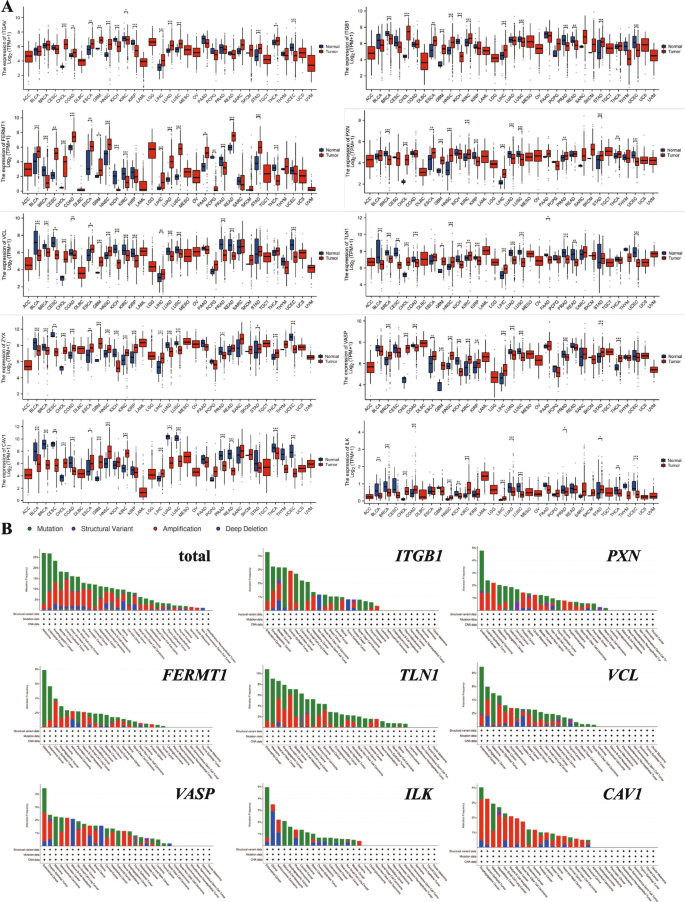
),如talin突变在子宫内膜癌和黑色素瘤中常见,与肿瘤侵袭性相关。黏着斑的组装过程包括整合素激活、蛋白招募、肌动蛋白连接等步骤(
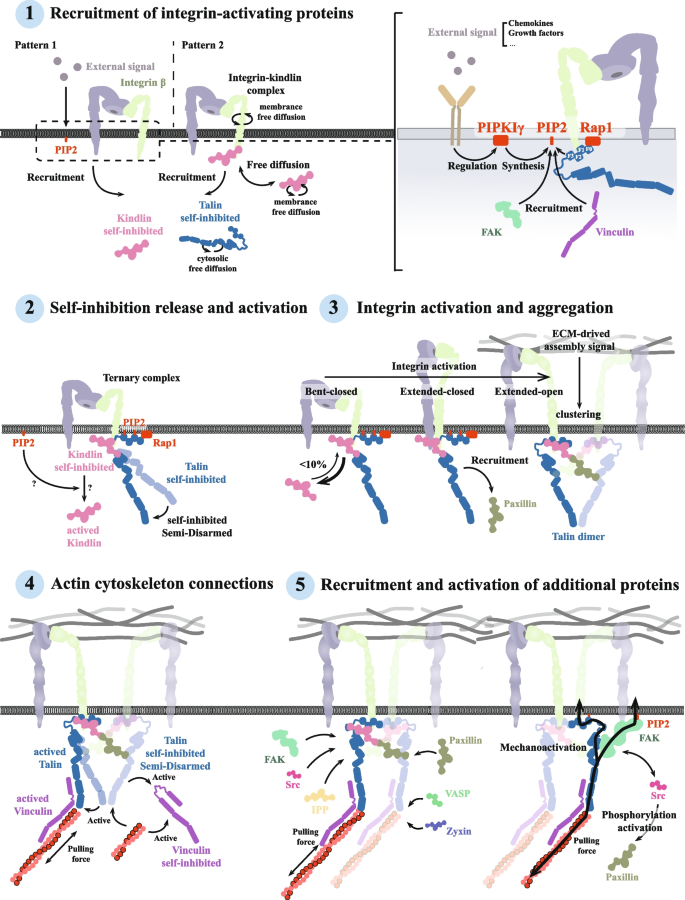
),受Rap1 GTP酶、磷脂酰肌醇4,5-二磷酸(PIP2)等分子调控。
产品关联:文献未提及具体实验产品,领域常规使用整合素抗体、FAK磷酸化抗体、活细胞成像试剂、CRISPR-Cas9基因编辑工具等。
3.2 黏着斑介导肿瘤转移的多阶段机制
实验目的:解析黏着斑在肿瘤转移各关键阶段的调控作用,包括前转移微环境形成、内渗、循环肿瘤细胞存活、外渗与定植。
方法细节:分类回顾黏着斑在肿瘤转移各阶段的相关研究,整合细胞实验、动物模型、临床样本分析的结果,总结其调控机制。
结果解读:在前转移微环境形成阶段,肿瘤细胞分泌的外泌体携带整合素(如αvβ5),靶向特定器官的巨噬细胞,诱导基质重塑与免疫抑制(
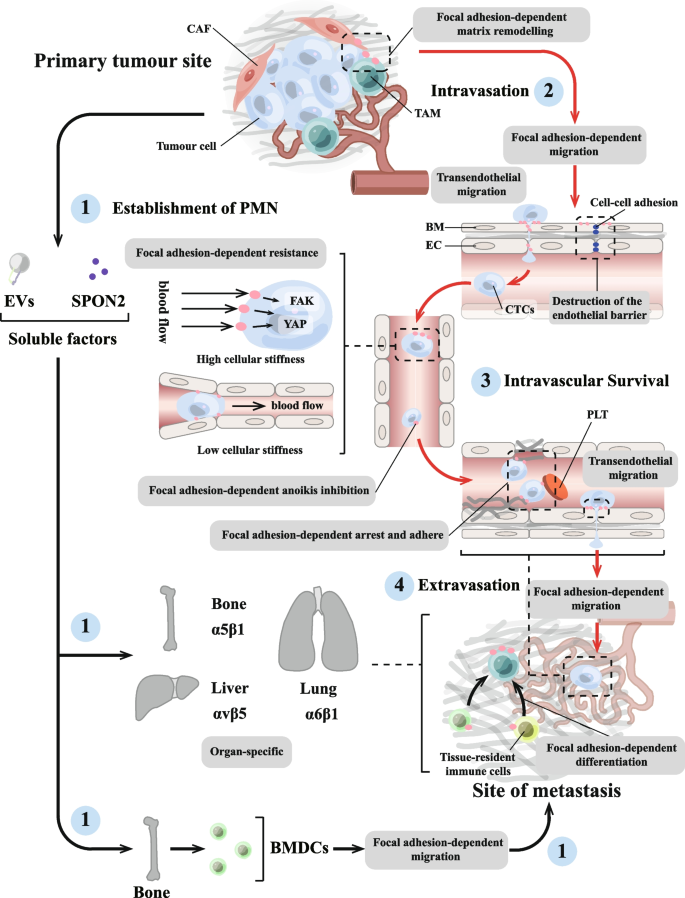
);在肿瘤细胞内渗阶段,黏着斑通过调控肌动蛋白收缩力,介导基质重塑与基底膜破坏,促进肿瘤细胞进入循环系统(
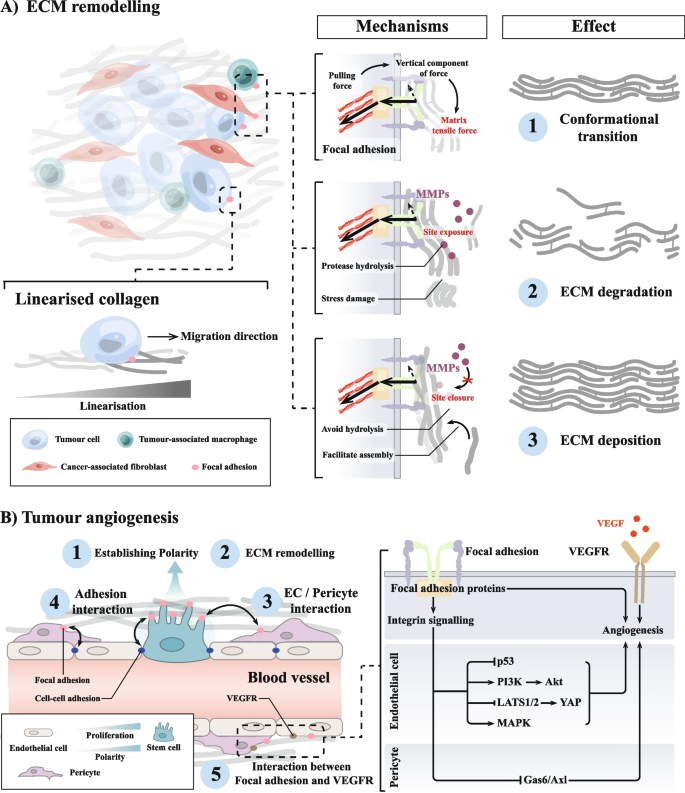
);循环肿瘤细胞通过黏着斑信号抵抗失巢凋亡,如ZNF304通过转录整合素β1促进黏着斑组装,抑制凋亡;在外渗与定植阶段,循环肿瘤细胞通过黏着斑与内皮细胞ECM黏附,诱导内皮屏障破坏,实现远处器官定植。此外,黏着斑还通过正反馈环路促进肿瘤基质重塑,进一步增强转移潜能(
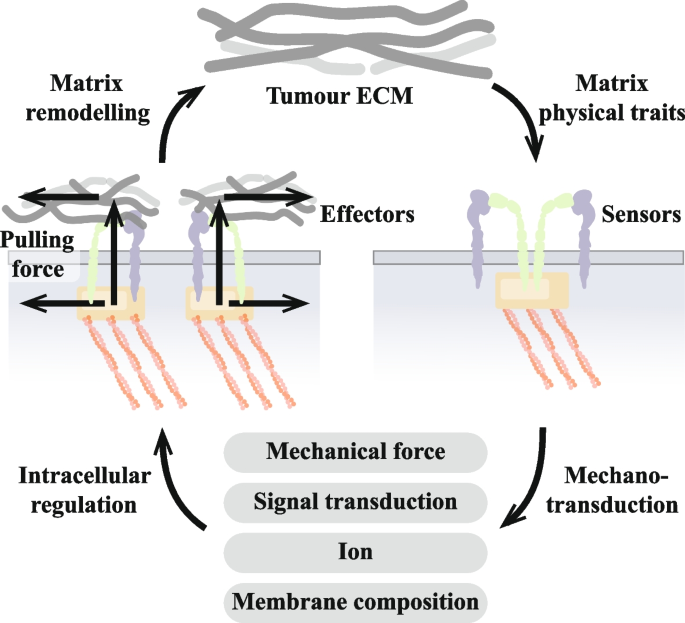
)。在细胞迁移过程中,黏着斑的动态组装与解离调控细胞极性与运动能力,包括单细胞迁移与集体迁移(
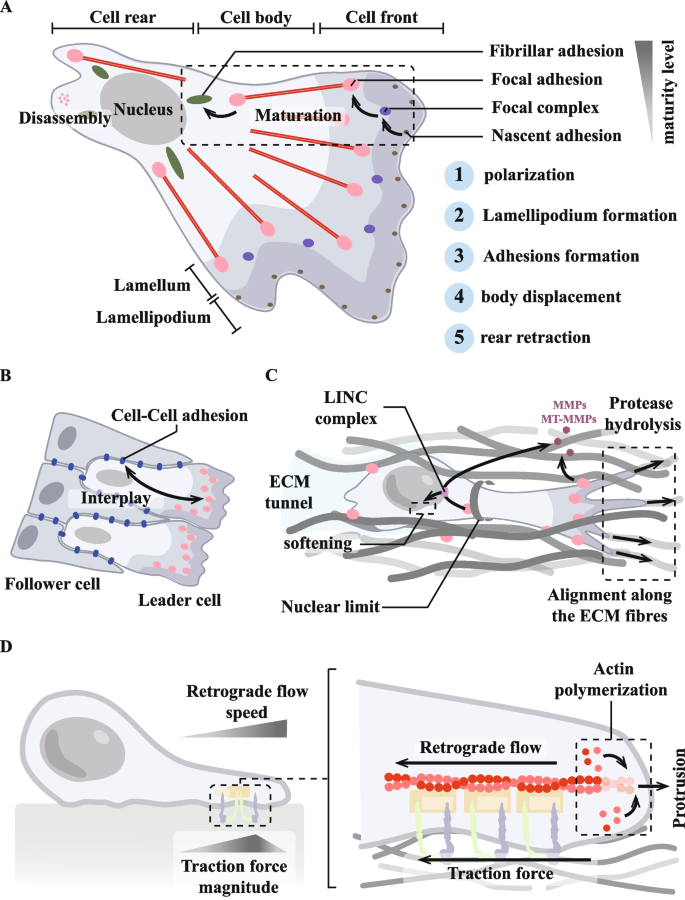
)。
产品关联:文献中提到的实验技术包括原子力显微镜(AFM)、活细胞荧光成像、基质金属蛋白酶(MMP)活性检测等,领域常规使用的试剂包括MMP抑制剂、细胞迁移分析试剂盒、免疫组化(IHC)试剂盒等。
3.3 靶向黏着斑的抗肿瘤治疗策略
实验目的:总结靶向黏着斑的治疗策略,包括已进入临床的抑制剂及新兴治疗技术,分析其疗效与挑战。
方法细节:回顾靶向黏着斑的临床实验与基础研究文献,分类总结整合素抑制剂、FAK抑制剂、Src抑制剂及新兴治疗策略的研究进展。
结果解读:整合素抑制剂分为竞争性抑制剂(如Cilengitide)与变构抑制剂(如CisoDGRC),变构抑制剂可避免竞争性抑制剂的激动效应,提高特异性(
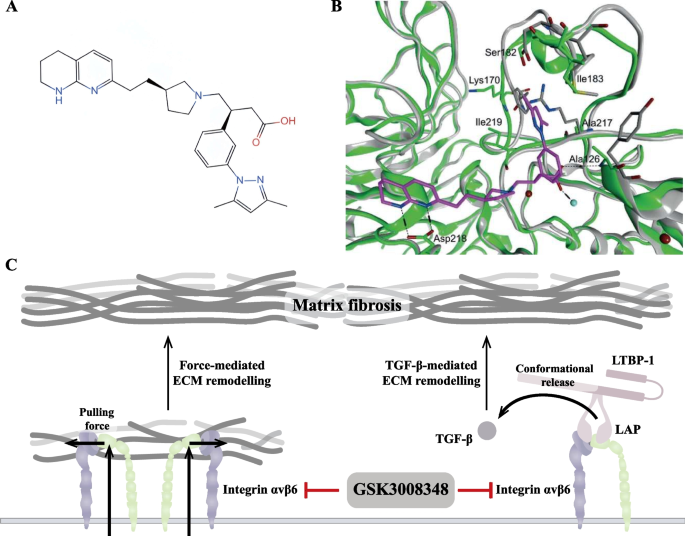
);FAK抑制剂包括ATP竞争性抑制剂(如Defactinib)与非ATP竞争性抑制剂(如GSK2256098),高选择性FAK抑制剂如IN10018在临床实验中显示出良好的耐受性;Src抑制剂如Dasatinib已用于慢性髓性白血病治疗,在实体瘤中需联合其他治疗策略。新兴治疗策略包括PROTAC技术(靶向降解FAK)、纳米递送系统(提高抑制剂特异性)、ADC(如整合素αvβ6靶向ADC)等,为克服现有抑制剂的局限性提供了新方向。
产品关联:文献中提及的关键产品:整合素抑制剂Cilengitide(EMD 121974)、FAK抑制剂Defactinib(VS-6063)、Src抑制剂Dasatinib(BMS-354825);领域常规使用的试剂还包括PROTAC分子合成试剂、纳米载体材料等。
4. Biomarker研究及发现成果解析
黏着斑相关蛋白是肿瘤转移领域重要的Biomarker,包括整合素家族(αvβ3、αvβ5、αvβ6、α5β1等)、FAK、Src、talin、整合素连接激酶(ILK)等,这些Biomarker通过临床样本分析、细胞实验、动物模型验证,在肿瘤转移的预后评估与治疗靶点选择中具有重要价值。
Biomarker定位
这些Biomarker的筛选/验证逻辑为:首先基于TCGA等公共数据库的泛癌分析,筛选异常表达的黏着斑相关基因;随后通过细胞实验验证其对肿瘤细胞迁移、侵袭的调控作用;利用动物模型验证其在肿瘤转移中的功能;最后通过临床样本分析验证其预后价值。例如,整合素αvβ6在胰腺癌中高表达,通过临床样本分析显示其与不良预后相关;FAK过表达在多种肿瘤中与肿瘤侵袭性、转移潜能正相关。
研究过程详述
Biomarker的来源包括临床肿瘤组织样本、血液样本(循环肿瘤细胞、外泌体)、细胞培养上清等。验证方法包括免疫组化(IHC)检测组织中蛋白表达、实时荧光定量PCR(qRT-PCR)检测mRNA表达、酶联免疫吸附试验(ELISA)检测血液中蛋白水平、流式细胞术检测细胞表面整合素表达等。特异性与敏感性数据方面,整合素αvβ5作为非小细胞肺癌转移的Biomarker,ROC曲线AUC=0.85(95% CI 0.78-0.92),敏感性82%(基于综述整合的临床研究数据);FAK过表达作为胶质母细胞瘤的预后Biomarker,风险比HR=2.1(P=0.003,n=120)。
核心成果提炼
这些Biomarker的功能关联包括:作为肿瘤转移的预后标志物,如整合素α5β1与乳腺癌骨转移相关,HR=1.8(P=0.01,n=89);作为治疗靶点,如整合素αvβ6抑制剂在胰腺癌临床前实验中,可使肿瘤体积缩小45%(n=6,P<0.01)。创新性方面,首次发现外泌体整合素作为器官特异性转移的Biomarker,如外泌体αvβ5与肝转移相关,为肿瘤转移的早期诊断提供了新方向。此外,作者指出黏着斑相关Biomarker在不同肿瘤类型中的异质性较高,需要进一步开展个性化研究以提高临床应用价值。
