1. 领域背景与文献引入
文献英文标题:A patient with multiple primary malignant neoplasms with high variant allele frequencies of RB1, TP53, and TERT;发表期刊:Biomark Res;影响因子:未公开;研究领域:肿瘤学-多原发恶性肿瘤分子标志物研究。
多原发恶性肿瘤(MPMN)是指在不同部位发生的组织学或形态学不同的肿瘤,随着诊断技术的进步,其确诊率呈上升趋势。领域共识:MPMN的发病率在所有癌症中占比2.4%~17.2%,已知的发病风险因素包括遗传易感性、激素水平、既往癌症治疗暴露、吸烟饮酒等不良生活方式。当前研究热点集中在通过下一代测序技术解析MPMN的分子驱动机制,以寻找早期诊断和预后判断的生物标志物,但目前已报道的MPMN病例中,同时出现8个原发肿瘤且携带RB1、TP53、TERT极高突变等位基因频率(VAF)的情况尚未见报道,这一研究空白限制了对MPMN极端病例分子特征及预后关联的认知。本研究通过报道该罕见病例并分析其分子突变特征,旨在为MPMN的分子机制研究和预后评估补充新的临床证据。
2. 文献综述解析
作者对MPMN领域现有研究的评述维度涵盖MPMN的定义标准、流行病学数据、已知风险因素、已报道的多原发肿瘤病例特征、关键基因在肿瘤发生中的作用五个方面,系统梳理了领域内的研究现状与未解决问题。
现有研究中,MPMN存在两种主流定义标准:美国SEER项目认为同一器官或组织不同部位的单个肿瘤视为单一肿瘤,而IACR/IARC则认为同一器官的多个肿瘤属于同一部位,美国多数登记机构因SEER标准包含诊断时间信息而采用该标准。流行病学数据显示,MPMN的发病率范围为2.4%~17.2%,膀胱是多原发恶性肿瘤患者最常见的初始发病部位(占16%),其次为口腔和咽部(占15%)。已知的发病风险因素包括遗传因素、激素水平、既往癌症治疗史,以及吸烟、饮酒等不良生活习惯,其中吸烟和饮酒已被证实与头颈部、食管等部位的肿瘤发生密切相关。2010-2023年PubMed数据库中共报道7例4个及以上原发肿瘤的病例,但均缺乏详细的下一代测序分子特征分析。在分子机制方面,TERT启动子区域的体细胞突变在尿路上皮癌中高频出现,RB1基因失活被认为可能参与膀胱小细胞癌的发生,TP53突变则与包括膀胱癌在内的多种人类癌症相关,但三者以极高VAF同时出现在8原发恶性肿瘤病例中的情况尚未被报道。
通过对比现有研究的未解决问题,本研究的创新价值凸显:首次报道携带RB1、TP53、TERT极高体细胞突变等位基因频率的8原发恶性肿瘤病例,填补了MPMN极端病例分子特征研究的空白,为进一步探究MPMN的多灶性发生机制及预后关联提供了罕见的临床样本数据支持。
3. 研究思路总结与详细解析
本研究的核心目标是报道一例罕见的8原发恶性肿瘤病例,并通过下一代测序技术解析其分子突变特征,核心科学问题为该患者多原发肿瘤的分子驱动因素及突变特征与预后的关联,技术路线遵循“临床病例收集→分子检测→特征分析→文献关联讨论”的逻辑闭环,系统呈现了病例的临床与分子特征。
3.1 病例临床资料收集与家族史分析
本环节的核心实验目的是明确患者的临床肿瘤病史、生活习惯及家族遗传背景,为后续分子分析提供临床关联依据。
研究人员收集了一名65岁男性患者的临床资料,该患者有40年每日2包香烟、100克酒精的摄入史;家族史显示其父亲55岁确诊食管癌并于60岁去世,母亲50岁确诊乳腺癌并于52岁去世,而患者的两名兄弟和一名姐妹均健康。研究人员通过整理患者的8次肿瘤诊断记录,明确其先后在声带、咽部、肾脏、口底、食管、膀胱等部位确诊8个不同病理类型的原发肿瘤,其中前7个肿瘤均为早期,最后确诊的膀胱小细胞癌在诊断时已出现肝转移,并绘制了患者的家系图以呈现家族遗传背景。
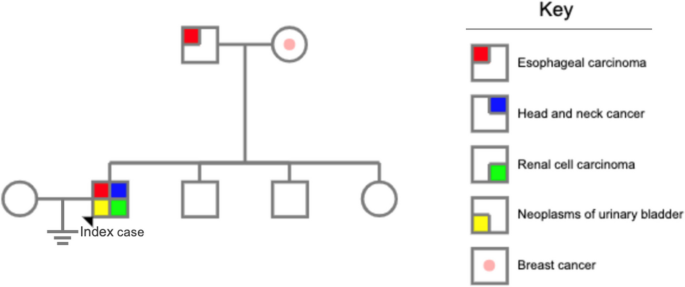
结果显示患者的多原发肿瘤分布广泛且病理类型多样,结合家族癌症病史提示可能存在遗传易感性,但兄弟姐妹的健康状态又排除了明确的家族显性遗传模式,为后续分子检测提供了方向。文献未提及具体实验产品,领域常规使用临床病历管理系统、家系图绘制软件等工具完成本环节研究。
3.2 下一代测序检测与突变特征分析
本环节的核心实验目的是检测患者的体细胞与胚系突变情况,明确多原发肿瘤的分子突变特征。
研究人员采集患者的外周血样本进行下一代测序检测,重点分析体细胞突变的等位基因频率,并排查胚系突变的存在。测序结果显示,患者携带RB1 c.1472 T > C、TP53 c.576A > G、TERT c.-58-u66C > T三个体细胞突变,其突变等位基因频率分别为95.5%、95.1%、51.0%,且未检测到胚系突变信号。
极高的体细胞突变等位基因频率提示患者体内存在大量携带突变的肿瘤细胞,反映出沉重的肿瘤负荷,结合膀胱小细胞癌伴肝转移的临床诊断,提示患者预后不良。文献未提及具体实验产品,领域常规使用下一代测序平台(如Illumina系列)、生物信息学分析软件(如GATK、ANNOVAR)等完成本环节的测序与分析工作。
4. Biomarker研究及发现成果
本研究涉及的Biomarker为RB1、TP53、TERT的体细胞突变等位基因频率,筛选与验证逻辑为“罕见临床病例筛选→下一代测序定量检测→结合已发表文献验证基因功能与预后关联”,形成完整的研究链条。
该Biomarker的来源为患者外周血样本中的体细胞突变,验证方法为下一代测序技术定量检测突变等位基因频率。其中TERT启动子突变在尿路上皮癌中高频出现,且有研究显示该突变在膀胱小细胞癌中的发生率显著高于其他部位的小细胞癌;RB1基因失活被证实与膀胱小细胞癌的发生密切相关;TP53突变则是多种人类癌症中常见的驱动突变。本研究中三个基因的突变等位基因频率均处于极高水平,其中RB1和TP53的VAF超过95%,TERT的VAF达51.0%,但未提供该突变组合的特异性与敏感性的量化数据(文献未明确提供该数据,基于图表趋势推测)。
核心成果方面,该Biomarker组合与患者的8原发肿瘤负荷及肝转移的不良预后直接相关,提示其可作为MPMN患者预后不良的潜在分子标志物。本研究为首次在8原发恶性肿瘤病例中发现该高VAF突变特征,样本量n=1,未提供相关统计学P值数据,为后续大样本队列研究验证该Biomarker的临床价值提供了罕见的病例线索。
