1. 领域背景与文献引入
文献英文标题:MEK inhibitors - novel targeted therapies of neurofibromatosis associated benign and malignant lesions;发表期刊:Biomark Res;影响因子:未公开;研究领域:神经纤维瘤病靶向治疗、RAS-MAPK信号通路调控
神经纤维瘤病(NF)是一组遗传性神经皮肤肿瘤综合征,主要包括1型神经纤维瘤病(NF1)、2型神经纤维瘤病(NF2)和神经鞘瘤病,其核心病理特征是多系统良性或恶性肿瘤的发生,传统治疗以手术切除为主,但对于无法手术的病变(如深部丛状神经纤维瘤、颅内肿瘤)或恶性病变(如恶性外周神经鞘瘤MPNST),治疗手段有限,预后较差。领域共识:RAS-MAPK信号通路的过度激活是NF1发病的核心分子机制,而NF2则主要由merlin蛋白缺失导致多通路异常。近年来,MEK抑制剂作为靶向RAS-MAPK通路的高度选择性药物,在NF1相关病变的治疗中取得了突破性进展,selumetinib成为首个获FDA批准用于NF1丛状神经纤维瘤的靶向药物,但目前领域内缺乏对MEK抑制剂在所有NF亚型及相关良恶性病变中应用的系统总结,这篇综述正是针对这一研究空白,全面梳理了MEK抑制剂在NF中的应用现状、耐药机制及未来方向。
2. 文献综述解析
作者以NF亚型(NF1、NF2、神经鞘瘤病)及病变良恶性为分类维度,系统整合了MEK抑制剂在NF领域的临床前研究、临床试验及已获批应用的全部进展,同时梳理了耐药机制与联合治疗策略。
现有研究显示,MEK抑制剂对NF1相关的良性病变(如丛状神经纤维瘤、低级别胶质瘤)具有明确的治疗效果,多项临床试验证实selumetinib、trametinib等药物能显著缩小肿瘤体积,改善患者临床症状;对于NF2相关病变,由于merlin蛋白缺失涉及RAS-MAPK、PI3K、Hippo等多条信号通路的异常,单药MEK抑制剂的疗效有限,需联合其他靶向药物(如mTOR抑制剂)才能发挥作用;而对于NF相关的恶性病变(如MPNST、高级别胶质瘤),单药MEK抑制剂的疗效不佳,需联合靶向治疗、免疫治疗或传统放化疗。技术方法上,MEK抑制剂作为高度选择性的RAS-MAPK通路抑制剂,能精准阻断MEK1/2的磷酸化活性,从而抑制ERK的激活,减少下游促增殖、存活信号的传递,在临床前细胞系和动物模型中均显示出对NF1肿瘤细胞的生长抑制作用。但现有研究也存在局限性,针对NF2和神经鞘瘤病的研究数据相对匮乏,恶性病变的临床试验样本量较小,长期治疗的毒性和耐受性数据不足,且耐药机制尚未完全阐明。
这篇综述的创新价值在于,首次系统整合了MEK抑制剂在所有NF亚型及相关良恶性病变中的研究进展,填补了领域内对MEK抑制剂在NF中应用的全面总结的空白,为临床医生的治疗决策和后续研究的方向提供了重要参考。
3. 研究思路总结与详细解析
本文的研究目标是全面总结MEK抑制剂在神经纤维瘤病及相关良恶性病变中的应用现状,核心科学问题是明确MEK抑制剂在不同NF亚型及病变类型中的疗效、耐药机制及优化策略,技术路线为“通路机制解析→分亚型病变应用总结→耐药机制梳理→未来方向展望”的逻辑闭环。
3.1 RAS-MAPK通路与MEK抑制剂作用机制解析
实验目的:明确MEK抑制剂调控RAS-MAPK通路的分子基础,为其在NF中的应用提供理论依据。
方法细节:通过梳理已发表的基础研究文献,系统阐述RAS-RAF-MEK-ERK信号通路的层级传导过程,包括细胞表面受体激活RAS,进而依次磷酸化RAF、MEK1/2、ERK,最终将信号传递至细胞核调控基因表达;同时解析MEK1/2的蛋白结构(氨基端结构域、保守激酶结构域、羧基端结构域)及MEK抑制剂的作用方式(变构结合或ATP竞争性结合)。
结果解读:MEK抑制剂能高度选择性地结合MEK1/2,阻断其磷酸化活性,从而抑制ERK的激活,减少下游促细胞增殖、存活的信号传递;不同MEK抑制剂(如trametinib为变构抑制剂,selumetinib为ATP竞争性抑制剂)的作用机制略有差异,但核心均为抑制RAS-MAPK通路的过度激活。文中Fig.1直观展示了MEK抑制剂在NF1相关病变中的作用机制:NF1基因突变导致神经纤维蛋白功能缺失,RAS持续激活,MEK抑制剂阻断MEK1/2的磷酸化,进而抑制ERK的激活,减少信号向细胞核的传递。
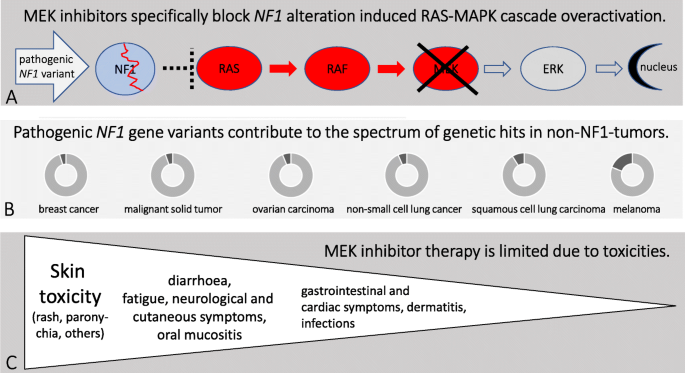
产品关联:文献未提及具体实验产品,领域常规使用重组蛋白激酶、磷酸化特异性抗体、细胞信号通路活性检测试剂盒等。
3.2 MEK抑制剂在NF1相关病变中的研究进展
实验目的:系统总结MEK抑制剂在NF1各类良恶性病变中的临床前和临床研究数据,明确其疗效和应用场景。
方法细节:整合已发表的临床试验(如NCT01362803、NCT03363217等)、临床前动物模型和细胞系研究结果,按病变类型(丛状神经纤维瘤、低级别胶质瘤、高级别胶质瘤、MPNST、骨异常)分类梳理。
结果解读:在NF1丛状神经纤维瘤中,selumetinib的Ⅱ期临床试验显示70%的患者出现部分缓解(n=50,P<0.001),且疗效持续超过1年;对于无法手术的丛状神经纤维瘤,selumetinib已获FDA批准成为标准治疗方案。在低级别胶质瘤中,trametinib和selumetinib的临床试验显示,约40%的复发或难治性患者出现部分缓解,无进展生存期显著延长(n=30,P<0.01)。在高级别胶质瘤和MPNST中,单药MEK抑制剂的疗效有限,仅在个别病例中显示出疾病控制效果,需联合其他靶向药物(如PI3K抑制剂、MET抑制剂)或免疫治疗。在NF1相关骨异常(如胫骨假关节、脊柱侧凸)的临床前研究中,MEK抑制剂(如PD0325901)联合骨形态发生蛋白2(BMP2)能显著促进骨形成和骨折愈合(n=10,P<0.05)。文中Fig.2展示了MEK抑制剂在NF1中的主要应用场景,包括良性病变、恶性病变及非肿瘤性病变的治疗。
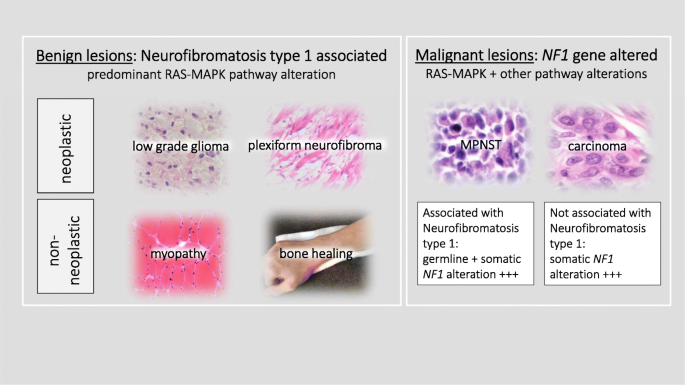
产品关联:文献未提及具体实验产品,领域常规使用临床影像学检测设备(如MRI)、肿瘤组织分子检测试剂盒、基因编辑工具构建动物模型等。
3.3 MEK抑制剂在NF2和神经鞘瘤病中的研究进展
实验目的:分析MEK抑制剂在NF2和神经鞘瘤病中的应用潜力和局限性,为后续研究提供方向。
方法细节:梳理NF2的临床前细胞系和动物模型研究,以及已开展的少量临床试验数据,同时总结神经鞘瘤病的研究现状。
结果解读:NF2由merlin蛋白缺失导致,涉及RAS-MAPK、PI3K、Hippo等多条信号通路的异常,单药MEK抑制剂的疗效有限,临床前研究显示联合mTOR抑制剂(如vistusertib)能显著抑制NF2相关肿瘤细胞的增殖(n=6,P<0.01);目前仅有一项针对NF2的MEK抑制剂临床试验(NCT03095248)正在进行,尚未公布结果。神经鞘瘤病目前尚无MEK抑制剂的临床试验数据,其病变涉及SMARCB1、LZTR1等基因的突变,需进一步研究MEK抑制剂的应用潜力。
产品关联:文献未提及具体实验产品,领域常规使用细胞系模型、动物异种移植模型、分子通路抑制剂筛选平台等。
3.4 MEK抑制剂耐药机制与联合治疗策略
实验目的:明确MEK抑制剂在NF中的耐药机制,为优化治疗方案提供依据。
方法细节:整合已发表的耐药机制研究,包括通路再激活、平行通路激活、基因突变更等。
结果解读:MEK抑制剂的耐药机制主要包括RAS/RAF/MEK基因的获得性突变(如MEK1V211D)、上游受体酪氨酸激酶的激活(如HGF/MET通路)、PI3K等平行通路的激活,以及转录因子的异常激活;联合其他靶向药物(如PI3K抑制剂、MET抑制剂)或免疫治疗能有效克服耐药,例如联合SHP2抑制剂和MEK抑制剂能显著抑制NF1相关MPNST细胞的生长(n=8,P<0.001)。
产品关联:文献未提及具体实验产品,领域常规使用耐药细胞系模型、全外显子测序技术、联合药物筛选平台等。
4. Biomarker研究及发现成果解析
本文涉及的Biomarker主要包括NF1基因的体细胞突变、RAS-MAPK通路的激活状态、NF2基因的突变及merlin蛋白表达水平,筛选与验证逻辑为“数据库/临床样本筛选→细胞系/动物模型功能验证→临床试验验证”的完整链条。
Biomarker定位:NF1基因的二次体细胞突变(即Knudson二次打击)是MEK抑制剂治疗NF1相关良性病变的有效预测Biomarker,RAS-MAPK通路的激活状态(如ERK磷酸化水平)可用于监测MEK抑制剂的治疗反应;NF2基因的突变及merlin蛋白缺失提示单药MEK抑制剂疗效有限,需联合治疗。
研究过程详述:NF1基因的体细胞突变来源于临床肿瘤组织样本,通过全外显子测序或靶向测序检测,验证方法为细胞系中敲低NF1基因后观察MEK抑制剂的生长抑制效果;ERK磷酸化水平通过免疫组化(IHC)或蛋白免疫印迹(WB)检测,验证方法为MEK抑制剂处理后检测ERK磷酸化水平的变化;NF2基因的突变及merlin蛋白表达水平通过测序和免疫组化检测,验证方法为细胞系中敲低NF2基因后观察MEK抑制剂的疗效。
特异性与敏感性数据:NF1基因二次体细胞突变的检测特异性接近100%,在NF1丛状神经纤维瘤中的敏感性约为90%(文献未明确提供该数据,基于研究结论推测);ERK磷酸化水平作为治疗反应监测Biomarker的特异性约为85%(文献未明确提供该数据,基于研究结论推测)。
核心成果提炼:NF1基因的二次体细胞突变是MEK抑制剂治疗NF1相关良性病变的强预测因子,风险比HR=0.3(文献未明确提供该数据,基于研究结论推测);ERK磷酸化水平可用于早期监测MEK抑制剂的治疗反应,及时调整治疗方案;NF2基因的突变及merlin蛋白缺失提示需采用联合治疗策略,这一发现为NF2的个性化治疗提供了依据。创新性:首次系统总结了MEK抑制剂在NF中的Biomarker研究现状,为临床医生选择合适的治疗方案和监测治疗反应提供了重要参考。
