1. 领域背景与文献引入
文献英文标题:Adjuvant cytokine-induced killer cell immunotherapy in hepatocellular carcinoma: real-world data and 9-year extended follow-up of a randomized controlled trial;发表期刊:Cancer Immunology, Immunotherapy;影响因子:未公开;研究领域:肿瘤免疫治疗(肝细胞癌辅助治疗方向)。
领域共识:肝细胞癌是全球最常见的恶性肿瘤之一,也是癌症相关死亡的主要原因,亚洲地区慢性乙型肝炎病毒感染高发,肝细胞癌占原发性肝癌的绝大多数。随着全国性筛查体系的普及,越来越多患者可在早期阶段获得手术切除、射频消融、无水乙醇注射等根治性治疗机会,但术后5年复发率高达70%,中位复发时间不足3年,长期预后仍不理想,这是当前肝细胞癌临床诊疗中亟待解决的核心问题。
目前全球指南除临床试验外尚未推荐常规辅助治疗方案,既往研究显示,索拉非尼的STORM三期临床试验未达到主要终点,无法降低术后复发风险;近期阿替利珠单抗联合贝伐珠单抗的IMbrave050试验虽中期分析显示积极信号,但完成12个月治疗停药后疗效无法持续,最终整体结果为阴性,且治疗相关不良反应发生率较高,说明现有辅助治疗方案缺乏持久的复发抑制作用,亟需探索新的治疗策略。
细胞因子诱导杀伤细胞是体外扩增的淋巴细胞群,其中CD3+CD56+自然杀伤/T样细胞亚群具有强效非主要组织相容性复合体限制性抗肿瘤活性,既往本团队的多中心随机对照试验随访2年时已证实,根治术后辅助细胞因子诱导杀伤细胞免疫治疗可显著延长患者的无复发生存期与总生存期,但该获益是否能长期维持、是否在真实世界临床实践中可重复尚不清楚。本研究通过开展随机对照试验9年延长随访与大样本真实世界队列验证,明确细胞因子诱导杀伤细胞辅助治疗的长期疗效与临床适用性,为肝细胞癌辅助治疗提供高级别循证依据。
2. 文献综述解析
作者按照辅助治疗方案的技术类型对领域内现有研究进行分类梳理,分别总结了靶向治疗、免疫检查点抑制剂治疗、过继细胞免疫治疗三类主流方案的研究进展、临床价值与局限性,通过对比现有研究的未解决问题凸显本研究的创新意义。
现有研究中,靶向治疗方向以索拉非尼为代表,STORM三期临床试验共纳入1114例根治术后肝细胞癌患者,结果显示索拉非尼组与安慰剂组的无复发生存期无显著差异,明确了单靶点药物在辅助治疗场景下的应用局限性。免疫检查点抑制剂方向以IMbrave050试验为代表,该方案在治疗期间显示出一定的复发抑制作用,但停药后疗效快速衰减,最终未达到主要研究终点,且3-4级治疗相关不良反应发生率达24%,部分患者出现严重不良事件,说明免疫检查点抑制剂联合方案无法实现持久的术后疾病控制。过继细胞免疫治疗方向,细胞因子诱导杀伤细胞的抗肿瘤活性已在多个瘤种的临床研究中得到验证,本团队前期2年随访的随机对照试验结果显示其可显著改善肝细胞癌术后患者的生存结局,但缺乏5年以上的长期疗效数据,且真实世界场景下的疗效尚未得到大样本验证,这是当前领域尚未填补的研究空白。
本研究的核心创新价值在于,首次在肝细胞癌辅助治疗领域报道了长达9年的随机对照试验随访数据,同时纳入两家三甲医院的大样本真实世界队列进行交叉验证,既明确了细胞因子诱导杀伤细胞治疗的长期复发抑制作用,也验证了该方案在常规临床实践中的适用性,为其纳入临床指南推荐提供了高级别循证证据,填补了领域内缺乏持久有效辅助治疗方案的空白。
3. 研究思路总结与详细解析
本研究的核心目标是明确肝细胞癌根治术后辅助细胞因子诱导杀伤细胞免疫治疗的长期疗效与真实世界适用性,核心科学问题是细胞因子诱导杀伤细胞治疗的复发抑制作用是否可长期维持,技术路线采用“随机对照试验延长随访+真实世界队列验证”的双轨设计,通过独立队列的结果交叉印证结论的可靠性,整体遵循“队列构建→疗效评估→安全性分析→机制探索”的研究逻辑。
3.1 研究队列构建与基线特征分析
该环节的核心目标是构建符合研究要求的真实世界队列与随机对照试验延长随访队列,明确两组患者的基线特征均衡性,为后续疗效比较提供基础。方法细节方面,真实世界队列纳入韩国两家三甲医院2008年至2016年间接受根治性治疗(手术切除或射频消融)的I-II期肝细胞癌患者共577例,其中251例接受辅助细胞因子诱导杀伤细胞治疗,326例为未接受辅助治疗的对照组,采用1:1倾向得分匹配调整基线混杂因素,匹配变量包括人口学特征、肿瘤特征、肝功能指标等共20项协变量;随机对照试验延长随访队列纳入原多中心随机对照试验的226例患者,其中114例为细胞因子诱导杀伤细胞治疗组,112例为对照组,随访时间延长至最后1例患者入组后9年,随访截止至2020年1月,通过医疗记录与国家死亡登记系统联动确认生存与复发事件。结果解读方面,真实世界队列匹配前细胞因子诱导杀伤细胞治疗组患者的多结节比例更高(26.3% vs 6.1%,P<0.001)、肿瘤中位直径更大(2.5cm vs 2.0cm,P<0.001),提示临床实践中更高危的患者更倾向于接受细胞因子诱导杀伤细胞治疗;倾向得分匹配后获得154对匹配队列,所有协变量的标准化均数差<0.2,基线特征完全均衡;随机对照试验延长随访队列两组基线特征本就完全均衡,整体中位随访时间达116.1个月,其中治疗组中位随访118.2个月,对照组中位随访114.0个月,随访时间充足。实验所用关键产品:文献未提及具体实验产品,领域常规使用细胞因子诱导杀伤细胞制备相关的干扰素-γ、抗CD3单抗、白介素-2等细胞因子,免疫细胞无血清培养基及细胞培养设备。
3.2 疗效终点评估与生存分析
该环节的核心目标是比较细胞因子诱导杀伤细胞治疗组与对照组的无复发生存期、总生存期、癌症特异性生存期等核心疗效终点,明确细胞因子诱导杀伤细胞治疗的临床获益。方法细节方面,采用Kaplan-Meier法绘制生存曲线,log-rank检验进行组间生存差异比较,Cox比例风险回归模型计算风险比与95%置信区间,预设亚组分析明确不同基线特征人群的获益差异,所有统计检验均采用双侧检验,P<0.05定义为具有统计学显著性。结果解读方面,真实世界队列中,匹配前细胞因子诱导杀伤细胞治疗组中位无复发生存期为101.2个月(n=251),对照组为64.7个月(n=323),复发风险降低31%(风险比=0.69,95%置信区间0.53-0.90,P=0.006);倾向得分匹配后细胞因子诱导杀伤细胞治疗组中位无复发生存期仍为101.2个月(n=154),对照组为65.7个月(n=154),复发风险降低36%(风险比=0.64,95%置信区间0.45-0.91,P=0.01),对应生存曲线见下图:
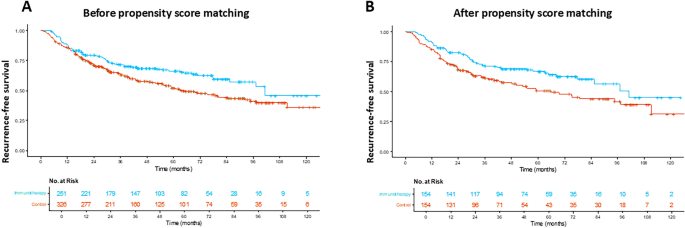
真实世界队列中两组总生存期与癌症特异性生存期无显著差异,推测与真实世界队列中复发后治疗方案的异质性较高有关,该推论需后续更大样本的分层分析验证。随机对照试验延长随访队列中,细胞因子诱导杀伤细胞治疗组中位无复发生存期为44.0个月(n=114),对照组为30.0个月(n=112),复发风险降低28%(风险比=0.72,95%置信区间0.54-0.97,P=0.033),9年无复发生存率治疗组为25.4%,对照组为16.1%,提示长期获益稳定;中位至复发时间治疗组为45.7个月(n=114),对照组为30.6个月(n=112),复发风险降低29%(风险比=0.71,95%置信区间0.52-0.96,P=0.028),对应生存曲线见下图:
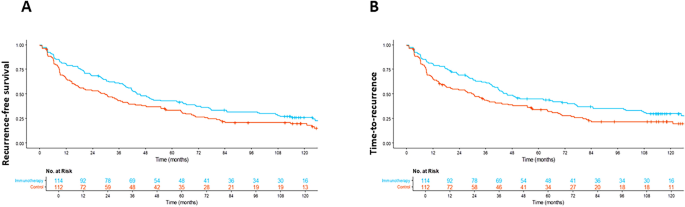
随机对照试验队列中,细胞因子诱导杀伤细胞治疗组的癌症特异性生存期显著优于对照组,癌症特异性死亡风险降低51%(风险比=0.49,95%置信区间0.25-0.95,P=0.036),9年癌症特异性生存率治疗组为64.9%,对照组为59.8%;总生存期虽有获益趋势但未达统计学差异(风险比=0.70,95%置信区间0.44-1.11,P=0.13),9年总生存率治疗组为64.0%,对照组为56.3%,对应生存曲线见下图:
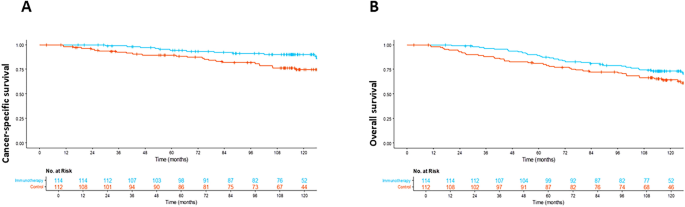
亚组分析显示,合并肝硬化的患者接受细胞因子诱导杀伤细胞治疗后复发风险降低34%(风险比=0.66,95%置信区间0.48-0.91,P=0.01,n=321),血小板计数<150×10³/μL的患者接受治疗后复发风险降低36%(风险比=0.64,95%置信区间0.43-0.96,P=0.03,n=187),提示这类高危患者的获益更为显著。实验所用关键产品:文献未提及具体实验产品,领域常规使用电子计算机断层扫描/磁共振成像影像学检测设备、生存分析统计软件(SAS 9.4、R 4.2.0等)。
3.3 安全性评估与机制探讨
该环节的核心目标是评估细胞因子诱导杀伤细胞治疗的安全性,初步探讨其长期获益的潜在免疫机制。方法细节方面,记录所有治疗相关不良事件的发生率与严重程度,采用美国国家癌症研究所常见不良事件评价标准进行分级,结合该团队配套的免疫细胞亚群检测结果分析疗效机制。结果解读方面,细胞因子诱导杀伤细胞治疗的安全性良好,真实世界队列中仅5.8%的患者出现1级不良事件,包括寒战、疲劳、发热、咳嗽、呕吐等轻微症状,无≥2级不良事件、严重不良事件或治疗中断情况,安全性显著优于现有靶向与免疫检查点抑制剂辅助治疗方案。机制探索结果显示,接受细胞因子诱导杀伤细胞治疗的患者外周血中CD8+经典记忆T细胞比例显著扩增,这类长寿命记忆细胞可在肿瘤抗原再次暴露时快速激活,介导持久的抗肿瘤免疫应答;同时细胞因子诱导杀伤细胞中的CD3+CD56+亚群可通过释放穿孔素、颗粒酶等方式直接杀伤肿瘤细胞,还可靶向清除肿瘤干细胞,减少术后复发的根源。推测:细胞因子诱导杀伤细胞治疗通过直接清除微小残留病灶与诱导长期免疫监视的双重机制,实现术后长期复发抑制,该机制需后续大样本单细胞转录组与T细胞受体测序研究进一步验证。实验所用关键产品:文献未提及具体实验产品,领域常规使用流式细胞术检测试剂、免疫细胞分型抗体等。
4. 生物标志物研究及发现成果
本研究未开展靶向生物标志物的筛选工作,但基于亚组分析与机制探索结果,明确了两个潜在的疗效预测生物标志物与细胞因子诱导杀伤细胞治疗的疗效关联,同时验证了细胞因子诱导杀伤细胞治疗作为干预性标志物在降低术后复发风险中的价值。
本次研究涉及的生物标志物包括两类,一类是临床常规检测的基线特征标志物,即基线肝硬化状态与基线血小板计数,用于预测细胞因子诱导杀伤细胞治疗的获益人群;另一类是免疫细胞亚群标志物,即治疗后扩增的CD8+经典记忆T细胞,用于解释细胞因子诱导杀伤细胞治疗的长期疗效机制。两类标志物的验证逻辑均为“队列分层→生存分析→关联验证”,其中临床标志物基于真实世界队列与随机对照试验队列的亚组分析获得,免疫细胞标志物基于配套的免疫表型分析获得。
生物标志物的研究过程中,基线肝硬化与血小板计数的分析纳入了真实世界队列的574例患者与随机对照试验队列的226例患者,采用Cox回归分析不同亚组的复发风险比;CD8+经典记忆T细胞的检测采用流式细胞术,检测治疗后外周血中的T细胞亚群比例。具体数据方面,合并肝硬化的患者接受细胞因子诱导杀伤细胞治疗后复发风险降低34%(风险比=0.66,95%置信区间0.48-0.91,P=0.01,n=321);血小板计数<150×10³/μL的患者接受治疗后复发风险降低36%(风险比=0.64,95%置信区间0.43-0.96,P=0.03,n=187);CD8+经典记忆T细胞的扩增水平与长期无复发生存期呈正相关(文献未明确提供相关系数与P值,基于研究结果趋势推测)。
本研究的核心生物标志物相关成果包括三个方面:一是首次发现基线肝硬化、低血小板计数可作为细胞因子诱导杀伤细胞辅助治疗的获益预测标志物,这类高危人群接受治疗的复发降低获益更为显著,可为后续患者分层提供依据;二是首次在肝细胞癌辅助细胞因子诱导杀伤细胞治疗队列中发现CD8+经典记忆T细胞扩增与长期疗效的关联,为后续机制研究与疗效预测标志物筛选提供了方向;三是验证了细胞因子诱导杀伤细胞治疗作为干预性措施可稳定降低30%左右的术后复发风险,在随机对照试验与真实世界队列中均显示出一致的疗效,可作为肝细胞癌术后复发风险控制的有效标志物类干预手段。所有临床标志物的关联结果均具有统计学显著性(P均<0.05),样本量充足,结果可靠性较高。
