1. 领域背景与文献引入
文献英文标题:Immunological effects of amivantamab in EGFR or MET-expressing non-small cell lung cancer;发表期刊:Cancer Immunology, Immunotherapy;影响因子:未公开;研究领域:肿瘤免疫治疗(非小细胞肺癌靶向免疫方向)。
领域共识:肺癌是全球癌症相关死亡的首要原因,其中非小细胞肺癌占比约85%,表皮生长因子受体(EGFR)突变是东亚人群非小细胞肺癌最常见的驱动突变,占比约50%。EGFR酪氨酸激酶抑制剂(EGFR-TKI)的应用显著改善了EGFR突变患者的预后,推动了非小细胞肺癌精准治疗的发展,但第三代EGFR-TKI奥希替尼的中位无进展生存期仍仅为12-16个月,获得性耐药是目前临床面临的核心瓶颈。MET原癌基因编码的受体酪氨酸激酶(MET)通路激活是EGFR-TKI获得性耐药的核心机制之一,埃万妥单抗作为EGFR/MET双特异性抗体,已获批用于EGFR外显子20插入突变的非小细胞肺癌治疗,现有临床前研究提示其可通过阻断受体信号、诱导抗体依赖的细胞毒性、吞噬作用等发挥抗肿瘤效应,但针对人临床样本中肿瘤浸润淋巴细胞的直接免疫调控作用尚未明确,也缺乏可靠的免疫效应预测生物标志物。本研究针对上述研究空白,基于40例非小细胞肺癌患者的手术新鲜样本开展实验,首次直接验证埃万妥单抗在人临床样本中的免疫激活效应,为其临床患者分层及扩大适用人群提供实验依据。
2. 文献综述解析
本研究文献综述部分按照“驱动突变靶向治疗发展→靶向药物的免疫调控效应→双特异性抗体的现有研究局限”的逻辑脉络展开评述,系统梳理了领域内现有研究的核心进展与不足。
现有研究的支持观点包括EGFR突变不仅通过激活下游信号通路驱动肿瘤细胞增殖,还可介导免疫抑制肿瘤微环境的形成,表现为CD8+T细胞、树突状细胞浸润减少,CD8+T细胞/调节性T细胞比例降低,抗肿瘤免疫应答受损;MET通路激活同样参与免疫抑制微环境的构建,可进一步加重EGFR-TKI治疗后的免疫抑制状态。现有技术方法的优势在于埃万妥单抗作为双特异性抗体,可同时阻断EGFR和MET的配体结合,介导受体内吞降解,同时其Fc段可招募自然杀伤细胞、巨噬细胞等固有免疫细胞,在临床前细胞系及动物模型中展现出显著的抗肿瘤活性,且在EGFR突变耐药患者的临床研究中已证实生存获益。现有研究的局限性在于,目前关于埃万妥单抗免疫效应的证据主要来自临床前模型,缺乏人新鲜临床肿瘤样本的直接验证,其免疫激活效应的影响因素及预测生物标志物尚未明确,无法支持临床精准分层用药。
本研究的创新价值在于首次利用人非小细胞肺癌手术切除的新鲜肿瘤样本构建体外肿瘤浸润淋巴细胞共培养体系,直接评估埃万妥单抗对人源免疫细胞的调控作用,突破了现有研究依赖临床前模型的局限性,同时明确了EGFR和MET蛋白表达作为其免疫激活效应预测标志物的潜在价值,为埃万妥单抗的临床应用及联合免疫治疗方案的开发提供了直接的实验依据。
3. 研究思路总结与详细解析
本研究的核心目标是明确埃万妥单抗在人非小细胞肺癌临床样本中的免疫调控效应,挖掘其免疫激活作用的预测生物标志物,核心科学问题是埃万妥单抗的免疫激活效应是否依赖于EGFR突变状态,是否可通过EGFR或MET蛋白表达水平进行预测,技术路线遵循“临床样本收集→基线免疫微环境分析→体外药物干预实验→标志物相关性验证→结论推导”的闭环逻辑,所有实验均基于临床真实样本开展,结果转化价值较高。
3.1 临床样本收集与基线免疫微环境分析
本环节的核心目标是明确EGFR突变非小细胞肺癌的基线免疫微环境特征,为后续药物效应分析提供基线参照。实验采用40例2023年12月至2024年12月在冈山大学医院接受手术切除的非小细胞肺癌患者的新鲜肿瘤组织,样本采集后立即分为两部分,一部分制备福尔马林固定石蜡包埋切片,用于免疫组化(IHC)检测CD8、CD11c、EGFR、MET蛋白表达,另一部分通过机械联合酶解法制备单细胞悬液,用于流式细胞术(FCM)分析免疫细胞表型,其中2例样本因组织量不足未纳入免疫组化分析。实验结果显示,免疫组化检测提示EGFR突变肿瘤的CD8+T细胞浸润呈降低趋势,树突状细胞浸润显著减少(文献未明确提供该数据,基于图表趋势推测,n=38);流式细胞术分析显示EGFR突变样本的CD8+T细胞/效应调节性T细胞比例、CD8+T细胞的程序性死亡受体1(PD-1)表达均呈降低趋势,而树突状细胞成熟标志物CD80、CD86表达与EGFR突变状态无显著相关性。实验所用关键产品:BD生物科学的肿瘤组织解离试剂(货号661563)、Cell Signaling Technology的CD8抗体(货号AB_2800052)、CD11c抗体(货号AB_2799286)、EGFR抗体(货号AB_2246311)、cMET抗体(货号AB_10858224)、免疫组化检测试剂盒(货号AB_10966207)、DAB底物试剂盒(货号AB_10796606)。
3.2 体外肿瘤浸润淋巴细胞功能实验构建
本环节的核心目标是建立人新鲜非小细胞肺癌样本的体外肿瘤浸润淋巴细胞共培养体系,直接评估埃万妥单抗的免疫调控效应。实验方法为将新鲜肿瘤制备的单细胞悬液接种于添加10%AB血清的RPMI-1640完全培养基中,分为不同处理组:CD3/CD28抗体刺激组、CD3/CD28抗体联合埃万妥单抗(0.5μg/mL)处理组,培养72小时后通过流式细胞术检测免疫细胞表型及细胞因子表达;其中树突状细胞及效应调节性T细胞的表型分析在无CD3/CD28刺激的条件下进行,以排除非特异性激活的干扰。实验结果对应流式细胞术分析图显示,埃万妥单抗处理后CD8+肿瘤浸润淋巴细胞的程序性死亡受体1表达、干扰素-γ分泌、肿瘤坏死因子-α分泌均显著升高,树突状细胞的CD80、CD86表达显著上调,而效应调节性T细胞的程序性死亡受体1、可诱导共刺激分子表达无显著变化(n=40,P<0.01),证实埃万妥单抗可直接激活人非小细胞肺癌中的抗肿瘤免疫应答。
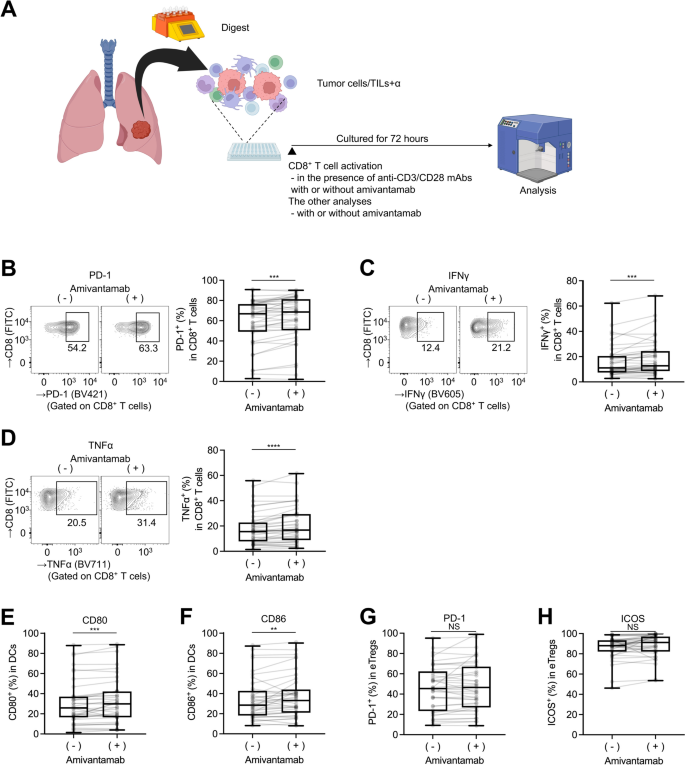
实验所用关键产品:BD生物科学的抗CD3抗体(货号AB_2869821)、赛默飞世尔科技的抗CD28抗体(货号AB_468926)、强生制药的埃万妥单抗(JNJ-61186372)、BD LSRFortessa X-20流式细胞仪。
3.3 EGFR突变状态与埃万妥单抗免疫效应的相关性分析
本环节的核心目标是验证埃万妥单抗的免疫激活效应是否仅局限于EGFR突变型非小细胞肺癌,明确其适用人群范围。实验根据临床常规检测的EGFR突变结果将样本分为EGFR突变组(13例)和EGFR野生型组(24例,3例未开展EGFR突变检测),分别分析两组经埃万妥单抗处理后的免疫细胞表型变化。实验结果对应分层分析图显示,EGFR突变组中埃万妥单抗可显著上调CD8+T细胞的程序性死亡受体1表达、干扰素-γ和肿瘤坏死因子-α分泌,同时促进树突状细胞CD80、CD86表达(n=13,P<0.05);而EGFR野生型组中同样观察到CD8+T细胞细胞因子分泌及树突状细胞成熟的显著上调(n=24,P<0.05),两组的效应调节性T细胞表型均无显著变化,提示埃万妥单抗的免疫激活效应不受EGFR突变状态的限制,EGFR野生型患者也可能从其治疗中获益。
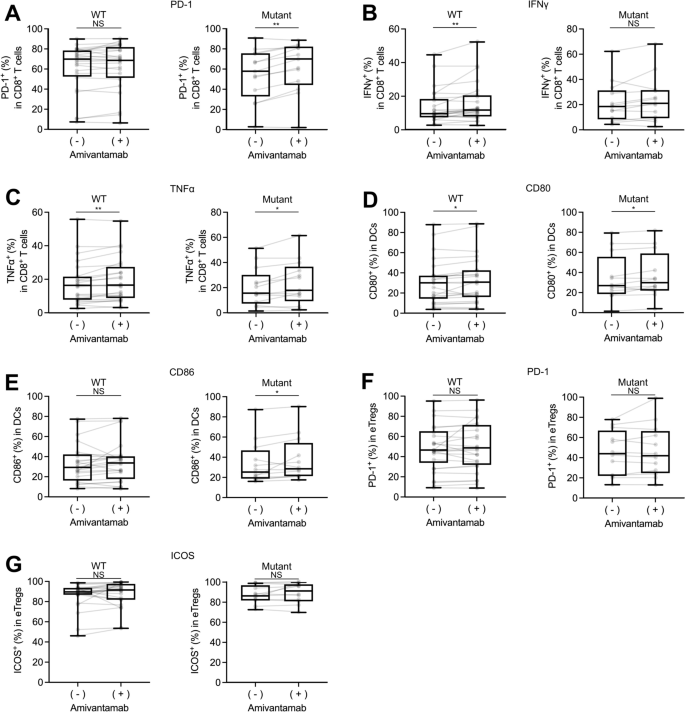
文献未提及该环节额外实验产品,领域常规使用核酸扩增类试剂进行EGFR突变检测。
3.4 EGFR/MET蛋白表达与埃万妥单抗免疫效应的相关性分析
本环节的核心目标是明确EGFR、MET蛋白表达水平对埃万妥单抗免疫激活效应的预测价值,挖掘可用于临床分层的生物标志物。实验通过免疫组化对EGFR、MET蛋白表达进行半定量评分,其中EGFR评分标准为≥10%肿瘤细胞出现中等及以上膜染色定义为高表达(≥2+),MET评分标准为≥50%肿瘤细胞出现中等及以上膜染色定义为高表达(≥2+),分层分析不同表达组的埃万妥单抗免疫调控效应差异。实验结果对应表达分层分析图显示,38例可评估样本中EGFR高表达占比66%(25/38),其中85%的EGFR突变样本为EGFR高表达,同时59%的EGFR野生型样本也呈EGFR高表达;MET高表达占比50%(19/38)。在EGFR高表达组中,埃万妥单抗可显著上调CD8+T细胞的程序性死亡受体1表达、干扰素-γ和肿瘤坏死因子-α分泌(n=25,P<0.05),并促进树突状细胞成熟,而EGFR低表达组中上述效应不显著;MET高表达组中同样观察到埃万妥单抗诱导的CD8+T细胞激活效应显著增强(n=19,P<0.05),MET低表达组中效应不显著。进一步将样本分为EGFR或MET至少一个高表达组和两者均低表达组,结果显示至少一个高表达组中埃万妥单抗的免疫激活效应显著,而两者均低表达组中无显著变化,提示EGFR或MET蛋白高表达可作为埃万妥单抗免疫激活效应的预测标志物。
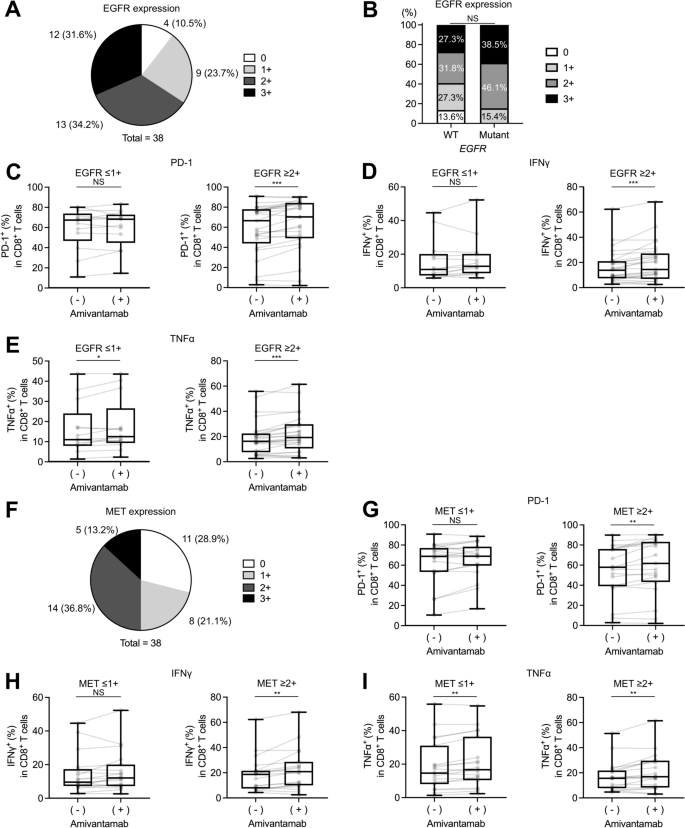
实验所用关键产品与3.1环节免疫组化试剂一致。
4. Biomarker研究及发现成果
本研究涉及的生物标志物为肿瘤组织EGFR和MET蛋白表达,属于肿瘤组织蛋白类预测标志物,筛选验证逻辑遵循“免疫组化半定量检测→单因素分层分析→联合分析验证”的完整链条,结果可靠性较高。
该生物标志物的检测样本为非小细胞肺癌患者手术切除的福尔马林固定石蜡包埋肿瘤组织,检测方法为免疫组化半定量评分,其中EGFR评分参考已发表的临床检测标准,≥10%肿瘤细胞出现中等及以上膜染色定义为高表达(≥2+),MET评分同样参考临床常规标准,≥50%肿瘤细胞出现中等及以上膜染色定义为高表达(≥2+)。针对埃万妥单抗免疫激活效应的预测价值分析显示,EGFR高表达样本中埃万妥单抗诱导CD8+T细胞干扰素-γ分泌的升高幅度显著高于低表达样本(n=38,P<0.01),MET高表达样本中该效应同样显著高于低表达样本(n=38,P<0.05);当EGFR和MET至少一个高表达时,预测埃万妥单抗免疫激活效应的特异性较高,文献未提供ROC曲线及AUC相关数据。
本研究的核心成果为EGFR或MET蛋白高表达可作为预测埃万妥单抗免疫激活效应的潜在生物标志物,创新性在于首次在人非小细胞肺癌临床新鲜样本中证实该标志物的预测价值,且其预测效能独立于EGFR突变状态,提示EGFR野生型但EGFR或MET高表达的患者也可能从埃万妥单抗治疗中获益,有望扩大埃万妥单抗的临床适用人群。统计学结果显示EGFR与MET表达水平呈显著正相关(Fisher精确检验,P=0.038,n=38),联合两个标志物的预测价值优于单个标志物。推测:EGFR/MET蛋白免疫组化检测可用于埃万妥单抗临床治疗的患者分层,其与免疫检查点抑制剂的联合方案也可能在EGFR或MET高表达人群中展现出更好的疗效,需后续大样本临床队列进一步验证。
