1. 领域背景与文献引入
文献英文标题:Protein-level profiling of TIGIT axis components in human PDAC reveals immune–suppressive expression patterns;发表期刊:Cancer Immunology, Immunotherapy;影响因子:未公开;研究领域:肿瘤免疫治疗(胰腺恶性肿瘤方向)。
胰腺导管腺癌是当前致死性最高的恶性实体瘤之一,原文数据显示其预计到2030年将成为全球第二大癌症相关死亡原因,5年总生存率不足10%,过去数十年间临床治疗进展极为有限,治疗耐药是制约患者生存的核心障碍。目前仅约20%的患者确诊时符合手术切除指征,多数患者确诊时已处于局部晚期或远处转移阶段,系统化疗仍是此类患者的主流治疗方案,包括FOLFIRINOX方案、吉西他滨联合白蛋白结合型紫杉醇方案等。
免疫检查点抑制剂的出现为多种恶性肿瘤的治疗带来了革命性突破,其中靶向程序性死亡蛋白1/程序性死亡配体1、细胞毒性T淋巴细胞相关蛋白4的免疫检查点抑制剂已在黑色素瘤、非小细胞肺癌等瘤种中取得显著临床获益,但此类药物在胰腺导管腺癌中的早期临床研究中,无论是单药还是联合用药均未显示出明确的客观应答,这一现象与胰腺导管腺癌高度免疫抑制的肿瘤微环境密切相关。该微环境中存在大量免疫抑制细胞群、功能失调的细胞毒性免疫细胞,共同介导肿瘤免疫逃逸与治疗耐药。
T细胞免疫球蛋白和ITIM结构域蛋白(TIGIT)是近年来新兴的免疫检查点分子,已被证实是胰腺导管腺癌免疫抑制的关键调控因子,其所属的调控轴包含TIGIT、DNAX辅助分子1(DNAM-1,又称CD226)、TACTILE(又称CD96)三类受体,可竞争性结合CD155、CD112等共有配体,调控免疫细胞的激活与细胞毒性功能,其中TIGIT通常可竞争性抑制DNAM-1的激活信号,介导肿瘤免疫逃逸。目前针对TIGIT的胰腺导管腺癌临床研究极少,部分TIGIT靶向临床试验甚至将胰腺导管腺癌患者排除入组,已开展的小样本TIGIT与程序性死亡蛋白1联合阻断临床试验也未显示出明确的治疗获益,提示当前对胰腺导管腺癌中TIGIT调控轴的蛋白水平表达特征、与程序性死亡蛋白1通路的关联仍缺乏深入解析,本研究正是针对这一研究空白,通过匹配的胰腺导管腺癌患者血液和肿瘤样本分析TIGIT调控轴组分的蛋白表达特征,为胰腺导管腺癌的免疫检查点联合治疗提供机制依据。
2. 文献综述解析
作者对领域内现有研究的分类围绕胰腺导管腺癌免疫治疗耐药机制、TIGIT调控轴的免疫调控功能、TIGIT靶向治疗的临床进展三个维度展开,系统梳理了领域内的研究进展与现存不足。
现有研究已明确胰腺导管腺癌的高度免疫抑制微环境是免疫检查点抑制剂疗效不佳的核心原因,TIGIT调控轴通过调控免疫细胞功能参与多种肿瘤的免疫逃逸过程,在其他瘤种中已证实程序性死亡蛋白1与TIGIT联合阻断具有潜在治疗价值,这些结论为TIGIT在胰腺导管腺癌中的研究提供了扎实的理论基础。技术层面,现有研究多采用转录组水平分析TIGIT调控轴的表达特征,部分预临床研究使用细胞系或动物模型验证TIGIT的功能,可在一定程度上反映通路的调控作用,但局限性在于缺乏胰腺导管腺癌患者临床样本的蛋白水平验证,同时针对TIGIT调控轴受体与配体在不同免疫细胞亚群、外周血和肿瘤微环境中的分布异质性分析不足,已开展的TIGIT靶向胰腺导管腺癌临床试验样本量极小,无法明确疗效差异的潜在机制。
本研究的创新价值在于首次在匹配的胰腺导管腺癌患者外周血与肿瘤组织样本中,同时从蛋白水平解析TIGIT调控轴所有关键受体及配体的表达分布特征,明确了不同免疫细胞亚群的TIGIT调控轴表达异质性,同时分析了其与程序性死亡蛋白1通路的共表达关联,填补了胰腺导管腺癌中TIGIT调控轴蛋白层面表达特征的研究空白,为后续联合免疫治疗临床试验的设计提供了直接的临床样本证据。
3. 研究思路总结与详细解析
本研究的核心目标是明确胰腺导管腺癌患者中TIGIT调控轴组分的蛋白表达特征及其与程序性死亡蛋白1/程序性死亡配体1表达的关联,揭示胰腺导管腺癌的免疫抑制机制,为后续免疫检查点联合靶向策略的开发提供依据。核心科学问题包括胰腺导管腺癌肿瘤微环境中TIGIT调控轴受体在不同免疫细胞亚群的表达模式、TIGIT调控轴配体在肿瘤组织中的分布特征、TIGIT调控轴与程序性死亡蛋白1通路的共表达关联三个层面。技术路线遵循“临床样本采集→多技术平台蛋白表达检测→公共数据库转录组验证→关联分析与机制推导”的逻辑闭环,首先纳入36例接受手术切除的胰腺导管腺癌患者,采集匹配的肿瘤组织与外周血样本,分别采用流式细胞术检测免疫细胞的TIGIT调控轴受体表达,免疫组化(IHC)检测肿瘤组织的配体表达,同时结合癌症基因组图谱(TCGA)/基因型-组织表达项目(GTEx)公共数据库的转录组数据验证配体的分布与基因表达特征,最终整合数据分析TIGIT调控轴的免疫抑制调控模式。
3.1 临床队列建立与样本预处理
实验目的为构建具有完整临床病理信息的胰腺导管腺癌患者队列,完成匹配的肿瘤组织与外周血样本的采集与预处理,为后续多维度表达分析提供合格的临床研究样本。方法细节方面,研究纳入36例在安特卫普大学医院接受手术切除(胰十二指肠切除术或远端胰腺切除术)的胰腺导管腺癌患者,其中男性25例、女性11例,平均年龄65岁,20%的患者接受过新辅助FOLFIRINOX治疗,75%的患者存在淋巴结转移,78%存在神经周浸润。术中采集新鲜肿瘤组织,切割为1-2mm³组织碎片后使用含10%二甲基亚砜的胎牛血清冻存于液氮,同时收集石蜡包埋肿瘤组织块;术中采集最多50mL外周血肝素抗凝样本,当日采用Ficoll密度梯度离心分离外周血单个核细胞,冻存于液氮中。结果解读显示,该队列涵盖IA至III期胰腺导管腺癌患者,包含匹配的血液与肿瘤组织样本,符合临床真实世界特征,可支持后续多维度表达分析。实验所用关键产品:GE Healthcare的Ficoll密度梯度离心试剂、Sigma-Aldrich的二甲基亚砜与脱氧核糖核酸酶试剂。
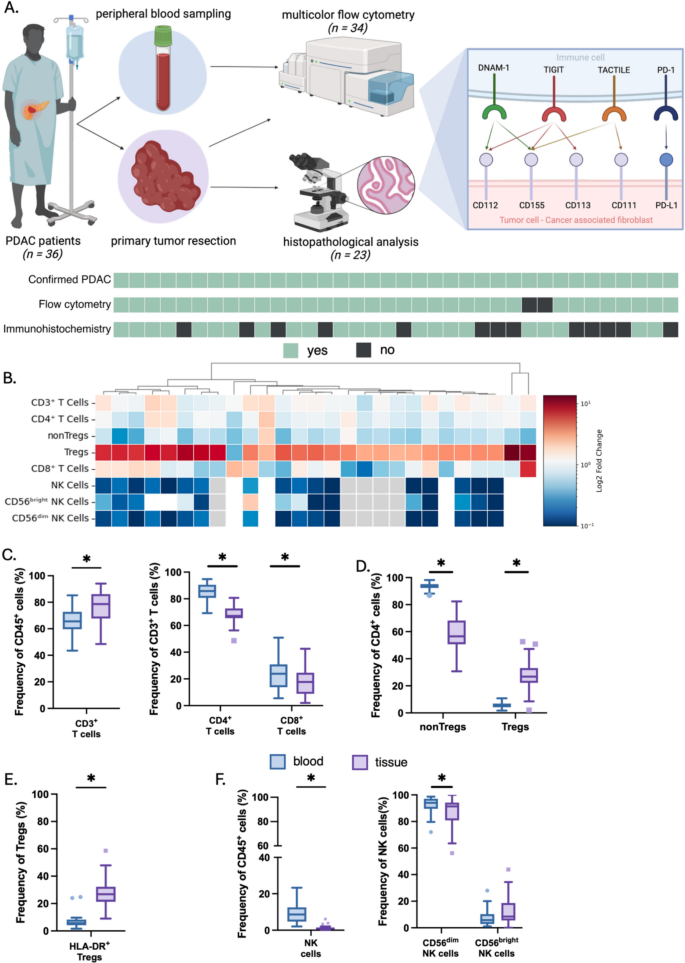
3.2 免疫细胞亚群与TIGIT调控轴受体表达的流式检测
实验目的为分析外周血与肿瘤组织中免疫细胞亚群的分布差异,以及各免疫细胞亚群中TIGIT调控轴受体(TIGIT、DNAM-1、TACTILE)的蛋白表达特征。方法细节方面,将冻存的外周血单个核细胞与肿瘤组织样本复苏后过夜静置,肿瘤组织使用2.5mg/mL胶原酶D与0.2mg/mL脱氧核糖核酸酶37℃振荡消化1小时制备单细胞悬液,所有样本使用10%正常人血清4℃封闭30分钟后,采用细胞表面抗体鸡尾酒试剂进行染色,4℃孵育30分钟后使用Agilent的NovoCyte Quanteon流式细胞仪采集数据,采用FlowJo软件进行分析。结果解读显示,流式检测的热图与箱线图结果显示,肿瘤组织中CD3+ T细胞总频率显著高于外周血,但CD4+与CD8+ T细胞的水平均显著低于外周血(n=36,P<0.05);调节性T细胞在肿瘤组织中显著富集,其中高免疫抑制性的HLA-DR阳性调节性T细胞比例显著升高,而非调节性CD4+ T细胞比例显著降低(n=36,P<0.05);自然杀伤细胞在肿瘤组织中的频率平均较外周血降低14.5倍,其中具有细胞毒性的CD56dim自然杀伤细胞比例显著下降,免疫调节型CD56bright自然杀伤细胞占比升高(n=36,P<0.05)。受体表达层面,所有肿瘤浸润淋巴细胞亚型的TIGIT表达均显著上调,其中调节性T细胞的TIGIT表达水平最高(n=36,P<0.05);活化受体DNAM-1在大部分肿瘤浸润免疫细胞亚型中表达显著降低,自然杀伤细胞中的下降最为显著,但调节性T细胞是唯一表现出DNAM-1表达上调的免疫细胞类型,且在HLA-DR阳性调节性T细胞中上调更为明显(n=36,P<0.05);TACTILE的表达在血液与肿瘤组织中整体差异较小,仅在肿瘤浸润调节性T细胞尤其是HLA-DR阳性调节性T细胞中出现显著富集(n=36,P<0.05)。上述结果证实胰腺导管腺癌肿瘤微环境中免疫细胞亚群向免疫抑制方向偏移,TIGIT调控轴受体的表达模式整体向抑制性倾斜。实验所用关键产品:Sigma-Aldrich的胶原酶D、BD Biosciences的FlowJo软件、Agilent的NovoCyte Quanteon流式细胞仪,文献未提及具体抗体品牌,领域常规使用肿瘤免疫研究相关的流式标记抗体。
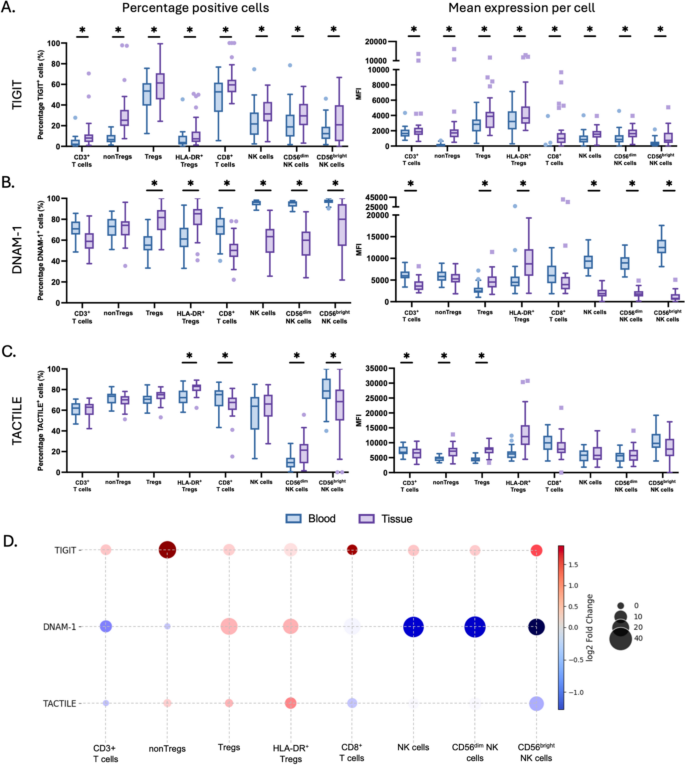
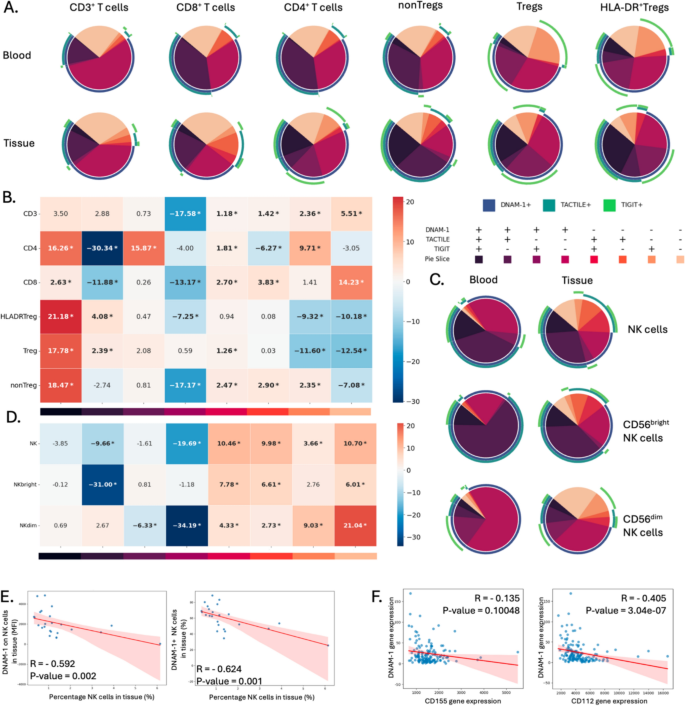
3.3 TIGIT调控轴受体共表达模式分析
实验目的为解析TIGIT调控轴三个受体的共表达特征,明确不同免疫细胞亚群的受体共表达异质性。方法细节方面,基于流式检测的三个受体表达数据,分析不同T细胞与自然杀伤细胞亚群中DNAM-1、TACTILE、TIGIT的共表达比例,采用线性混合效应模型进行组间差异统计,使用Benjamini-Hochberg法校正P值。结果解读显示,外周血中除HLA-DR阳性调节性T细胞有8%的三受体共阳性细胞外,其余T细胞亚群的三受体共阳性比例均低于4%;肿瘤组织中调节性T细胞的三受体共阳性比例最高,其中HLA-DR阳性调节性T细胞的三阳性比例达29%,而肿瘤浸润CD8+ T细胞中三个受体均阴性的细胞比例显著富集(n=36,校正后P<0.05)。自然杀伤细胞中,肿瘤组织内缺乏DNAM-1表达的自然杀伤细胞比例显著升高,且DNAM-1在自然杀伤细胞上的表达水平与肿瘤组织内自然杀伤细胞的浸润丰度呈负相关(Spearman相关系数R=-0.58,P<0.001),即自然杀伤细胞的DNAM-1表达越低,其在肿瘤内的浸润水平越低。癌症基因组图谱数据库的转录组数据分析显示,DNAM-1的基因表达与CD155(R=-0.32,P<0.001)、CD112(R=-0.28,P<0.001)的基因表达均呈负相关,推测:配体的高表达可能介导了DNAM-1的表达下调,需后续功能实验验证。上述结果证实调节性T细胞是胰腺导管腺癌肿瘤微环境中TIGIT调控轴受体共表达的主要细胞类群,DNAM-1的下调与自然杀伤细胞浸润不足相关。
3.4 TIGIT调控轴配体的免疫组化与转录组验证
实验目的为明确胰腺导管腺癌肿瘤组织中TIGIT调控轴配体(CD111、CD112、CD113、CD155)的表达与分布特征。方法细节方面,将石蜡包埋的胰腺导管腺癌肿瘤组织切片为5μm厚度,进行热诱导抗原修复后,采用免疫组化法检测CD111、CD112、CD113、CD155的表达,程序性死亡配体1的检测使用DAKO的PD-L1 IHC 22C3 pharmDx试剂盒在Agilent Omnis平台上完成,所有切片由经验丰富的病理医师进行判读;同时使用GEPIA2工具整合癌症基因组图谱的胰腺导管腺癌肿瘤数据与基因型-组织表达项目的正常胰腺组织数据,分析配体的基因表达差异,结合已发表的单细胞RNA测序数据分析配体在成纤维细胞亚群中的表达。结果解读显示,免疫组化结果显示CD112与CD155在胰腺导管腺癌肿瘤组织中广泛表达,首次发现CD112在肿瘤基质中也存在定位;癌症基因组图谱数据分析证实CD112与CD155在胰腺导管腺癌肿瘤组织中的基因表达水平显著高于正常胰腺组织,且在癌症相关成纤维细胞中存在高表达(n=179例肿瘤,n=171例正常,P<0.05)。实验所用关键产品:DAKO/Agilent的PD-L1 IHC 22C3 pharmDx试剂盒、Cell Signaling Technology的CD155抗体(货号81254)、Sigma-Aldrich的CD112抗体(货号HPA012759)、Santa Cruz Biotechnology的CD111抗体(货号sc-21722)、Sigma-Aldrich的CD113抗体(货号SAB1402559)、Philips的超高速切片扫描仪。
4. Biomarker研究及发现成果
本研究涉及的生物标志物主要为TIGIT调控轴的相关蛋白,包括TIGIT、DNAM-1及配体CD112、CD155,筛选逻辑遵循“临床样本蛋白水平检测→共表达特征分析→公共数据库转录组验证”的完整链条,明确其作为胰腺导管腺癌免疫治疗靶点与免疫抑制状态标志物的潜在价值。
TIGIT属于免疫检查点蛋白类生物标志物,DNAM-1属于免疫活化受体类生物标志物,CD112、CD155属于免疫检查点配体类生物标志物。筛选过程首先基于36例胰腺导管腺癌患者的匹配血液与肿瘤样本,通过流式细胞术与免疫组化检测蛋白表达,再结合癌症基因组图谱队列的转录组数据进行多维度验证。TIGIT的检测来源为肿瘤浸润淋巴细胞与外周血淋巴细胞,验证方法为流式细胞术,结果显示肿瘤浸润CD8+ T细胞与调节性T细胞的TIGIT表达水平较外周血显著上调,TIGIT与程序性死亡蛋白1在肿瘤浸润淋巴细胞中频繁共表达,该结果的样本量为36例,组间差异P<0.05。DNAM-1的检测来源同样为淋巴细胞,流式检测显示肿瘤内自然杀伤细胞与CD8+ T细胞的DNAM-1阳性比例显著降低,其表达水平与自然杀伤细胞浸润丰度呈负相关(Spearman相关系数R=-0.58,P<0.001)。CD112与CD155的检测来源为胰腺导管腺癌肿瘤组织,验证方法为免疫组化与转录组分析,结果显示二者在胰腺导管腺癌组织中广泛表达,且CD112存在基质定位特征,癌症基因组图谱队列中其表达显著高于正常胰腺组织(n=179例肿瘤,n=171例正常,P<0.05)。
核心成果方面,TIGIT在胰腺导管腺癌肿瘤微环境中普遍高表达,且与程序性死亡蛋白1频繁共表达,可作为胰腺导管腺癌免疫联合治疗的潜在靶点,创新性在于首次在蛋白水平证实胰腺导管腺癌中TIGIT的广泛上调与细胞分布特征;DNAM-1在效应免疫细胞中的下调与自然杀伤细胞浸润不足相关,提示恢复DNAM-1信号可作为改善胰腺导管腺癌免疫抑制的潜在策略;CD112与CD155的广泛表达为TIGIT调控轴的免疫抑制作用提供了配体基础,其中基质CD112的定位为首次报道。所有结果均经过统计学验证,其中受体表达的组间比较P值均<0.05,相关性分析的P值均<0.001。本研究未报道上述生物标志物的诊断敏感性、特异性及预后风险比数据,相关临床价值需后续大样本队列验证。
