1. 领域背景与文献引入
文献英文标题:IL-6 as a driver of bone invasion in IFIT2-depleted oral squamous cell carcinoma;发表期刊:Cancer Immunology, Immunotherapy;影响因子:未公开;研究领域:头颈部肿瘤(口腔鳞状细胞癌方向)。
口腔鳞状细胞癌(OSCC)是头颈部最常见的恶性肿瘤类型之一,具有侵袭性强、局部复发率高的特征,其中颌骨侵袭是OSCC进展的关键表型,会直接导致患者治疗难度提升、预后变差,是目前OSCC临床管理中的重点难点问题。领域共识:OSCC的骨侵袭过程依赖“肿瘤细胞-破骨细胞”的交互作用,OSCC细胞可分泌IL-6、核因子κB受体活化因子配体(RANKL)等多种促破骨细胞生成因子,诱导破骨前体细胞分化为成熟破骨细胞,介导骨基质溶解,而骨基质释放的生长因子又会进一步促进肿瘤细胞增殖和侵袭,形成“溶骨-肿瘤进展”的恶性循环,该机制的解析为OSCC骨侵袭的干预提供了潜在靶点,但目前针对该恶性循环的上游调控因子的研究仍存在较多空白。干扰素诱导四肽重复蛋白2(IFIT2)已被证实是OSCC的抑癌因子,其表达下调会促进OSCC的上皮间质转化、化疗耐药及远处转移,且可调控炎症因子的表达,但IFIT2是否参与OSCC骨侵袭的调控,以及其具体作用机制尚未阐明,也缺乏相关临床标志物的验证。本研究针对该研究空白,探究IFIT2缺失调控OSCC骨侵袭的分子机制,明确IL-6的核心介导作用,并验证IL-6/IFIT2轴的临床预后价值,为OSCC骨侵袭的靶向干预和预后评估提供新的理论依据。
2. 文献综述解析
作者对领域内现有研究的分类维度主要包括OSCC骨侵袭的病理机制、细胞因子在骨侵袭中的调控作用、IFIT2的肿瘤生物学功能三个方向,系统梳理了各方向的研究进展与局限性。
现有OSCC骨侵袭机制研究明确了破骨细胞是肿瘤诱导骨破坏的核心效应细胞,证实肿瘤分泌的多种细胞因子可通过激活破骨细胞分化驱动骨侵袭,该类研究为骨侵袭的干预提供了核心靶点,但尚未阐明不同促骨侵袭因子的上游调控网络,缺乏将抑癌因子功能与骨侵袭表型关联的机制研究。细胞因子调控方向的研究已将骨侵袭相关细胞因子分为IL-1超家族、TNF超家族、IL-17超家族、IL-6超家族、I型超家族、II型超家族六大类,证实IL-6、TNF-α等促炎因子在OSCC中表达升高,且OSCC条件培养基可在体外诱导破骨细胞分化,提示细胞因子是骨侵袭干预的潜在靶点,但现有研究多聚焦于单一细胞因子的功能验证,缺乏对抑癌因子调控细胞因子网络的系统性解析。IFIT2功能方向的研究已证实IFIT2作为干扰素刺激基因具有抗病毒功能,且在OSCC中发挥抑癌作用,其缺失会介导上皮间质转化、化疗耐药和转移表型,同时会上调TNF-α等炎症因子的表达,提示IFIT2可能参与肿瘤炎症微环境的调控,但目前尚无研究揭示IFIT2与OSCC骨侵袭表型的关联。本研究的创新价值在于首次将IFIT2的抑癌功能与OSCC骨侵袭表型关联,明确了IFIT2缺失通过上调IL-6表达促进破骨细胞分化和骨侵袭的机制,同时验证了IL-6/IFIT2轴作为OSCC预后标志物的临床价值,填补了IFIT2功能研究在骨侵袭方向的空白,为OSCC骨侵袭的靶向治疗提供了新的潜在靶点。
3. 研究思路总结与详细解析
本研究的核心研究目标是解析IFIT2调控OSCC骨侵袭的分子机制,明确IL-6在该过程中的核心介导作用,并验证IL-6及IL-6/IFIT2轴的临床预后价值。核心科学问题为IFIT2是否通过调控促破骨细胞因子的表达介导OSCC的骨侵袭,以及IL-6是否为该调控通路的关键效应分子。技术路线遵循“体外细胞功能验证→体内动物表型验证→分子机制解析→临床样本验证”的闭环逻辑:首先在OSCC细胞系中敲低IFIT2,检测细胞因子表达变化筛选关键效应分子;随后通过体外破骨细胞分化实验和体内移植瘤模型验证IFIT2缺失对骨侵袭的调控作用;再通过IL-6中和实验明确IL-6的介导功能;最后通过临床血清样本和组织芯片验证相关分子的临床意义。
3.1 IFIT2敲低细胞系构建与细胞因子表达检测
该环节的核心实验目的是验证IFIT2缺失对OSCC细胞细胞因子分泌谱的调控作用,筛选介导骨侵袭的关键效应分子。实验采用人OSCC细胞系CAL27,通过慢病毒转染构建稳定IFIT2敲低细胞株(sh-IFIT2#1、sh-IFIT2#2)和对照细胞株(sh-control),待细胞汇合度超过80%时更换无血清DMEM培养基培养24小时,收集细胞上清离心后得到条件培养基,采用液相芯片技术检测细胞因子谱的变化,同时通过实时荧光定量PCR(qRT-PCR)检测细胞中IL-6的mRNA表达水平。实验结果显示,与对照细胞株相比,IFIT2敲低细胞株中IL-6的mRNA水平显著升高,条件培养基中IL-6的分泌量也显著上调;体内荷瘤实验中,荷IFIT2敲低肿瘤的小鼠血清IL-6水平显著高于荷对照肿瘤的小鼠(n=5,P<0.001),而IL-10、IL-4等抗炎因子的表达无明显变化,提示IFIT2缺失可特异性上调OSCC细胞中IL-6的表达和分泌。对应实验结果图如下:
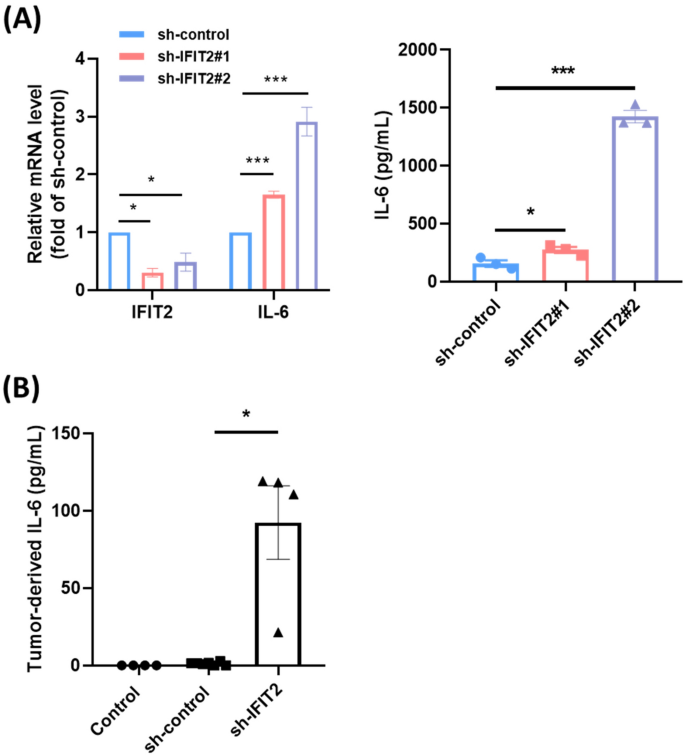
实验所用关键产品:Millipore的HCYTMAG-60 K-PX41细胞因子检测试剂盒,Molecular Research Center的TRI试剂,Life Technologies的SuperScript III第一链合成试剂盒,Roche的LightCycler 480实时荧光定量PCR系统。
3.2 IFIT2缺失调控骨侵袭的体内外功能验证
该环节的核心实验目的是明确IFIT2缺失是否可促进OSCC诱导的破骨细胞分化和体内骨侵袭。体外实验采用小鼠RAW 264.7破骨前体细胞,在添加50ng/ml RANKL的完全培养基中加入10%的IFIT2敲低株或对照株条件培养基,连续培养4天,每2天更换一次培养基,培养结束后通过抗酒石酸酸性磷酸酶(TRAP)染色计数成熟破骨细胞的数量和面积,通过F-肌动蛋白染色检测成熟破骨细胞特征性的肌动蛋白环形成情况,通过蛋白质免疫印迹检测破骨细胞分化标志物整合素β3(ITGB3)、基质金属蛋白酶9(MMP-9)、组织蛋白酶K(CTSK)的表达水平。体内实验采用雄性NOD/SCID小鼠,通过尾静脉注射5×10^5个IFIT2敲低株或对照株细胞,饲养8周后收集脊柱组织,通过微型计算机断层扫描(μCT)分析骨微结构参数,通过苏木精-伊红(HE)染色验证肿瘤细胞的骨侵袭情况。实验结果显示,体外实验中IFIT2敲低株条件培养基处理组的TRAP阳性破骨细胞总面积和平均面积显著高于对照组(n=3,P<0.0001),肌动蛋白环荧光强度显著升高(n=3,P<0.01),破骨细胞分化标志物的表达也显著上调;体内实验中荷IFIT2敲低肿瘤的小鼠脊柱可见明显的肿瘤细胞浸润骨组织,μCT分析显示其骨体积分数(BV/TV)、骨小梁厚度(Tb.Th)、骨小梁数量(Tb.N)均显著低于对照组(n=5,P<0.001),提示IFIT2缺失可通过增强破骨细胞的分化和激活促进OSCC的骨侵袭。对应实验结果图如下:
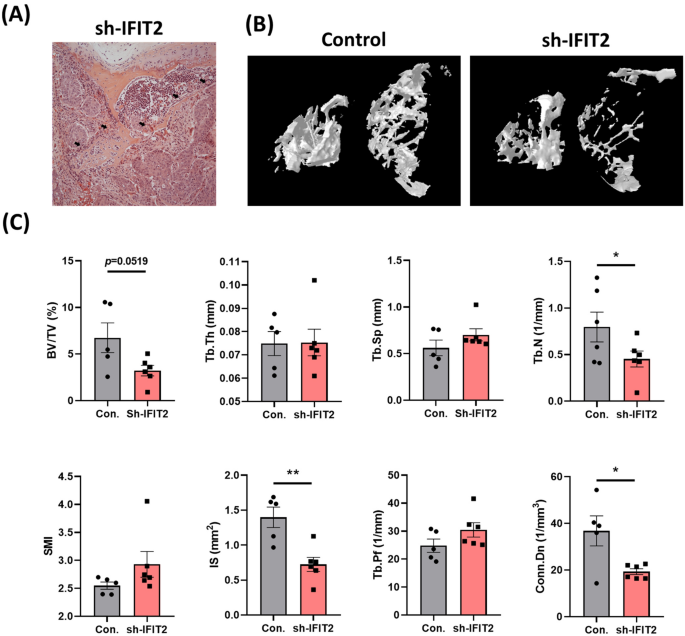
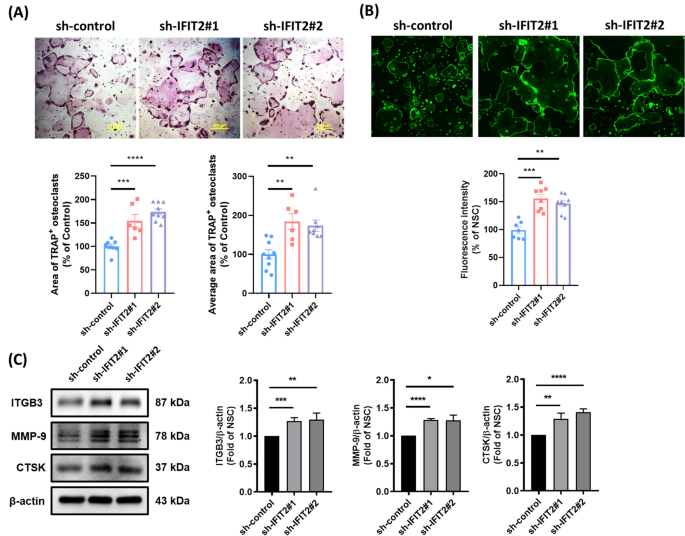
实验所用关键产品:Sigma-Aldrich的抗酒石酸酸性磷酸酶染色试剂盒(货号387-A),Abnova的F-肌动蛋白染色试剂盒(货号KA4116),GeneTex的抗整合素β3抗体(货号GTX02823)、抗基质金属蛋白酶9抗体(货号GTX04573),Abcam的抗组织蛋白酶K抗体(货号ab19027),Sigma的抗β-肌动蛋白抗体(货号A5441),Bruker的Skyscan 1276微型计算机断层扫描系统。
3.3 IL-6介导破骨细胞分化的功能验证
该环节的核心实验目的是明确IL-6是否是IFIT2缺失诱导破骨细胞分化的关键介导因子。实验在IFIT2敲低株条件培养基处理RAW 264.7细胞的培养体系中,分别加入IL-6中和抗体或IgG同型对照,连续培养4天后,采用与上述相同的方法检测TRAP阳性破骨细胞数量、肌动蛋白环形成情况以及破骨细胞分化标志物的表达水平。实验结果显示,加入IL-6中和抗体后,IFIT2敲低株条件培养基诱导的TRAP阳性破骨细胞形成被显著抑制(n=3,P<0.0001),肌动蛋白环的荧光强度显著降低(n=3,P<0.001),破骨细胞分化标志物整合素β3、基质金属蛋白酶9、组织蛋白酶K的表达也显著下调,提示阻断IL-6可逆转IFIT2缺失诱导的破骨细胞分化,证实IL-6是IFIT2缺失介导OSCC骨侵袭的关键效应分子。对应实验结果图如下:
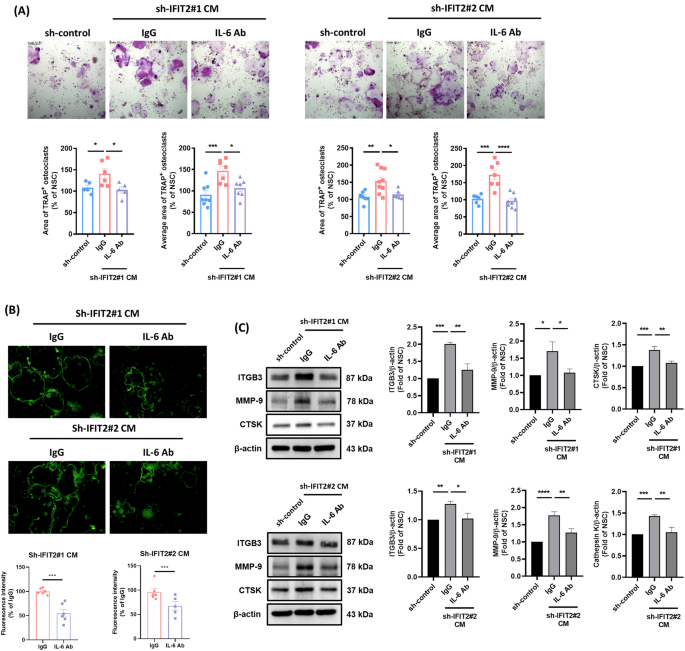
实验所用关键产品:文献未提及IL-6中和抗体的具体品牌,领域常规使用抗人IL-6中和抗体类试剂进行相关阻断实验。
3.4 临床样本中IL-6及IL-6/IFIT2轴的临床意义验证
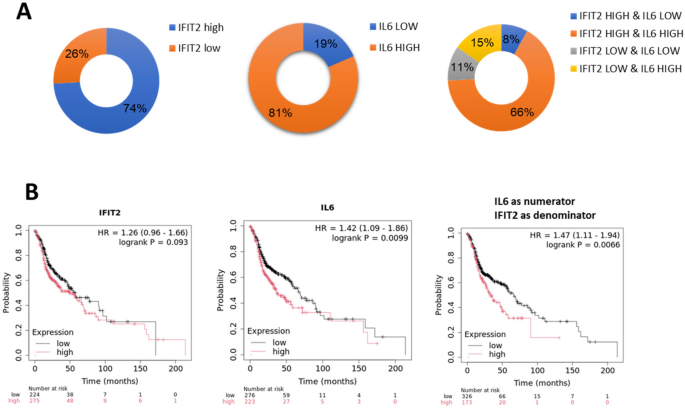
该环节的核心实验目的是验证IL-6的临床相关性,以及IL-6/IFIT2轴作为OSCC预后标志物的价值。实验收集47例OSCC患者的血清样本,采用液相芯片技术检测血清中IL-6的水平,分析其与患者肿瘤分期、淋巴结转移等临床病理特征的相关性,同时通过斯皮尔曼等级相关分析IL-6与其他细胞因子的表达相关性。采用商业口腔癌组织芯片(包含73例口腔癌、18例咽/下咽癌、11例正常口腔组织),通过免疫组化(IHC)检测组织中IL-6和IFIT2的表达水平,结合TCGA数据库的生存数据分析IL-6/IFIT2表达比值与患者预后的关系。实验结果显示,T4期OSCC患者的血清IL-6水平为22.21pg/ml,显著高于T1-T3期患者的11.04pg/ml(n=47,P=0.027);Ⅳ期患者的血清IL-6水平为21.31pg/ml,显著高于Ⅰ-Ⅲ期患者的11.68pg/ml(n=47,P=0.043);存在淋巴结转移的患者血清IL-6水平为24.38pg/ml,显著高于无淋巴结转移患者的14.4pg/ml(n=47,P=0.027)。相关性分析显示血清IL-6水平与G-CSF(r=0.706,P<0.0001)、VEGF-α(r=0.454,P<0.01)等促瘤细胞因子呈显著正相关。组织芯片分析显示77%的患者中IL-6与IFIT2的表达呈正相关,23%的患者呈负相关;生存分析显示高IL-6/IFIT2比值的患者中位生存期为32.93个月,显著低于低比值患者的66.73个月(P<0.01),提示IL-6/IFIT2轴可作为OSCC的预后评估标志物。对应实验结果图如下:
实验所用关键产品:Pantomics的口腔癌组织芯片(货号ORC1021),Millipore的HCYTMAG-60 K-PX41细胞因子检测试剂盒。
4. Biomarker 研究及发现成果
本研究涉及的生物标志物包括血清IL-6和肿瘤组织IL-6/IFIT2表达比值,分别属于体液蛋白标志物和组织蛋白标志物,其筛选验证逻辑为“细胞系水平分子调控关系验证→动物模型功能验证→临床血清样本病理特征相关性分析→组织芯片预后价值验证”,逻辑链条完整,为后续临床转化提供了扎实的基础。
血清IL-6来源于OSCC患者的外周血血清,采用液相芯片技术进行定量检测,检测结果显示血清IL-6水平与OSCC的肿瘤进展显著相关:T4期患者血清IL-6水平较T1-T3期升高101.2%(n=47,P=0.027),Ⅳ期患者较Ⅰ-Ⅲ期升高82.4%(n=47,P=0.043),伴淋巴结转移患者较无转移患者升高69.3%(n=47,P=0.027),同时血清IL-6与G-CSF、VEGF-α等促瘤细胞因子呈显著正相关,提示其可作为OSCC进展的辅助监测标志物。文献未明确提供血清IL-6单独诊断OSCC骨侵袭的敏感性、特异性及ROC曲线下面积数据,相关诊断效能需后续扩大样本量进一步验证。
IL-6/IFIT2表达比值来源于OSCC患者的肿瘤组织石蜡切片,采用免疫组化检测两种蛋白的表达水平后计算比值,生存分析显示高IL-6/IFIT2比值患者的中位生存期较低比值患者缩短33.8个月(n=73,P<0.01),提示该比值可作为OSCC的预后评估标志物,其创新性在于首次将IFIT2的表达水平与IL-6联合作为预后评估指标,明确了IFIT2缺失介导IL-6上调的调控关系在OSCC进展中的临床意义,为OSCC的预后分层提供了新的参考指标。本研究未验证该比值在其他肿瘤类型中的普适性,后续可开展多中心、大样本研究进一步确认其临床应用价值。
